Tabla Periódica de los Elementos
# Atómico
Electrones
Símbolo
Nombre
Peso Atómico
3
2
1
Li
Litio
6,94
4
2
2
Be
Berilio
9,0122
5
2
3
B
Boro
10,81
6
2
4
C
Carbono
12,011
7
2
5
N
Nitrógeno
14,007
8
2
6
O
Oxígeno
15,999
9
2
7
F
Flúor
18,998
10
2
8
Ne
Neón
20,180
11
2
8
1
Na
Sodio
22,990
12
2
8
2
Mg
Magnesio
24,305
13
2
8
3
Al
Aluminio
26,982
14
2
8
4
Si
Silicio
28,085
15
2
8
5
P
Fósforo
30,974
16
2
8
6
S
Azufre
32,06
17
2
8
7
Cl
Cloro
39,948
18
2
8
8
Ar
Argón
39,948
19
2
8
8
1
K
Potasio
39,098
20
2
8
8
2
Ca
Calcio
40,078
21
2
8
9
2
Sc
Escandio
44,956
22
2
8
10
2
Ti
Titanio
47,867
23
2
8
11
2
V
Vanadio
50,942
24
2
8
13
1
Cr
Cromo
51,996
25
2
8
13
2
Mn
Manganeso
54,938
26
2
8
14
2
Fe
Hierro
55,845
27
2
8
15
2
Co
Cobalto
58,933
28
2
8
16
2
Ni
Níquel
58,693
29
2
8
18
1
Cu
Cobre
63,546
30
2
8
18
2
Zn
Cinc
65,38
31
2
8
18
3
Ga
Galio
69,723
32
2
8
18
4
Ge
Germanio
72,630
33
2
8
18
5
As
Arsénico
74,922
34
2
8
18
6
Se
Selenio
78,971
35
2
8
18
7
Br
Bromo
79,904
36
2
8
18
8
Kr
Kriptón
83,798
37
2
8
18
8
1
Rb
Rubidio
85,468
38
2
8
18
8
2
Sr
Estroncio
87,62
39
2
8
18
9
2
Y
Itrio
88,906
40
2
8
18
10
2
Zr
Circonio
91,224
41
2
8
18
12
1
Nb
Niobio
92,906
42
2
8
18
13
1
Mo
Molibdeno
95,95
43
2
8
18
13
2
Tc
Tecnecio
(98)
44
2
8
18
15
1
Ru
Rutenio
101,07
45
2
8
18
16
1
Rh
Rodio
102,91
46
2
8
18
18
Pd
Paladio
106,42
47
2
8
18
18
1
Ag
Plata
107,87
48
2
8
18
18
2
Cd
Cadmio
112,41
49
2
8
18
18
3
In
Indio
114,82
50
2
8
18
18
4
Sn
Estaño
118,71
51
2
8
18
18
5
Sb
Antimonio
121,76
52
2
8
18
18
6
Te
Telurio
127,60
53
2
8
18
18
7
I
Yodo
126,90
54
2
8
18
18
8
Xe
Xenón
131,29
55
2
8
18
18
8
1
Cs
Cesio
132,91
56
2
8
18
18
8
2
Ba
Bario
137,33
57
2
8
18
18
9
2
La
Lantano
138,91
72
2
8
18
32
10
2
Hf
Hafnio
178,49
73
2
8
18
32
11
2
Ta
Tantalio
180,95
74
2
8
18
32
12
2
W
Wolframio
183,84
75
2
8
18
32
13
2
Re
Renio
186,21
76
2
8
18
32
14
2
Os
Osmio
190,23
77
2
8
18
32
15
2
Ir
Iridio
192,22
78
2
8
18
32
17
1
Pt
Platino
195,08
79
2
8
18
32
18
1
Au
Oro
196,97
80
2
8
18
32
18
2
Hg
Mercurio
200,59
81
2
8
18
32
18
3
Tl
Talio
204,38
82
2
8
18
32
18
4
Pb
Plomo
207,2
83
2
8
18
32
18
5
Bi
Bismuto
208,98
84
2
8
18
32
18
6
Po
Polonio
(209)
85
2
8
18
32
18
7
At
Astato
(210)
86
2
8
18
32
18
8
Rn
Radón
(222)
87
2
8
18
32
18
8
1
Fr
Francio
(223)
88
2
8
18
32
18
8
2
Ra
Radio
(226)
89
2
8
18
32
18
9
2
Ac
Actinio
(227)
104
2
8
18
32
32
10
2
Rf
Rutherfordio
(267)
105
2
8
18
32
32
11
2
Db
Dubnio
(268)
106
2
8
18
32
32
12
2
Sg
Seaborgio
(269)
107
2
8
18
32
32
13
2
Bh
Bohrio
(270)
108
2
8
18
32
32
14
2
Hs
Hassio
(277)
109
2
8
18
32
32
15
2
Mt
Meitnerio
(278)
110
2
8
18
32
32
17
1
Ds
Darmstatio
(281)
111
2
8
18
32
32
17
2
Rg
Roentgenio
(282)
112
2
8
18
32
32
18
2
Cn
Copernicio
(285)
113
2
8
18
32
32
18
3
Nh
Nihonium
(286)
114
2
8
18
32
32
18
4
Fl
Flerovio
(289)
115
2
8
18
32
32
18
5
Mc
Moscovium
(290)
116
2
8
18
32
32
18
6
Lv
Livermorio
(293)
117
2
8
18
32
32
18
7
Ts
Tennessine
(294)
118
2
8
18
32
32
18
8
Og
Oganesson
(294)
58
2
8
18
19
9
2
Ce
Cerio
140,12
59
2
8
18
21
8
2
Pr
Praseodimio
140,91
60
2
8
18
22
8
2
Nd
Neodimio
144,24
61
2
8
18
23
8
2
Pm
Prometio
(145)
62
2
8
18
24
8
2
Sm
Samario
150,36
63
2
8
18
25
8
2
Eu
Europio
151,96
64
2
8
18
25
9
2
Gd
Gadolinio
157,25
65
2
8
18
27
8
2
Tb
Terbio
158,93
66
2
8
18
28
8
2
Dy
Disprosio
162,50
67
2
8
18
29
8
2
Ho
Holmio
164,93
68
2
8
18
30
8
2
Er
Erbio
167,26
69
2
8
18
31
8
2
Tm
Tulio
168,93
70
2
8
18
32
8
2
Yb
Iterbio
173,05
71
2
8
18
32
9
2
Lu
Lutecio
174,97
90
2
8
18
32
18
9
2
Th
Torio
232,04
91
2
8
18
32
20
9
2
Pa
Protactinio
231,04
92
2
8
18
32
21
9
2
U
Uranio
238,03
93
2
8
18
32
22
9
2
Np
Neptunio
(237)
94
2
8
18
32
24
8
2
Pu
Plutonio
(244)
95
2
8
18
32
25
8
2
Am
Americio
(247)
96
2
8
18
32
25
9
2
Cm
Curio
(247)
97
2
8
18
32
27
8
2
Bk
Berkelio
(247)
98
2
8
18
32
28
8
2
Cf
Californio
(251)
99
2
8
18
32
29
8
2
Es
Einstenio
(252)
100
2
8
18
32
30
8
2
Fm
Fermio
(257)
101
2
8
18
32
31
8
2
Md
Mendelevio
(258)
102
2
8
18
32
32
8
2
No
Nobelio
(259)
103
2
8
18
32
32
8
3
Lr
Lawrencio
(266)
Hidrógeno
El hidrógeno (en griego, de ὕδωρ hýdōr, genitivo ὑδρός hydrós, y γένος génos «que genera o produce agua») es el elemento químico de número atómico 1, representado por el símbolo H. Con una masa atómica de 1,00797 es el más ligero de la tabla periódica de los elementos. Por lo general, se presenta en su forma molecular, formando el gas diatómico H2 en condiciones normales. Este gas es inflamable, incoloro, inodoro, no metálico e insoluble en agua.
Debido a sus distintas y variadas propiedades, el hidrógeno no se puede encuadrar claramente en ningún grupo de la tabla periódica, aunque muchas veces se sitúa en el grupo 1 (o familia 1A) por poseer un solo electrón en la capa de valencia o capa superior.
El hidrógeno es el elemento químico más abundante, al constituir aproximadamente el 75 % de la materia visible del universo. En su secuencia principal, las estrellas están compuestas principalmente por hidrógeno en estado de plasma. El hidrógeno elemental es relativamente raro en la Tierra y es producido industrialmente a partir de hidrocarburos como, por ejemplo, el metano. La mayor parte del hidrógeno elemental se obtiene in situ, es decir, en el lugar y en el momento en que se necesita. Los mayores mercados del mundo disfrutan de la utilización del hidrógeno para el mejoramiento de combustibles fósiles (en el proceso de hidrocraqueo) y en la producción de amoníaco (principalmente para el mercado de fertilizantes). El hidrógeno puede obtenerse a partir del agua por un proceso de electrólisis, pero resulta un método mucho más caro que la obtención a partir del gas natural.
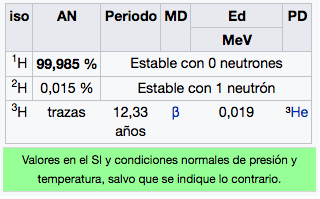
El isótopo del hidrógeno más común es el protio, cuyo núcleo está formado por un único protón y ningún neutrón. En los compuestos iónicos, puede tener una carga positiva (convirtiéndose en un catión llamado hidrón, H+, compuesto únicamente por un protón, a veces en presencia de 1 o 2 neutrones); o carga negativa (convirtiéndose en un anión conocido como hidruro, H-). También se pueden formar otros isótopos, como el deuterio, con un neutrón, y el tritio, con dos neutrones. En 2001, fue creado en laboratorio el isótopo 4H y, a partir de 2003, se sintetizaron los isótopos 5H hasta 7H. El hidrógeno forma compuestos con la mayoría de los elementos y está presente en el agua y en la mayoría de los compuestos orgánicos. Tiene un papel particularmente importante en la química ácido-base, en la que muchas reacciones implican el intercambio de protones (iones hidrógeno, H+) entre moléculas solubles. Puesto que es el único átomo neutro para el que se puede resolver analíticamente la ecuación de Schrödinger, el estudio de la energía y del enlace del átomo de hidrógeno ha sido fundamental hasta el punto de haber desempeñado un papel principal en el desarrollo de la mecánica cuántica.
Las características de este elemento y su solubilidad en diversos metales son muy importantes en la metalurgia, puesto que muchos metales pueden sufrir fragilidad en su presencia, y en el desarrollo de formas seguras de almacenarlo para su uso como combustible. Es altamente soluble en diversos compuestos que poseen tierras raras y metales de transición, y puede ser disuelto tanto en metales cristalinos como amorfos. La solubilidad del hidrógeno en los metales está influenciada por las distorsiones locales o impurezas en la estructura cristalina del metal.
Etimología
El término hidrógeno proviene del latín hydrogenium, y este del griego antiguo ὕδωρ (hydro): ‘agua’ y γένος-ου(genos): ‘generador’; es decir, «productor de agua». Fue ese el nombre con el que lo bautizó Antoine Lavoisier. La palabra puede referirse tanto al átomo de hidrógeno, descrito en este artículo, como a la molécula diatómica (H2), que se encuentra a nivel de trazas en la atmósfera terrestre. Los químicos tienden a referirse a esta molécula como dihidrógeno, molécula de hidrógeno, o hidrógeno diatómico, para distinguirla del átomo del elemento, que no existe de forma aislada en las condiciones ordinarias.
Historia
Descubrimiento del hidrógeno y uso
El hidrógeno diatómico gaseoso, H2, fue el primero producido artificialmente y formalmente descrito por T. von Hohenheim (más conocido como Paracelso), que lo obtuvo artificialmente mezclando metales con ácidos fuertes. Paracelso no era consciente de que el gas inflamable generado en estas reacciones químicas estaba compuesto por un nuevo elemento químico. En 1671, Robert Boyle redescubrió y describió la reacción que se producía entre limaduras de hierro y ácidos diluidos, lo que resulta en la producción de gas hidrógeno. En 1766, Henry Cavendish fue el primero en reconocer el hidrógeno gaseoso como una sustancia discreta, identificando el gas producido en la reacción metal-ácido como «aire inflamable» y descubriendo más profundamente, en 1781, que el gas produce agua cuando se quema. Generalmente, se le da el crédito por su descubrimiento como un elemento químico. En 1783, Antoine Lavoisier dio al elemento el nombre de hidrógeno (del griego υδρώ (hydro), agua y γένος-ου (genes) generar, es decir, «productor de agua») cuando él y Laplace reprodujeron el descubrimiento de Cavendish, donde se produce agua cuando se quema hidrógeno.
Lavoisier produjo hidrógeno para sus experimentos sobre conservación de la masa haciendo reaccionar un flujo de vapor con hierro metálico a través de un tubo de hierro incandescente calentado al fuego. La oxidación anaerobia de hierro por los protones del agua a alta temperatura puede ser representada esquemáticamente por el conjunto de las siguientes reacciones:
- Fe + H2O → FeO + H2
- 2 Fe + 3 H2O → Fe2O3 + 3 H2
- 3 Fe + 4 H2O → Fe3O4 + 4 H2
Muchos metales, tales como circonio, se someten a una reacción similar con agua, lo que conduce a la producción de hidrógeno.
El hidrógeno fue licuado por primera vez por James Dewar en 1898 al usar refrigeración regenerativa, y su invención se aproxima mucho a lo que conocemos hoy en día como termo. Produjo hidrógeno sólido al año siguiente. El deuterio fue descubierto en diciembre de 1931 por Harold Urey, y el tritio fue preparado en 1934 por Ernest Rutherford, Marcus Oliphant, y Paul Harteck. El agua pesada, que tiene deuterio en lugar de hidrógeno regular en la molécula de agua, fue descubierta por el equipo de Urey en 1932.
François Isaac de Rivaz construyó el primer dispositivo de combustión interna propulsado por una mezcla de hidrógeno y oxígeno en 1806. Edward Daniel Clarke inventó el rebufo de gas de hidrógeno en 1819. La lámpara de Döbereiner y la Luminaria Drummond fueron inventadas en 1823.
El llenado del primer globo con gas hidrógeno fue documentado por Jacques Charles en 1783. El hidrógeno proveía el ascenso a la primera manera confiable de viajes aéreos después de la invención del primer dirigible de hidrógeno retirado en 1852 por Henri Giffard. El conde alemán Ferdinand von Zeppelin promovió la idea de utilizar el hidrógeno en dirigibles rígidos, que más tarde fueron llamados zepelines, el primero de los cuales tuvo su vuelo inaugural en 1900. Los vuelos normales comenzaron en 1910, y para el inicio de la Primera Guerra Mundial, en agosto de 1914, se había trasladado a 35 000 pasajeros sin ningún incidente grave. Los dirigibles elevados con hidrógeno se utilizan como plataformas de observación y bombarderos durante la guerra.
La primera travesía transatlántica sin escalas fue hecha por el dirigible británico R34 en 1919. A partir de 1928, con el Graf Zeppelin LZ 127, el servicio regular de pasajeros prosiguió hasta mediados de la década de 1930 sin ningún incidente. Con el descubrimiento de las reservas de otro tipo de gas ligero en los Estados Unidos, este proyecto debió ser modificado, ya que el otro elemento prometió más seguridad, pero el Gobierno de Estados Unidos se negó a vender el gas a tal efecto. Por lo tanto, el H2 fue utilizado en el dirigible Hindenburg, que resultó destruido en un incidente en vuelo sobre Nueva Jersey el 6 de mayo de 1937. El incidente fue transmitido en vivo por radio y filmado. El encendido de una fuga de hidrógeno se atribuyó como la causa del incidente, pero las investigaciones posteriores señalaron a la ignición del revestimiento de tejido aluminizado por la electricidad estática.
Abundancia en la naturaleza
El hidrógeno es el elemento químico más abundante del universo, suponiendo más del 75 % en materia normal por masa y más del 90 % en número de átomos. Este elemento se encuentra en abundancia en las estrellas y los planetas gaseosos gigantes. Las nubes moleculares de H2 están asociadas a la formación de las estrellas. El hidrógeno también juega un papel fundamental como combustible de las estrellas por medio de las reacciones de fusión nuclear entre núcleos de hidrógeno.
En el universo, el hidrógeno se encuentra principalmente en su forma atómica y en estado de plasma, cuyas propiedades son bastante diferentes a las del hidrógeno molecular. Como plasma, el electrón y el protón del hidrógeno no se encuentran ligados, por lo que presenta una alta conductividad eléctrica y una gran emisividad (origen de la luz emitida por el Sol y otras estrellas). Las partículas cargadas están fuertemente influenciadas por los campos eléctricos y magnéticos. Por ejemplo, en los vientos solares las partículas interaccionan con la magnetosfera terrestre generando corrientes de Birkeland y el fenómeno de las auroras.
Bajo condiciones normales de presión y temperatura, el hidrógeno existe como gas diatómico, H2. Sin embargo, el hidrógeno gaseoso es extremadamente poco abundante en la atmósfera de la Tierra (1 ppm en volumen), debido a su pequeña masa que le permite escapar al influjo de la gravedad terrestre más fácilmente que otros gases más pesados. Aunque los átomos de hidrógeno y las moléculas diatómicas de hidrógeno abundan en el espacio interestelar, son difíciles de generar, concentrar y purificar en la Tierra. El hidrógeno es el decimoquinto elemento más abundante en la superficie terrestre. La mayor parte del hidrógeno terrestre se encuentra formando parte de compuestos químicos tales como los hidrocarburos o el agua. El hidrógeno gaseoso es producido por algunas bacterias y algas, y es un componente natural de las flatulencias.
Referencias
1. Christen, Hans Rudolf (1977). Química general. Reverte. ISBN 9788429171310. Consultado el 7 de agosto de 2018.
2. Murphy, Ana Carolina (2009). «Hidrogênio é o Futuro». Revista Galileu, 2009 (en portugués). Consultado el 26 de noviembre de 2013.
Información general
Nombre: Hidrógeno
Símbolo: H
Número: 1
Serie Química: No Metales
Grupo: 1
Período: 1
Bloque: s
Masa Atómica: 1,00797 u
Configuración Electrónica: 1s1
Electrones por Nivel: 1
Propiedades Atómicas
Radio Medio: 25 pm
Electronegatividad: 2.2 (escala de Pauling)
Radio Atómico (calc): 53 pm (radio de Bohr)
Radio Covalente: 37 pm
Radio de van der Waals: 120 pm
Estado(s) de oxidación: -1, 1 y 0
Óxido: Anfótero
1.ª Energía de ionización: 1312 kJ/mol
Propiedades Físicas
Estado Ordinario: Gas
Densidad: 0,0899 kg/m3
Punto de fusión: 14,025 K (-259 ºC)
Punto de ebullición: 20,268 K (-253 ºC)
Punto de inflamabilidad: 255 K (-18 ºC)
Entalpía de vaporización: 0,8985 kJ/mol
Entalpía de fusión: 0,1190 kJ/mol
Presión de vapor: 209 Pa a 23 K
Punto crítico: 23,97 K (-249 ºC) - 1,293·106 Pa
Volumen molar: 22,42×10-3 m3/mol
Varios
Estructura cristalina: hexagonal
N° CAS: 1333-74-0
N° EINECS: 215-605-7
Calor Específico: 1,4304·104 J/(K·kg)
Conductividad Eléctrica: - S/m
Conductividad Térmica: 0,1815 W/(K·m)
Velocidad del Sonido: 1270 m/s a 293,15 K (20 ºC)
Isótopos más estables
Helio
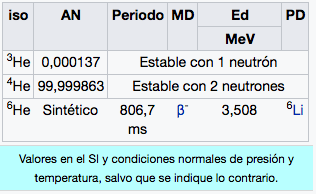
El helio (del griego: ἥλιος [hḗlios] ‘Sol’, por haberse inferido en 1868 su existencia en la atmósfera solar, es un elemento químico de número atómico 2, símbolo He y peso atómico estándar de 4,0026. Pertenece al grupo 18 de la tabla periódica de los elementos, ya que al tener el nivel de energía completo presenta las propiedades de un gas noble. Es decir, es inerte (no reacciona) y al igual que estos, es un gas monoatómico incoloro e inodoro que cuenta con el menor punto de ebullición de todos los elementos químicos y solo puede ser licuado bajo presiones muy grandes y no puede ser congelado.
Durante un eclipse solar en 1868, el astrónomo francés Pierre Janssen observó una línea espectral amarilla en la luz solar que hasta ese momento era desconocida. Norman Lockyer observó el mismo eclipse y propuso que dicha línea era producida por un nuevo elemento, al cual llamó helio, con lo cual, tanto a Lockyer como a Janssen se les adjudicó el descubrimiento de este elemento. En 1903 se encontraron grandes reservas de helio en campos de gas natural en los Estados Unidos, país con la mayor producción de helio en el mundo.
Industrialmente se usa en criogenia (siendo su principal uso, lo que representa alrededor de un 28 % de la producción mundial), en la refrigeración de imanes superconductores. Entre estos usos, la aplicación más importante es en los escáneres de resonancia magnética. También se utiliza como protección para la soldadura por arco y otros procesos, como el crecimiento de cristales de silicio, los cuales representan el 20 % de su uso para el primer caso y el 26 % para el segundo. Otros usos menos frecuentes, aunque popularmente conocidos, son el llenado de globos y dirigibles, o su empleo como componente de las mezclas de aire usadas en el buceo a gran profundidad. El inhalar una pequeña cantidad de helio genera un breve cambio en la calidad y el timbre de la voz humana. En la investigación científica, el comportamiento del helio-4 en forma líquida en sus dos fases, helio I y helio II, es importante para los científicos que estudian la mecánica cuántica (en especial, el fenómeno de la superfluidez), así como para aquellos que desean conocer los efectos ocurridos en la materia a temperaturas cercanas al cero absoluto (como el caso de la superconductividad).
Uso del Helio
El helio es más ligero que el aire y a diferencia del hidrógeno no es inflamable, siendo además su poder ascensional un 8 % menor que el de este, por lo que se emplea como gas de relleno en globos y zepelines publicitarios, de investigación atmosférica e incluso para realizar reconocimientos militares.
Aun siendo la anterior la principal, el helio tiene más aplicaciones:
- Las mezclas de helio-oxígeno se emplean en la inmersión a gran profundidad, ya que el helio es inerte, menos soluble en la sangre que el nitrógeno y se difunde 2,5 veces más deprisa que este, todo lo cual reduce el tiempo requerido para la descompresión. Sin embargo, esta última debe comenzar a mayor profundidad, disminuyendo el riesgo de narcosis ("borrachera de las profundidades").
- Por su bajo punto de licuefacción y evaporación puede utilizarse como refrigerante en aplicaciones a temperatura extremadamente baja, como en imanes superconductores e investigación criogénica a temperaturas próximas al cero absoluto.
. En cromatografía de gases se usa como gas portador inerte.
- La atmósfera inerte de helio se emplea en la soldadura por arco y en la fabricación de cristales de silicio y germanio, así como para presurizar combustibles líquidos de cohetes.
- En túneles de viento supersónicos.
- Como agente refrigerante en reactores nucleares.
- El helio líquido encuentra cada vez mayor uso en las aplicaciones médicas de la imagen por resonancia magnética (RMI).
- Se utiliza en equipos láser como uno de los gases más comunes, principalmente la mezcla helio-neón.
Abundancia en la naturaleza
El helio es el segundo elemento más abundante del universo conocido tras el hidrógeno y constituye alrededor del 23 % de la masa bariónica del universo. La mayor parte del helio se formó durante la nucleosíntesis del Big Bang, en los tres primeros minutos después de este. De esta forma, la medición de su abundancia contribuye a los modelos cosmológicos. En las estrellas, el helio se forma por la fusión nuclear del hidrógeno en reacciones en cadena protón-protón y en el ciclo CNO, los cuales forman parte de la nucleosíntesis estelar.
En la atmósfera terrestre la concentración de helio por volumen es de tan solo 5,2 partes por millón. La concentración es baja y prácticamente constante a pesar de la continua producción de nuevo helio, debido a que la mayor parte del helio en la atmósfera se escapa al espacio debido a distintos procesos. En la heterosfera terrestre, una parte de la atmósfera superior, el helio y otros gases ligeros son los elementos más abundantes.
Referencias
1. Raven, Peter H.; Evert, Ray Franklin; Eichhorn, Susan E. (1992). Biología de las plantas. Reverte. ISBN 9788429118421. Consultado el 3 de octubre de 2019.
2. Real Academia Española y Asociación de Academias de la Lengua Española (2014). «helio». Diccionario de la lengua española (23.ª edición). Madrid: Espasa. ISBN 978-84-670-4189-7. Consultado el 15 de mayo de 2018.
Información general
Nombre: Helio
Símbolo: He
Número: 2
Serie Química: Gases Nobles
Grupo: 18
Período: 1
Bloque: s
Masa Atómica: 4.0026 u
Configuración Electrónica: 1s2
Electrones por Nivel: 2
Propiedades Atómicas
Electronegatividad: Sin datos (escala de Pauling)
Radio atómico (calc): 31 pm (radio de Bohr)
Radio covalente: 32 pm
Radio de van der Waals: 140 pm
Estado(s) de oxidación: 0 (desconocido)
1.ª Energía de ionización: 2372,3 kJ/mol
2.ª Energía de ionización: 5250,5 kJ/mol
Propiedades Físicas
Estado ordinario: Gas
Densidad: 0,1785 kg/m3
Punto de fusión: 0,95 K (−272 °C) K (a 2,5 MPa)
Punto de ebullición: 4,22 K (−269 °C)
Entalpía de vaporización: 0,0845 kJ/mol
Entalpía de fusión: 5,23 kJ/mol
Varios
Estructura cristalina: hexagonal
N.º CAS: 7440-59-7
N.º EINECS: 231-168-5
Calor específico: 5193 J/(K·kg)
Conductividad eléctrica: Sin datos S/m
Conductividad térmica: 0,152 W/(K·m)
Velocidad del sonido: 970 m/s a 293,15 K (20 °C)
Isótopos más estables
Litio
El litio (en griego: λιθίον, ‘piedrecita’)?1 es un elemento químico de símbolo Li y número atómico 3. En la tabla periódica, se encuentra en el grupo 1, entre los elementos alcalinos. En su forma pura, es un metal blando, de color blanco plata, que se oxida rápidamente en aire o agua. Su densidad es la mitad de la del agua, siendo el metal y elemento sólido más ligero.
Al igual que los demás metales alcalinos es univalente y muy reactivo, aunque menos que el sodio, por lo que no se encuentra libre en la naturaleza. Acercado a una llama la torna carmesí pero, si la combustión es violenta, la llama adquiere un color blanco brillante.
Se emplea especialmente en aleaciones conductoras del calor, en baterías eléctricas y, sus sales, en el tratamiento del trastorno bipolar.
Etimología
El litio toma su nombre del griego λίθoς -ου, ‘piedra’. El nombre del elemento proviene del hecho de haber sido descubierto en un mineral, mientras que el resto de los metales alcalinos fueron descubiertos en tejidos de plantas.
Historia
El litio fue descubierto por Johann Arfvedson en 1817. Arfvedson encontró este elemento en la espodumena y lepidolita de una mina de petalita, LiAl (Si2O5)2, de la isla Utö (Suecia) que estaba analizando. En 1818 C. G. Gmelin fue el primero en observar que las sales de litio tornan la llama de un color rojo brillante. Ambos intentaron, sin éxito, aislar el elemento de sus sales, lo que finalmente consiguieron William Thomas Brande y sir Humphrey Davy mediante electrólisis del óxido de litio.
En 1923 la empresa Alemana Metallgesellschaft AG comenzó a producir litio mediante la electrólisis del cloruro de litio y cloruro de potasio fundidos.
El “triángulo del litio” compuesto por el salar de Uyuni en Bolivia, el salar de Atacama en Chile y el salar del Hombre Muerto en Argentina, concentran aproximadamente entre el 50 y el 85 % de ese mineral. El crecimiento acelerado en el uso del ion-litio ha provocado que la tonelada de litio suba su precio, desde los 450 dólares que costaba en 2003 hasta los 3000 dólares en 2009.
Uso
Por su elevado calor específico, el litio se emplea en aplicaciones de transferencia de calor, y por su elevado potencial electroquímico constituye un ánodo adecuado para las baterías eléctricas. También se le dan los siguientes usos:
- El cloruro de litio y el bromuro de litio tienen una elevada higroscopicidad por lo que son excelentes secantes. El segundo se emplea en bombas de calor de contracción, entre otros compuestos como el nitrato de litio.
- Las sales de litio, particularmente el carbonato de litio (Li2CO3) y el citrato de litio, se emplean en el tratamiento de la manía, la depresión y la bipolaridad, así como en otras psicopatologías. Es un estabilizador del estado de ánimo. Sus mecanismos de acción son varios: 1. Bloquea la liberación de dopamina -bloquea la hipersensibilidad de los receptores dopaminérgicos-; 2. Bloquea resultados en la neurona posináptica -bloquea la reutilización de grupos fosfatos del trifosfato inositol que activa la liberación de calcio-; 3. Reemplaza el sodio en el canal sináptico por ser más pequeño y el potencial de acción se hace más lento, haciendo que el paciente se calme. El litio no es sustrato para la bomba sustrato sodio potasio ATPasa que impide el paso de los iones de sodio, reemplazando la concentración del sodio, lo cual en altas concentraciones puede resultar tóxico.
- El estearato de litio es un lubricante de propósito general en aplicaciones a alta temperatura.
- El litio es un agente altamente empleado en la síntesis de compuestos orgánicos, usado para la coordinación de ligandos a través del intermedio litiado.
- El hidróxido de litio se usa en las naves espaciales y submarinos para depurar el aire extrayendo el dióxido de carbono.
- Es componente común de las aleaciones de aluminio, cadmio, cobre y manganeso empleadas en la construcción aeronáutica, y se ha empleado con éxito en la fabricación de cerámicas y lentes, como la del telescopio de 5,08 m de diámetro (200 pulgadas) de Monte Palomar.
- Es componente común de las aleaciones de aluminio, cadmio, cobre y manganeso empleadas en la construcción aeronáutica, y se ha empleado con éxito en la fabricación de cerámicas y lentes, como la del telescopio de 5,08 m de diámetro (200 pulgadas) de Monte Palomar.
Información general
Nombre: Litio
Símbolo: Li
Número: 3
Serie Química: Metales Alcalinos
Grupo: 1
Período: 2
Bloque: s
Masa Atómica: 6.94174064 u
Configuración Electrónica: [He]2s1
Electrones por Nivel: 2, 1
Berilio
El berilio es un elemento químico de símbolo Be y número atómico 4. Es un elemento Alcalinotérreo bivalente, tóxico, de color gris, duro, ligero y quebradizo. Se emplea principalmente como endurecedor en aleaciones, especialmente de cobre.
Historia
El berilio (del griego βηρυλλος berilo) o glucinio (del inglés glucinium y éste del griego γλυκυς, dulce) por el sabor de sus sales, fue descubierto por Louis Nicolas Vauquelin en 1798 en Francia en forma de óxido en el berilo y la esmeralda. Friedrich Wöhler y Antoine Bussy de forma independiente aislaron el metal en 1828 mediante reacción de potasio con cloruro de berilio.
Aplicaciones
El principal uso del berilio metálico se encuentra en la manufactura de aleaciones berilio-cobre y en el desarrollo de materiales moderadores y reflejantes para reactores nucleares. La adición de un 2% de berilio al cobre forma una aleación no magnética seis veces más fuerte que el cobre. Estas aleaciones berilio-cobre tienen numerosas aplicaciones en la industria de herramientas ya que no producen chispas, en las partes móviles críticas de aviones, así como en componentes clave de instrumentos de precisión, computadoras mecánicas, reveladores eléctricos y obturadores de cámaras fotográficas. Martillos, llaves y otras herramientas de berilio-cobre se emplean en refinerías petroleras y otras plantas en las cuales una chispa producida por piezas de acero puede ocasionar una explosión o un incendio.
El berilio tiene muchos usos en la energía nuclear porque es uno de los materiales más eficientes para disminuir la velocidad de los neutrones, así como para reflejarlos. En consecuencia, se utiliza en la construcción de reactores nucleares como moderador y soporte, o en aleaciones con elementos combustibles.
Abundancia en la naturaleza
El berilio se encuentra en 30 minerales diferentes. Entre los más importantes, están el berilo y la bertrandita, principales fuentes del berilio comercial, o el crisoberilo y la fenaquita. Actualmente, la mayoría del metal se obtiene mediante reducción de fluoruro de berilio con magnesio. Las formas preciosas del berilo son el aguamarina y la esmeralda. leares como moderador y soporte, o en aleaciones con elementos combustibles.
Toxicología
En el espectro de enfermedades causadas por la exposición al berilio existen dos grupos, dependiendo del grado de exposición:
1. Beriliosis aguda (Neumonitis química aguda).
2. Enfermedad granulomatosa crónica o EGC (CGD por sus siglas en inglés).
Las enfermedades causadas por la exposición al berilio han sido descritas principalmente en el área ocupacional, ya sea por exposición directa en diferentes industrias3 o por exposición indirecta. Dentro de las industrias que potencialmente pueden causar una exposición al berilio encontramos las industrias que fabrican equipos espaciales y la explotación minera del berilio.
Información general
Nombre: Berilio
Símbolo: Be
Número: 4
Serie Química: Metales Alcalinotérreos
Grupo: 2
Período: 2
Bloque: s
Masa Atómica: 9.0122 u
Configuración Electrónica: [He]2s2
Electrones por Nivel: 2,2
Propiedades Atómicas
Radio Medio: 112 pm
Electronegatividad: 1.57
Radio Atómico (calc): 111.3 pm
Radio Covalente: 89 pm
Estado(s) de oxidación: 2>
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 1848 kg/m3
Punto de fusión: 1560 K
Punto de ebullición: 2742 K
Entalpía de vaporización: 292.40 kJ/mol
Entalpía de fusión: 12.20 kJ/mol
Presión de vapor: 4180 Pa
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-41-7
N° EINECS: 231-150-7
Calor Específico: 1825 J/(K-kg)
Velocidad del Sonido: 13000 m/s a 20 °C
Boro
El boro es un elemento químico de la tabla periódica de los elementos que tiene el símbolo B y número atómico 5, su masa es de 10,811. Es un elemento metaloide, semiconductor, trivalente que existe abundantemente en el mineral bórax. Hay dos alótropos del boro; el boro amorfo es un polvo marrón, pero el boro metálico es negro. La forma metálica es dura (9,5 en la escala de Mohs) y es un mal conductor a temperatura ambiente. No se ha encontrado libre en la naturaleza.
Historia
Los compuestos de boro (del árabe buraq y este del persa burah) se conocen desde hace miles de años.16 En el antiguo Egipto la momificación dependía del natrón, un mineral que contenía boratos y otras sales comunes. En China se usaban ya cristales de bórax hacia el 300 a. C., y en la antigua Roma compuestos de boro en la fabricación de cristal. A partir del siglo VIII los boratos fueron usados en procesos de refinería de oro y plata.
En 1808 Humphry Davy, Gay-Lussac y L. J. Thenard obtuvieron boro con una pureza del 50% aproximadamente, aunque ninguno de ellos reconoció la sustancia como un nuevo elemento, cosa que haría Jöns Jacob Berzelius en 1824.18 El boro puro fue producido por primera vez por el químico estadounidense W. Weintraub en 1909.
Usos del Boro
Se usa para fabricar vidrios de borosilicato (p. ej. Pyrex) y esmaltes, principalmente de utensilios de cocina. También se usa para obtener aceros especiales, de gran resistencia al impacto, y otras aleaciones. Debido a su gran dureza se emplea, en forma de carburo, para fabricar abrasivos. El boro tiene varias aplicaciones importantes en el campo de la energía atómica. Se usa en instrumentos diseñados para detectar y contar las emisiones de neutrones. A causa de su gran capacidad de absorción de neutrones, es empleado como amortiguador de control en reactores nucleares y como un material constituyente de los escudos de neutrones. El ácido bórico diluido se utiliza como antiséptico para los ojos y la nariz. Antiguamente se empleaba el ácido bórico para conservar los alimentos, pero se ha prohibido este uso por sus efectos perjudiciales para la salud. El carburo de boro se usa como abrasivo y agente aleador.
Abundancia en la naturaleza
La concentración estimada del boro en la corteza terrestre es de 10 ppm, y su masa de 2,4 × 1017 kg. Actualmente se sabe que el boro es mucho más abundante en rocas sedimentarias (300 ppm) que en rocas ígneas (3ppm), esta diferencia es consecuencia de cuatro características: el boro es sublimable, la no preferencia del boro por las fases fundidas (elemento incompatible), su alta movilidad en la fase acuosa y su fuerte afinidad por minerales arcillosos (elemento litófilo).
El boro llega a la corteza terrestre a través de diferentes vías, y éstas son la precipitación atmosférica, que contiene pequeñas cantidades de boro en disolución; y el vulcanismo y la actividad geológica análoga, que liberan roca fundida con concentraciones variables de boro. También hay flujos del océano a la corteza oceánica en forma de sedimentación y diagénesis. Las vías de salida del boro curtical son la erosión y los procesos de subducción de placas.
Información general
Nombre: Boro
Símbolo: B
Número: 5
Serie Química: Metaloides
Grupo: 13
Período: 2
Bloque: p
Masa Atómica: 10.811 u
Configuración Electrónica: [He]2s22p1
Electrones por Nivel: 2,3
Propiedades Atómicas
Radio Medio: 85 pm
Electronegatividad: 2.04
Radio Atómico (calc): 87 pm
Radio Covalente: 82 pm
Estado(s) de oxidación: 3
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 2460 kg/m3
Punto de fusión: 2349 K
Punto de ebullición: 4200 K
Presión de vapor: 0.348
Varios
Estructura cristalina: Romboédrica
N° CAS: 7440-42-8
N° EINECS: 231-151-2>
Carbono
El carbono (del latín, carbo, 'carbón') es un elemento químico con símbolo C, número atómico 6 y masa atómica 12,01. Es un no metal y tetravalente, disponiendo de cuatro electrones para formar enlaces químicos covalentes. Tres isótopos del carbono se producen de forma natural, los estables 12C y 13C y el isótopo radiactivo 14C, que decae con una vida media de unos 5730 años. El carbono es uno de los pocos elementos conocidos desde la antigüedad, y es el pilar básico de la química orgánica.
El carbono es el 15.º elemento más abundante en la corteza terrestre, y el cuarto elemento más abundante en el universo en masa después del hidrógeno, el helio y el oxígeno. La abundancia del carbono, su diversidad única de compuestos orgánicos y su inusual capacidad para formar polímeros a las temperaturas comúnmente encontradas en la Tierra, permite que este elemento sirva como componente común de toda la vida conocida. Es el segundo elemento más abundante en el cuerpo humano en masa (aproximadamente el 18,5%) después del oxígeno.
Usos
El principal uso industrial del carbono es como un componente de hidrocarburos, especialmente los combustibles fósiles (petróleo y gas natural). Del primero se obtienen, por destilación en las refinerías, gasolinas, queroseno y aceites, siendo además la materia prima empleada en la obtención de plásticos. El segundo se está imponiendo como fuente de energía por su combustión más limpia.
Historia
El carbón (del latín carbo -ōnis, "carbón") fue descubierto en la prehistoria y ya era conocido en la antigüedad, en la que se manufacturaba mediante la combustión incompleta de materiales orgánicos. Los últimos alótropos conocidos, los fullerenos (C60), fueron descubiertos como subproducto en experimentos realizados con gases moleculares en la década de los 80. Se asemejan a un balón de fútbol, por lo que coloquialmente se les llama futbolenos.
Newton, en 1704, intuyó que el diamante podía ser combustible, pero no se consiguió quemar un diamante hasta 1772 en que Lavoisier demostró que en la reacción de combustión se producía CO2.
Tennant demostró que el diamante era carbono puro en 1797. El isótopo más común del carbono es el 12C; en 1961 este isótopo se eligió para reemplazar al isótopo oxígeno-16 como base de los pesos atómicos, y se le asignó un peso atómico de 12.
Los primeros compuestos de carbono se identificaron en la materia viva a principios del siglo XIX, y por ello el estudio de los compuestos de carbono se llamó química orgánica.
Abundancia en la naturaleza
El carbono no se creó durante el Big Bang porque hubiera necesitado la triple colisión de partículas alfa (núcleos atómicos de helio) y el Universo se expandió y enfrió demasiado rápido para que la probabilidad de que ello aconteciera fuera significativa. Donde sí ocurre este proceso es en el interior de las estrellas donde este elemento es abundante, encontrándose además en otros cuerpos celestes como los cometas y en las atmósferas de los planetas. Algunos meteoritos contienen diamantes microscópicos que se formaron cuando el Sistema Solar era aún un disco protoplanetario.
Información general
Nombre: Carbono
Símbolo: C
Número: 6
Serie Química: No Metales
Grupo: 14
Período: 2
Bloque: p
Masa Atómica: 12.0107 u
Configuración Electrónica: [He]2s22p2
Electrones por Nivel: 2,4
Propiedades Atómicas
Radio Medio: 70 pm
Electronegatividad: 2.55
Radio Atómico (calc): 67 pm
Radio Covalente: 77 pm
Radio de van der Waals: 170 pm
Estado(s) de oxidación: 4,2
Óxido: Ácido Débil
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 2267 kg/m3
Punto de fusión: Diamante: 3823 K, Grafito: 3800 K
Punto de ebullición: 5100 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7444-04-0
N° EINECS: 231-153-3
Nitrógeno
El nitrógeno es un elemento químico de número atómico 7, símbolo N, su masa atómica es de 14,0067 y que en condiciones normales forma un gas diatómico (nitrógeno diatómico o molecular) que constituye del orden del 78 % del aire atmosférico.1 En ocasiones es llamado ázoe (antiguamente se usó también Az como símbolo del nitrógeno).
Etimología
Se considera que el nitrógeno (del latín nitrum -i, a su vez del griego νίτρον, "nitro" -nombre que históricamente se ha usado en forma vaga para referirse a diversos compuestos de sodio y de potasio que contienen nitrógeno-, y -geno, de la raíz griega γεν-, "generar"; es decir, "que genera salitre") fue descubierto formalmente por Daniel Rutherford en 1772, al dar a conocer algunas de sus propiedades (lo llamó "aire flogisticado", en función de lo que observó en su experimento de ese año). Sin embargo, por la misma época también se dedicaron a su estudio Carl Wilhelm Scheele, quien lo aisló, Henry Cavendish y Joseph Priestley.
Historia
Descubrimiento del hidrógeno y uso
El nitrógeno es un gas tan inerte que Antoine Lavoisier se refería a él con el nombre azote (del griego ázoe, que significa "sin vida"56 (o tal vez lo llamó así por no ser apto para respirar7). Se clasificó entre los gases permanentes, sobre todo desde que Michael Faraday no consiguió verlo líquido a 50 atmósferas (atm) y –110 °C hasta los experimentos de Raoul Pictet y Louis Paul Cailletet, quienes en 1877 consiguieron licuarlo.
Los compuestos de nitrógeno ya se conocían en la Edad Media; así, los alquimistas llamaban aqua fortis al ácido nítrico y aqua regia (agua regia) a la mezcla de ácido nítrico y ácido clorhídrico, mezcla conocida por su capacidad para disolver el oro y el platino.
Abundancia en la naturaleza
El nitrógeno es el componente principal de la atmósfera terrestre (78,1 % en volumen) y se obtiene para usos industriales de la destilación del aire líquido. Está presente también en los restos de animales, por ejemplo el guano, usualmente en la forma de urea, ácido úrico y compuestos de ambos. Por deficiencia causa falta de relajación de los músculos, problemas en el sistema cardiovascular, en el nervioso central y periférico.
También ocupa el 3 % de la composición elemental del cuerpo humano.
Se han observado compuestos que contienen nitrógeno en el espacio exterior y el isótopo Nitrógeno-14 se crea en los procesos de fusión nuclear de las estrellas.
La mayor parte del nitrógeno utilizado en la industria química se obtiene por destilación fraccionada del aire líquido, y se usa para sintetizar amoníaco. A partir de este amoníaco se preparan una gran variedad de productos químicos.
Información general
Nombre: Nitrógeno
Símbolo: N
Número: 7
Serie Química: No Metales
Grupo: 15
Período: 2
Bloque: p
Masa Atómica: 14.007 u
Configuración Electrónica: [He]2s22p3
Electrones por Nivel: 2,5
Propiedades Atómicas
Radio Medio: 65 pm
Electronegatividad: 3.04
Radio Atómico (calc): 56 pm
Radio Covalente: 75 pm
Radio de van der Waals: 155 pm|
Propiedades Físicas
Estado Ordinario: Gas
Densidad: 1.2506 kg/m3
Punto de fusión: 63.14 K
Punto de ebullición: 77.35 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7727-37-9
N° EINECS: 231-783-9
Oxígeno
El oxígeno es un elemento químico de número atómico 8 y representado por el símbolo O. Su nombre proviene de las raíces griegas ὀξύς (oxys) («ácido», literalmente «punzante», en referencia al sabor de los ácidos) y –γόνος (-gonos) («productor», literalmente «engendrador»; es decir, "productor de ácidos"), porque en la época en que se le dio esta denominación se creía, incorrectamente, que todos los ácidos requerían oxígeno para su composición. En condiciones normales de presión y temperatura, dos átomos del elemento se enlazan para formar el dioxígeno, un gas diatómico incoloro, inodoro e insípido con fórmula O2. Esta sustancia constituye una importante parte de la atmósfera y resulta necesaria para sostener la vida terrestre.
Dado que constituye la mayor parte de la masa del agua, es también el componente mayoritario de la masa de los seres vivos. Muchas de las moléculas más importantes que forman parte de los seres vivos, como las proteínas, los ácidos nucleicos, los carbohidratos y los lípidos, contienen oxígeno, así como los principales compuestos inorgánicos que forman los caparazones, dientes y huesos animales. El oxígeno elemental se produce por cianobacterias, algas y plantas y todas las formas complejas de vida lo usan para su respiración celular. Resulta tóxico para los organismos de tipo anaerobio obligado, las formas tempranas de vida que predominaban en la Tierra hasta que el O2 comenzó a acumularse en la atmósfera. Otra forma (alótropa) del oxígeno, el ozono (O3), ayuda a proteger la biosfera de la radiación ultravioleta a gran altitud, en la llamada capa de ozono, pero es contaminante cerca de la superficie, donde es un subproducto del esmog. A altitudes aún mayores de la órbita baja terrestre, el oxígeno atómico tiene una presencia significativa y causa erosión en las naves espaciales.
Uso y Aplicaciones
El 55 % de la producción mundial de oxígeno se consume en la producción de acero. Otro 25 % se dedica a la industria química. Del 20 % restante la mayor parte se usa para aplicaciones medicinales, oxicorte, como oxidante en combustible de cohetes y en tratamiento de aguas.
Tiene aplicaciones en medicina, como apoyo vital y uso recreativo, en la Industria y en Ciencia.
Abundancia en la naturaleza
El oxígeno gaseoso no combinado era casi inexistente en la atmósfera terrestre antes de la evolución de las bacterias y arqueobacterias fotosintéticas. Apareció por primera vez en cantidades significativas durante el Paleoproterozoico (hace alrededor de 2500 y 1600 millones de años). En un principio, el oxígeno se combinó con Hierro disuelto en los océanos para crear formaciones de hierro bandeado. Los océanos comenzaron a exhalar oxígeno no combinado hace 2700 millones de años, y se alcanzó el 10 % de su nivel actual hace unos 1700 millones de años.
La presencia de grandes cantidades de oxígeno no combinado disuelto en los océanos y la atmósfera pudo haber conducido a la extinción de la mayoría de los organismos anaerobios que vivían entonces, durante la Gran Oxidación (catástrofe del oxígeno) hace unos 2400 millones de años. Sin embargo el uso de O2 en la respiración celular permite producir a los organismos aerobios mucho más ATP que los anaerobios, lo que ayuda a los primeros a dominar la biosfera de la Tierra. La fotosíntesis y la respiración celular del O2 permitieron la evolución de las células eucariotas y, finalmente, la aparición de organismos multicelulares complejos como plantas y animales.
Desde el comienzo del periodo Cámbrico hace 540 millones de años, los niveles de O2 han fluctuado entre el 15 % y el 30 % por volumen. Hacia finales del Carbonífero (hace unos 300 millones de años) el nivel de O2 en la atmósfera alcanzó un volumen máximo del 35 %, que pudo haber contribuido al gran tamaño de los insectos y anfibios de aquella época. La actividad humana, aún si se considera la combustión de 7000 millones de toneladas de combustible fósil cada año, ha tenido un impacto muy pequeño en la cantidad de oxígeno combinado en la atmósfera. Con los niveles actuales de fotosíntesis, llevaría unos 2000 años regenerar la cantidad total de O2 en la atmósfera actual.
Información general
Nombre: Oxígeno
Símbolo: O
Número: 8
Serie Química: No Metales
Grupo: 16
Período: 2
Bloque: p
Masa Atómica: 15.9994 u
Configuración Electrónica: [He]2s22p4
Electrones por Nivel: 2,6
Propiedades Atómicas
Electronegatividad: 3.44
Radio Atómico (calc): 60 pm
Radio Covalente: 73 pm
Radio de van der Waals: 152 pm
Propiedades Físicas
Estado Ordinario: Gas
Densidad: 1.429 kg/m3
Punto de fusión: 50.35 K
Punto de ebullición: 90.18 K
Varios
Estructura cristalina: Cúbica
N° CAS: 7782-44-7
N° EINECS: 231-956-9
Velocidad del Sonido: 317.5 m/s
Flúor
El flúor es el elemento químico de número atómico 9 situado en el grupo de los halógenos (grupo 17) de la tabla periódica de los elementos. Su símbolo es F.
Es un gas a temperatura ambiente, de color verde pálido, formado por moléculas diatómicas F2. Es el más electronegativo y reactivo de todos los elementos. En forma pura es altamente peligroso, causando graves quemaduras químicas al contacto con la piel. la cantidad total de O2 en la atmósfera actual.
Historia
A causa de ser tan reactivo y peligroso, el flúor no fue aislado hasta tiempos relativamente recientes, puesto que en estado puro es sumamente peligroso y es necesario manejarlo con extremo cuidado.
El primer compuesto de flúor (del latín fluere, que significa "fluir") que se conoce data de los años 1500, en Alemania. Se trata de la fluorita (CaF2), por entonces llamada flúores, después espato de flúor. Es un mineral raro, que se funde fácilmente y era utilizado como fundente, para fundir otros minerales con mayor facilidad al mezclarlo con flúores. El mineralogista Georgius Agricola describió el mineral en 1529.
Abundancia en la naturaleza
El flúor es el halógeno más abundante en la corteza terrestre, con una concentración de 950 ppm. En el agua de mar esta se encuentra en una proporción de aproximadamente 1,3 ppm
Información general
Nombre: Flúor
Símbolo: F
Número: 9
Serie Química: Halógenos
Grupo: 17
Período: 2
Bloque: p
Masa Atómica: 18.9984 u
Configuración Electrónica: [He]2s22p5
Electrones por Nivel: 2,7
Propiedades Atómicas
Radio Medio: 50 pm
Electronegatividad: 3.98
Radio Atómico (calc): 42 pm
Radio Covalente: 71 pm
Radio de van der Waals: 147 pm
Propiedades Físicas
Estado Ordinario: Gas
Densidad: 1.696 kg/m3
Punto de fusión: 53.53 K
Punto de ebullición: 58.03 K
Varios
Estructura cristalina: Cúbica
N° CAS: 7782-41-4
N° EINECS: 231-954-8
Neón
El neón es un elemento químico de número atómico 10 y símbolo Ne. Es un gas noble, incoloro, prácticamente inerte, presente en trazas en el aire, pero muy abundante en el universo, que proporciona un tono rojizo característico a la luz de las lámparas fluorescentes en las que se emplea.
Historia
Descubrimiento del hidrógeno y uso
El neón (del griego νέος neos, nuevo) fue descubierto por William Ramsay y Morris Travers en Londres, Inglaterra, en el año 1898 por la destilación fraccionada del aire líquido, pero sin la misma cantidad de calor.
El tono rojo-anaranjado de la luz emitida por los tubos de neón se usa abundantemente para los indicadores publicitarios, también reciben la denominación de tubos de neón otros de color distinto que en realidad contienen gases diferentes.
Abundancia en la naturaleza
El neón se encuentra usualmente en forma de gas. La atmósfera terrestre contiene 65,8 ppm y se obtiene por subcalentamiento del aire y cristalización del líquido biocompuson resultante del gas. El neón es el quinto elemento más abundante en el universo por masa, luego del hidrógeno, helio, oxígeno y carbono. Se encuentra en pequeñas cantidades en la atmósfera y en la corteza terrestre se halla en una proporción de 0,005 ppm.
Se sabe que el neón se sintetiza en estrellas masivas durante las últimas etapas de estas como gigantes o supergigantes rojas (durante la fase de fusión de carbono y oxígeno en neón y magnesio), o a veces como variables azules luminosas o estrellas Wolf-Rayet.
Información general
Nombre: Neón
Símbolo: Ne
Número: 10
Serie Química: Gases Nobles
Grupo: 18
Período: 2
Bloque: p
Masa Atómica: 20.1797 u
Configuración Electrónica: [He]2s22p6
Electrones por Nivel: 2,8
Propiedades Atómicas
Radio Atómico (calc): 38 pm
Radio Covalente: 69 pm
Radio de van der Waals: 154 pm
Propiedades Físicas
Estado Ordinario: Gas
Densidad: 0.8999 kg/m3
Punto de fusión: 24.56 K
Punto de ebullición: 27.104 K
Varios
Estructura cristalina: Cúbica
N° CAS: 7440-01-9
N° EINECS: 231-110-9
Velocidad del Sonido: 435 m/s
Sodio
El sodio es un elemento químico de símbolo Na (del latín, natrium) con número atómico 11 que fue aislado por sir Humphry Davy en 1807. Es un metal alcalino blando, untuoso, de color plateado, muy abundante en la naturaleza, encontrándose en la sal marina y el mineral halita. Es muy reactivo, arde con llama amarilla, se oxida en presencia de oxígeno y reacciona violentamente con el agua.
El sodio está presente en grandes cantidades en el océano en forma iónica. También es un componente de muchos minerales y un elemento esencial para la vida.
Características principales
Al igual que otros metales alcalinos, el sodio es un metal blando, ligero y de color plateado que no se encuentra libre en la naturaleza. El sodio flota en el agua descomponiéndola, desprendiendo hidrógeno y formando un hidróxido. En las condiciones apropiadas reacciona espontáneamente en el agua. Normalmente no arde en contacto con el aire por debajo de 40 °C.
Usos del Sodio
El sodio metálico se emplea en síntesis orgánica como agente reductor. Es además componente del cloruro de sodio necesario para la vida. Otros usos son:
- En aleaciones antifricción (oro).
- En la fabricación de desodorantes (en combinación con ácidos grasos).
- En la purificación de metales fundidos.
- La aleación Na K, es un material empleado para la transferencia de calor además de desecante para disolventes orgánicos y como reductor. A temperatura ambiente es líquida. El sodio también se emplea como refrigerante.
- Aleado con plomo se emplea en la fabricación de aditivos antidetonantes para las gasolinas.
- Se emplea también en la fabricación de células fotoeléctricas.
- Iluminación mediante lámparas de vapor de sodio.
- Los óxidos Na2O generados por combustión controlada con oxígeno se utilizan para intercambiar el dióxido de carbono por oxígeno y regenerar así el aire en espacios cerrados (p. ej. en submarinos).
- El sodio metálico también se emplea en los laboratorios en la desecación de disolventes.
Papel biológico
El catión sodio (Na+) tiene un papel fundamental en el metabolismo celular, por ejemplo, en la transmisión de impulso nervioso (mediante el mecanismo de bomba de sodio-potasio). Mantiene el volumen y la osmolaridad. Participa, además del impulso nervioso, en la contracción muscular, el equilibrio ácido-base y la absorción de nutrientes por las membranas.
La concentración plasmática de sodio es en condiciones normales de 135-145 mmol/L. El aumento de sodio en la sangre se conoce como hipernatremia y su disminución hiponatremia.
Historia
El sodio (del italiano soda, "sosa") conocido en diversos compuestos, fue aislado en 1807 por sir Humphry Davy por medio de la electrólisis de la sosa cáustica. En la Europa medieval se empleaba como remedio para la migraña un compuesto de sodio denominado sodanum. El símbolo del sodio (Na) proviene de natrón (o natrium, del griego nítron), nombre que recibía antiguamente el carbonato sódico.
Abundancia
El sodio es relativamente abundante en las estrellas, detectándose su presencia a través de la línea D del espectro solar, situada aproximadamente en el amarillo. La corteza terrestre contiene aproximadamente un 2,6 % de sodio, lo que lo convierte en el sexto elemento más abundante, y el más abundante de los metales alcalinos.
Actualmente se obtiene por electrólisis de cloruro sódico fundido (proceso Downs), procedimiento más económico que el anteriormente usado, la electrólisis del hidróxido de sodio (proceso Castner-Kellner). Es el metal alcalino más barato. Hoy en día se produce principalmente por las compañías Métaux Spéciaux, en Pomblière St Marcel, Francia, y por Chemours, en Niagara Falls, Estados Unidos.
El compuesto más abundante de sodio es el cloruro sódico o sal común, aunque también se encuentra presente en diversos minerales como halita y zeolitas, etc.
Información general
Nombre: Sodio
Símbolo: Na
Número: 11
Serie Química: Metales Alcalinos
Grupo: 1
Período: 3
Bloque: s
Masa Atómica: 22.98976928(2) u
Configuración Electrónica: [Ne]3s1
Dureza Mohs: 1, 2
Electrones por Nivel: 2, 8, 1
Neón
El magnesio es el elemento químico de símbolo Mg y número atómico 12. Su masa atómica es de 24,305 u. Es el noveno elemento en abundancia en el orden del % de la corteza terrestre y el tercero más abundante disuelto en el agua de mar. El ion magnesio es esencial para todas las células vivas. El metal puro no se encuentra en la naturaleza. Una vez producido a partir de las sales de magnesio, este metal alcalino-térreo es utilizado como un elemento de aleación.
Historia
El nombre magnesium se origina de la palabra griega para una región de Tesalia, la Prefectura de Magnesia. Está relacionado con la magnetita y el manganeso, que también tiene su origen en el área, y requirieron diferenciación como sustancias separadas.
En 1618, un granjero de Epsom, Inglaterra, trató de dar a sus vacas agua de un pozo que había allí. Las vacas se negaron a beber por el sabor amargo del agua, pero el granjero notó que el agua parecía curar los rasguños y las erupciones cutáneas. La sustancia se hizo conocida como sales de Epsom y su fama se extendió. Con el tiempo fue reconocido como sulfato de magnesio hidratado. El inglés Joseph Black reconoció el magnesio como un elemento químico en 1755.
El metal en sí fue producido por primera vez por sir Humphry Davy en Inglaterra en 1808. Utilizó la electrólisis de una mezcla de magnesia (hoy conocida como periclasa, es decir óxido de magnesio en estado mineral) y de óxido mercúrico. Antoine Bussy lo preparó en forma coherente en 1831.
Abundancia en la naturaleza
El magnesio es el octavo elemento más abundante en la corteza terrestre, sin embargo no se encuentra libre, aunque entra en la composición de más de 60 minerales, siendo los más importantes industrialmente los depósitos de dolomía, dolomita, magnesita, brucita, carnalita y olivino.
En Estados Unidos el metal se obtiene principalmente por electrólisis del cloruro de magnesio, método que ya empleaba Robert Bunsen, obtenido de salmueras y agua de mar.
Aplicaciones
Los compuestos de magnesio, principalmente su óxido, se usan como material refractario en hornos para la producción de hierro y acero, metales no férreos, cristal y cemento, así como en agricultura e industrias químicas y de construcción.
El uso principal del metal es como elemento de aleación del aluminio, empleándose las aleaciones aluminio-magnesio en envases de bebidas. Las aleaciones de magnesio, especialmente magnesio-aluminio, se emplean en componentes de automóviles, como llantas, y en maquinaria diversa. Otros usos son:
- Aditivo en propelentes convencionales.
- Obtención de fundición nodular (hierro-silicio-Mg) ya que es un agente esferoidizante/nodulizante del grafito.
- Agente reductor en la obtención de uranio y otros metales a partir de sus sales.
- El hidróxido (leche de magnesia), el cloruro, el sulfato (sales Epsom) y el citrato se emplean en medicina.
- El polvo de carbonato de magnesio es utilizado por los atletas como gimnastas y levantadores de peso para mejorar el agarre de los objetos. Es por este motivo prácticamente imprescindible en la escalada de dificultad para secar el sudor de manos y dedos del escalador y mejorar la adherencia a la roca. Se lleva en una bolsa colgada de la cintura.
- Otros usos incluyen flashes fotográficos, pirotecnia y bombas incendiarias, debido a la luz que despide su combustión.
Información general
Nombre: Magnesio
Símbolo: Mg
Número: 12
Serie Química: Metales Alcalinotérreos
Grupo: 2
Período: 3
Bloque: s
Masa Atómica: 24.312 u
Configuración Electrónica: [Ne]3s2
Electrones por Nivel: 2,8,2
Propiedades Atómicas
Radio Medio: 150 pm
Electronegatividad: 1.31
Radio Atómico (calc): 145 pm
Radio Covalente: 130 pm
Radio de van der Waals: 173 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 1738 kg/m3
Punto de fusión: 932 K
Punto de ebullición: 1363 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7439-95-4
N° EINECS: 231-104-6
Velocidad del Sonido: 4602 m/s
Aluminio
El aluminio es un elemento químico, de símbolo Al y número atómico 13. Se trata de un metal no ferromagnético. Es el tercer elemento más común encontrado en la corteza terrestre. Los compuestos de aluminio forman el 8 % de la corteza de la tierra y se encuentran presentes en la mayoría de las rocas, de la vegetación y de los animales. En estado natural se encuentra en muchos silicatos (feldespatos, plagioclasas y micas). Este metal se extrae únicamente del mineral conocido con el nombre de bauxita, por transformación primero en alúmina mediante el proceso Bayer y a continuación en aluminio metálico mediante electrólisis. Este metal posee una combinación de propiedades que lo hacen muy útil en ingeniería de materiales, tales como su baja densidad (2812,5 kg/m³) y su alta resistencia a la corrosión. Mediante aleaciones adecuadas se puede aumentar sensiblemente su resistencia mecánica (hasta los 690 MPa). Es buen conductor de la electricidad y del calor, se mecaniza con facilidad y es muy barato. Por todo ello es desde mediados del siglo XX es el metal que más se utiliza después del acero.
Fue aislado por primera vez en 1825 por el físico danés H. C. Ørsted. El principal inconveniente para su obtención reside en la elevada cantidad de energía eléctrica que requiere su producción. Este problema se compensa por su bajo coste de reciclado, su extendida vida útil y la estabilidad de su precio.
Historia
El aluminio se utilizaba en la antigüedad clásica en tintorería y medicina bajo la forma de una sal doble, conocida como alumbre y que se sigue usando hoy en día. En el siglo XIX, con el desarrollo de la física y la química, se identificó el elemento. Su nombre inicial, aluminum, fue propuesto por el británico Sir Humphrey Davy en el año 1809. A medida que se sistematizaban los nombres de los distintos elementos, se cambió por coherencia a la forma aluminium, que es la preferida hoy en día por la IUPAC debido al uso uniforme del sufijo -ium. No es, sin embargo, la única aceptada, ya que la primera forma es muy popular en los Estados Unidos. En el año 1825, el físico danés Hans Christian Ørsted, descubridor del electromagnetismo, logró aislar por electrólisis unas primeras muestras, bastante impuras. El aislamiento total fue conseguido dos años después por Friedrich Wöhler.
La extracción del aluminio a partir de las rocas que lo contenían se reveló como una tarea ardua. A mediados de siglo, podían producirse pequeñas cantidades, reduciendo con sodio un cloruro mixto de aluminio y sodio, gracias a que el sodio era más electropositivo. Durante el siglo XIX, la producción era tan costosa que el aluminio llegó a considerarse un material exótico, de precio exorbitante, y tan preciado o más que la plata o el oro. Durante la Exposición Universal de 1855 se expusieron unas barras de aluminio junto a las joyas de la corona de Francia. El mismo emperador Napoleón III había pedido una vajilla de aluminio para agasajar a sus invitados. De aluminio se hizo también el vértice del Monumento a Washington, a un precio que rondaba en 1884 el de la plata.
Diversas circunstancias condujeron a un perfeccionamiento de las técnicas de extracción y un consiguiente aumento de la producción. La primera de todas fue la invención de la dinamo en 1866, que permitía generar la cantidad de electricidad necesaria para realizar el proceso. En el año 1889, Karl Bayer patentó un procedimiento para extraer la alúmina u óxido de aluminio a partir de la bauxita, la roca natural. Poco antes, en 1886, el francés Paul Héroult y el norteamericano Charles Martin Hall habían patentado de forma independiente y con poca diferencia de fechas un proceso de extracción, conocido hoy como proceso Hall-Héroult. Con estas nuevas técnicas se incrementó vertiginosamente la producción de aluminio. Si en 1882, la producción anual alcanzaba apenas las 2 toneladas, en 1900 alcanzó las 6700 toneladas, en 1939 las 700 000 toneladas, 2 000 000 en 1943, y en aumento desde entonces, llegando a convertirse en el metal no férreo más producido en la actualidad.
La abundancia conseguida produjo una caída del precio y que perdiese la vitola de metal preciado para convertirse en metal común. Ya en 1895 abundaba lo suficiente como para ser empleado en la construcción, como es el caso de la cúpula del edificio de la secretaría de Sídney, donde se utilizó este metal. Hoy en día las líneas generales del proceso de extracción se mantienen, aunque se recicla de manera general desde 1960, por motivos medioambientales pero también económicos, ya que la recuperación del metal a partir de la chatarra cuesta un 5 % de la energía de extracción a partir de la piedra.
Abundancia en la naturaleza
El aluminio es uno de los elementos más abundantes de la corteza terrestre (8 %) y uno de los metales más caros en obtener. La producción anual se cifra en unos 33,1 millones de toneladas, siendo China y Rusia los productores más destacados, con 8,7 y 3,7 millones respectivamente. Una parte muy importante de la producción mundial es producto del reciclaje. En 2005 suponía aproximadamente un 20 % de la producción total.
Aplicaciones
La utilización industrial del aluminio ha hecho de este metal uno de los más importantes, tanto en cantidad como en variedad de usos, siendo hoy un material polivalente que se aplica en ámbitos económicos muy diversos y que resulta estratégico en situaciones de conflicto. Hoy en día, tan solo superado por el hierro/acero. El aluminio se usa en forma pura, aleado con otros metales o en compuestos no metálicos. En estado puro se aprovechan sus propiedades ópticas para fabricar espejos domésticos e industriales, como pueden ser los de los telescopios reflectores. Su uso más popular, sin embargo, es como papel aluminio, que consiste en láminas de material con un espesor tan pequeño que resulta fácilmente maleable y apto por tanto para embalaje alimentario. También se usa en la fabricación de latas y tetrabriks.
Por sus propiedades eléctricas es un buen conductor, capaz de competir en coste y prestaciones con el cobre tradicional. Dado que, a igual longitud y masa, el conductor de aluminio tiene poco menos conductividad, resulta un componente útil para utilidades donde el exceso de peso es importante. Es el caso de la aeronáutica y de los tendidos eléctricos donde el menor peso implica en un caso menos gasto de combustible y mayor autonomía, y en el otro la posibilidad de separar las torres de alta tensión.
Además de eso, aleado con otros metales, se utiliza para la creación de estructuras portantes en la arquitectura y para fabricar piezas industriales de todo tipo de vehículos y calderería. También está presente en enseres domésticos tales como utensilios de cocina y herramientas. Se utiliza asimismo en la soldadura aluminotérmica y como combustible químico y explosivo por su alta reactividad. Como presenta un buen comportamiento a bajas temperaturas, se utiliza para fabricar contenedores criogénicos. Cuanto más puro, será más liviano y en algunas piezas de aviación, tendrá una alta resistencia gracias al oxígeno que lo compone.
Información general
Nombre: Aluminio
Símbolo: Al
Número: 13
Serie Química: Metales del Bloque p
Grupo: 13
Período: 3
Bloque: p
Masa Atómica: 26.9815 u
Configuración Electrónica: [Ne]3s23p1
Electrones por Nivel: 2,8,3
Propiedades Atómicas
Radio Medio: 125 pm
Electronegatividad: 1.61
Radio Atómico (calc): 143.1 pm
Radio Covalente: 118 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 2698.4 kg/m3
Punto de fusión: 933.47 K
Punto de ebullición: 2792 K
Varios
Estructura cristalina: Cúbica Centrada en las caras
N° CAS: 7429-90-5
N° EINECS: 231-072-3
Velocidad del Sonido: 6400 m/s
Silicio
El silicio (del latín: sílex) es un elemento químico metaloide, número atómico 14 y situado en el grupo 14 de la tabla periódica de los elementos de símbolo Si.1 Es el segundo elemento más abundante en la corteza terrestre (25,7 % en peso)2 después del oxígeno. Se presenta en forma amorfa y cristalizada; el primero es un polvo parduzco, más activo que la variante cristalina, que se presenta en octaedros de color azul grisáceo y brillo metálico.
Abundancia en la naturaleza
El silicio es uno de los componentes principales de los aerolitos, una clase de meteoroides.
Medido en peso, el silicio representa más de la cuarta parte de la corteza terrestre y es el segundo elemento más abundante por detrás del oxígeno. El silicio no se encuentra en estado nativo; arena, cuarzo, amatista, ágata, pedernal, ópalo y jaspe son algunos de los minerales en los que aparece el óxido, mientras que formando silicatos se encuentra, entre otros, en el granito, feldespato, arcilla, hornblenda y mica.
Aplicaciones
Se utiliza en aleaciones, en la decantación de las siliconas, en la industria de la cerámica técnica y, debido a que es un material semiconductor muy abundante, tiene un interés especial en la industria electrónica y microelectrónica como material básico para la creación de obleas o chips que se pueden implantar en transistores, pilas solares y una gran variedad de circuitos electrónicos. El silicio es un elemento vital en numerosas industrias. El dióxido de silicio (arena y arcilla) es un importante constituyente del hormigón y los ladrillos, y se emplea en la producción de cemento portland. Por sus propiedades semiconductoras se usa en la fabricación de transistores, células solares y todo tipo de dispositivos semiconductores; por esta razón se conoce como el Valle del Silicio a la región de California en la que concentran numerosas empresas del sector de la electrónica y la informática. También se están estudiando las posibles aplicaciones del siliceno, que es una forma alotrópica del silicio que forma una red bidimensional similar al grafeno.
Información general
Nombre: Silicio
Símbolo: Si
Número: 14
Serie Química: Metaloides
Grupo: 14
Período: 3
Bloque: p
Masa Atómica: 28.085 u
Configuración Electrónica: [Ne]3s23p2
Electrones por Nivel: 2,8,4
Propiedades Atómicas
Radio Medio: 120 pm
Electronegatividad: 1.9
Radio Atómico (calc): 111 pm
Radio Covalente: 111 pm
Radio de van der Waals: 210 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 2.33 kg/m3
Punto de fusión: 1687 K
Punto de ebullición: 3538 K
Varios
Estructura cristalina:
N° CAS: 7440-21-3
N° EINECS: 231-130-8
Velocidad del Sonido: 8433 m/s
Fósforo
El fósforo es un elemento químico de número atómico 15 y símbolo P. El nombre proviene del griego φώς [fos] ‘luz’ y φόρος [foros] ‘portador’. Es un no metal multivalente perteneciente al grupo del nitrógeno (Grupo 15 (VA): nitrogenoideos) que se encuentra en la naturaleza combinado en fosfatos inorgánicos y en organismos vivos pero nunca en estado fundamental. Es muy reactivo y se oxida espontáneamente en contacto con el oxígeno atmosférico emitiendo luz.
Es un ciclo sedimentario, su reservorio es la corteza terrestre. El elemento se almacena en rocas fosfatadas y a medida que estas son erosionadas se van liberando compuestos fosfatados hacia el suelo y el agua. Luego son absorbidos por las plantas, a través de las raíces, incorporándose a los componentes vivos del sistema, a medida que pasan por los distintos niveles tróficos. Una vez que los organismos (plantas o animales) mueren, se descomponen y se libera el fósforo contenido en la materia orgánica.
Historia
El fósforo —del latín phosphŏrus, y este del griego φωσφόρος, portador de luz— antiguo nombre del planeta Venus, fue descubierto por el alquimista alemán Hennig Brand en 1669 en Hamburgo al destilar una mezcla de orina y arena (utilizó 50 cubos) mientras buscaba la piedra filosofal; al evaporar la urea obtuvo un material blanco que brillaba en la oscuridad y ardía con una llama brillante; desde entonces, las sustancias que brillan en la oscuridad sin emitir calor se las llama fosforescentes. Brand mantuvo su descubrimiento en secreto pero otro alquimista alemán, Kunckel, lo redescubrió en 1677 y enseñó a Boyle la forma de producirlo y aplicarlo.
Abundancia en la naturaleza
Debido a su reactividad, el fósforo no se encuentra nativo en la naturaleza, pero forma parte de numerosos minerales. La apatita es una importante fuente de fósforo, existiendo importantes yacimientos en Marruecos, Rusia, Estados Unidos y otros países.
La forma alotrópica blanca se puede obtener por distintos procedimientos; en uno de ellos, el fosfato tricálcico, obtenido de las rocas, se calienta en un horno a 1450 °C en presencia de sílice y carbono reduciendo el fósforo que se libera en forma de vapor.
Información general
Nombre: Fósforo
Símbolo: P
Número: 15
Serie Química: No Metales
Grupo: 15
Período: 3
Bloque: p
Masa Atómica: 30.9737620 u
Configuración Electrónica: [Ne]3s23p3
Electrones por Nivel: 2,8,5
Propiedades Atómicas
Radio Medio: 100 pm
Electronegatividad: 2.19
Radio Atómico (calc): 98 pm
Radio Covalente: 106 pm
Radio de van der Waals: 180 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 1823 kg/m3
Punto de fusión: 317.3 K
Punto de ebullición: 550 K
Varios
Estructura cristalina: Monoclínica
N° CAS: 7723-14-0
N° EINECS: 231-768-7
Azufre
El azufre es un elemento químico de número atómico 16 y símbolo S (del latín sulphur). Es un no metal abundante con un color amarillo característico. Dicho elemento es generado en estrellas masivas en las que predominan temperaturas que provocan la fusión entre un núcleo de silicio y otro de helio en un proceso denominado nucleosíntesis de supernovas.
El azufre se encuentra en forma nativa en regiones volcánicas y en sus formas reducidas formando sulfuros y sulfosales o bien en sus formas oxidadas como sulfatos. Es un elemento químico esencial constituyente de los aminoácidos cisteina y metionina y, por consiguiente, necesario para la síntesis de proteínas presentes en todos los organismos vivos. Se usa principalmente como fertilizante pero también en la fabricación de pólvora, laxantes, fósforos e insecticidas.
Historia
El azufre (del latín sulphur, sulfŭris, vinculado con el sánscrito śulbāri) es conocido desde la Antigüedad, y ya los egipcios lo utilizaban para purificar los templos.
Abundancia en la naturaleza
El azufre es un elemento muy abundante en la corteza terrestre, se encuentra en grandes cantidades combinado en forma de sulfuros como pirita y galena y de sulfatos como yeso. En forma nativa se encuentra en las cercanías de aguas termales, zonas volcánicas y en minas de cinabrio, galena, esfalerita y estibina, y en Luisiana (Estados Unidos, primer productor mundial) se extrae mediante el proceso Frasch consistente en inyectar vapor de agua sobrecalentado para fundir el azufre que posteriormente es bombeado al exterior utilizando aire comprimido.También se obtiene separándolo del gas natural, si bien su obtención anteriormente era a partir de depósitos de azufre puro impregnado en cenizas volcánicas (Italia, y más recientemente Argentina).
También está presente, en pequeñas cantidades, en combustibles fósiles (carbón y petróleo) cuya combustión produce dióxido de azufre que combinado con agua produce la lluvia ácida; para evitarlo las legislaciones de los países industrializados exigen la reducción del contenido de azufre de los combustibles, constituyendo este azufre, posteriormente refinado, un porcentaje importante del total producido en el mundo. También se extrae del gas natural que contiene sulfuro de hidrógeno que una vez separado se quema para obtener azufre.
El color distintivo de Ío, la luna volcánica de Júpiter, se debe a la presencia de diferentes formas de azufre en estado líquido, sólido y gaseoso. El azufre se encuentra, además, en varios tipos de meteoritos, y se cree que la mancha oscura que puede observarse cerca del cráter lunar Aristarco puede ser un depósito de azufre.
Aplicaciones
El azufre se usa en multitud de procesos industriales, como la producción de ácido sulfúrico para baterías, la fabricación de pólvora y el vulcanizado del caucho.
Los sulfitos se usan para blanquear el papel y en fósforos. El tiosulfato de sodio o amonio se emplea en la industria fotográfica como «fijador» ya que disuelve el bromuro de plata; y el sulfato de magnesio (sal de Epsom) tiene usos diversos como laxante, exfoliante, o suplemento nutritivo para plantas.
También el azufre se emplea en la industria enológica como antiséptico. Uno de sus principales usos es como anhídrido sulfuroso.
El azufre tiene usos como fungicida y en la manufactura de fosfatos fertilizantes.
Información general
Nombre: Azufre
Símbolo: S
Número: 16
Serie Química: No Metales
Grupo: 16
Período: 3
Bloque: p
Masa Atómica: 32.065 u
Configuración Electrónica: [Ne]3s23p4
Electrones por Nivel: 2,8,6
Propiedades Atómicas
Radio Medio: 100 pm
Electronegatividad: 2.58
Radio Atómico (calc): 88 pm
Radio Covalente: 102 pm
Radio de van der Waals: 180 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 1960 kg/m3
Punto de fusión: 388.36 K
Punto de ebullición: 717.87 K
Varios
Estructura cristalina: Ortorrómbica
N° CAS: 7704-34-9
N° EINECS: 231-722-6
Cloro
El cloro es un elemento químico de número atómico 17 situado en el grupo de los halógenos (grupo VIIA) de la tabla periódica de los elementos. Su símbolo es Cl. En condiciones normales y en estado puro forma dicloro: un gas tóxico amarillo-verdoso formado por moléculas diatómicas (Cl2) unas 2,5 veces más pesado que el aire, de olor desagradable y tóxico. Es un elemento abundante en la naturaleza y se trata de un elemento químico esencial para muchas formas de vida.
Historia
El cloro (del griego χλωρος, que significa «verde pálido») fue descubierto en su forma diatómica en 1774 por el sueco Carl Wilhelm Scheele, aunque creía que se trataba de un compuesto que contenía oxígeno.
Además de su carácter asfixiante, descubrió que decoloraba muchos pigmentos vegetales. Poco después, Claude Louis Berthollet llevó este descubrimiento a la práctica, para el blanqueo de tejidos, utilizando una disolución de cloro en agua. Leonard Alban y Mathieu Vallet introdujeron una mejora muy importante, al disolver el cloro en una solución de potasa en agua, lo que reducía el desprendimiento de vapores tóxicos. Por su parte, Charles Tennant obtuvo el hipoclorito de calcio, haciendo reaccionar el cloro gas con cal sólida. Este material era más eficaz como decolorante, y más fácil de manejar.
En 1810 el químico inglés Humphry Davy demostró que se trataba de un elemento químico, al que dio el nombre de cloro debido a su color. El gas cloro se empleó en la Primera Guerra Mundial, siendo el primer caso de uso de armas químicas como el fosgeno y el gas mostaza.
Abundancia en la naturaleza
El cloro se encuentra en la naturaleza combinado con otros elementos formando principalmente sales iónicas; como es el caso del cloruro sódico y cálcico; también con la mayoría de metales; desde el cloruro de hafnio hasta el cloruro de plata. Podría decirse que el cloro combina de forma natural bastante bien con la mayoría de elementos, excepto con los de su grupo, halógenos y gases nobles, aunque en las últimas décadas de manera sintética forma parte de los mismos en compuestos conocidos como son los fluorocloruros y cloruros de xenón.
Finalmente cabe destacar que la gran mayoría de estos compuestos suelen encontrarse con impurezas formando parte de minerales como la carnalita.
Aplicaciones
El cloro tiene diversos usos en la producción de insumos industriales y de consumo, purificación y desinfección, químca, geología y aún como arma química.
Información general
Nombre: Cloro
Símbolo: Cl
Número: 17
Serie Química: Halógenos
Grupo: 17
Período: 3
Bloque: p
Masa Atómica: 35.453 u
Configuración Electrónica: [Ne]3s23p5
Electrones por Nivel: 2,8,7
Propiedades Atómicas
Radio Medio: 100 pm
Electronegatividad: 3.16
Radio Atómico (calc): 79 pm
Radio Covalente: 99 pm
Radio de van der Waals: 175 pm
Propiedades Físicas
Estado Ordinario: Gas
Densidad: 3.214 kg/m3
Punto de fusión: 171.16 K
Punto de ebullición: 239.16 K
Varios
Estructura cristalina: Ortorrómbica
N° CAS: 7782-50-5
N° EINECS: 231-959-5
Argón
El argón es un elemento químico de número atómico 18 y símbolo Ar. Es el tercero de los gases nobles, incoloro e inerte como ellos, constituye el 0,934 % del aire seco. Su nombre proviene del griego ἀργός [argos], que significa inactivo (debido a que no reacciona).
Historia
Henry Cavendish, en 1785, expuso una muestra de nitrógeno a descargas eléctricas repetidas en presencia de oxígeno para formar óxido de nitrógeno que posteriormente eliminaba y encontró que alrededor del 1 % del gas original no se podía disolver, afirmando entonces que no todo el «aire flogisticado» era nitrógeno. En 1892 Lord Rayleigh descubrió que el nitrógeno atmosférico tenía una densidad mayor que el nitrógeno puro obtenido a partir del nitro. Rayleigh y Sir William Ramsay demostraron que la diferencia se debía a la presencia de un segundo gas poco reactivo más pesado que el nitrógeno, anunciando el descubrimiento del argón (del griego αργóν, inactivo, vago o perezoso) en 1894, anuncio que fue acogido con bastante escepticismo por la comunidad científica.
En 1904 Rayleigh recibió el premio Nobel de Física por sus investigaciones acerca de la densidad de los gases más importantes y el descubrimiento de la existencia del argón.
Abundancia en la naturaleza
El gas se obtiene por medio de la destilación fraccionada del aire licuado, en el que se encuentra en una proporción de aproximadamente el 0,94 %, y posterior eliminación del oxígeno residual con hidrógeno.
Aplicaciones
Se emplea como gas de relleno en lámparas incandescentes ya que no reacciona con el material del filamento incluso a alta temperatura y presión, prolongando de este modo la vida útil de la bombilla, y en sustitución del neón en lámparas fluorescentes cuando se desea un color verde-azul en vez del rojo del neón. También como sustituto del nitrógeno molecular cuando este no se comporta como gas inerte por las condiciones de operación.
En el ámbito industrial y científico se emplea universalmente de la recreación de atmósferas inertes (no reaccionantes) para evitar reacciones químicas indeseadas en multitud de operaciones.
Información general
Nombre: Argón
Símbolo: Ar
Número: 18
Serie Química: Gases Nobles
Grupo: 18
Período: 3
Bloque: p
Masa Atómica: 39.948 u
Configuración Electrónica: [Ne]3s23p6
Electrones por Nivel: 2,8,8
Propiedades Atómicas
Radio Atómico (calc): 71 pm
Radio Covalente: 97pm
Radio de van der Waals: 188 pm
Propiedades Físicas
Estado Ordinario: Gas
Densidad: 1.784 kg/m3
Punto de fusión: 83.8 K
Punto de ebullición: 87.3 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-37-1
N° EINECS: 231-147-0
Velocidad del Sonido: 319 m/s
Potasio
El potasio es un elemento químico de la tabla periódica cuyo símbolo químico es K (del latín Kalium y del árabe. القلية, DMG al-qalya, "ceniza de plantas"), cuyo número atómico es 19. Es un metal alcalino de color blanco-plateado, que abunda en la naturaleza en los elementos relacionados con el agua salada y otros minerales. Se oxida rápidamente en el aire, es muy reactivo, especialmente en agua, y se parece químicamente al sodio.
Características principales
Es el quinto metal más ligero y liviano; es un sólido blando que se corta con facilidad con un cuchillo, tiene un punto de fusión muy bajo, arde con llama violeta y presenta un color plateado en las superficies expuestas al aire, en cuyo contacto se oxida con rapidez, lo que obliga a almacenarlo recubierto de aceite.
Al igual que otros metales alcalinos reacciona violentamente con el agua desprendiendo hidrógeno, incluso puede inflamarse espontáneamente en presencia de agua
Aplicaciones
- El potasio metal se usa en células fotoeléctricas.
- El cloruro y el nitrato se emplean como fertilizantes.
- El peróxido de potasio se usa en aparatos de respiración autónomos de bomberos y mineros.
- El nitrato se usa en la fabricación de pólvora y el cromato y dicromato en pirotecnia.
- El carbonato potásico se emplea en la fabricación de cristales.
- La aleación NaK, una aleación de sodio y potasio, es un material empleado para la transferencia de calor.
- El cloruro de potasio se utiliza para provocar un paro cardíaco en las ejecuciones con inyección letal.
Otras sales de potasio importantes son el bromuro, cianuro, hidróxido, yoduro, y el sulfato.
El ion K+ está presente en los extremos de los cromosomas (en los telómeros) estabilizando la estructura. Asimismo, el ion hexahidratado (al igual que el correspondiente ion de magnesio) estabiliza la estructura del ADN y del ARN compensando la carga negativa de los grupos fosfato.
La bomba de sodio es un mecanismo por el cual se consiguen las concentraciones requeridas de iones K+ y Na+ dentro y fuera de la célula —concentraciones de iones K+ más altas dentro de la célula que en el exterior— para posibilitar la transmisión del impulso nervioso.
Las hortalizas (brócoli, remolacha, berenjena y coliflor) judías y las frutas (los bananos y las de hueso, como aguacate, albaricoque, melocotón, cereza, ciruela), son alimentos ricos en potasio.
El descenso del nivel de potasio en la sangre provoca hipopotasemia.
Es uno de los elementos esenciales para el crecimiento de las plantas —es uno de los tres que se consumen en mayor cantidad— ya que el ion potasio, que se encuentra en la mayoría de los tipos de suelo, interviene en la respiración.
Historia
El potasio (del latín científico potassium, y éste del alemán pottasche, ceniza de pote) nombre con que lo bautizó Humphrey Davy al descubrirlo en 1807, fue el primer elemento metálico aislado por electrólisis, en su caso del hidróxido de potasio (KOH), compuesto de cuyo nombre latino, Kalĭum, proviene el símbolo químico del potasio.
El propio Davy hacía el siguiente relato de su descubrimiento ante la Royal Society of London el 19 de noviembre de 1807: «Coloqué un pequeño fragmento de potasa sobre un disco aislado de platino que comunicaba con el lado negativo de una batería eléctrica de 250 placas de cobre y zinc en plena actividad. Un hilo de platino que comunicaba con el lado positivo fue puesto en contacto con la cara superior de la potasa. Todo el aparato funcionaba al aire libre. En estas circunstancias se manifestó una actividad muy viva; la potasa empezó a fundirse en sus dos puntos de electrización. Hubo en la cara superior (positiva) una viva efervescencia, determinada por el desprendimiento de un fluido elástico; en la cara inferior (negativa) no se desprendía ningún fluido elástico, pero pequeños glóbulos de vivo brillo metálico completamente semejantes a los glóbulos de mercurio. Algunos de estos glóbulos, a medida que se formaban, ardían con explosión y llama brillante; otros perdían poco a poco su brillo y se cubrían finalmente de una costra blanca. Estos glóbulos formaban la sustancia que yo buscaba; era un principio combustible particular, era la base de la potasa: el potasio.»
La importancia del descubrimiento radica en que confirmó la hipótesis de Antoine Lavoisier de que si la sosa y la potasa reaccionaban con los ácidos de igual modo que los óxidos de plomo y plata era porque estaban formados de la combinación de un metal con el oxígeno, extremo que se confirmó al aislar el potasio y tan solo una semana después el sodio por electrólisis de la sosa. Además, la obtención del potasio permitió el descubrimiento de otros elementos, ya que dada su gran reactividad es capaz de descomponer óxidos para combinarse y quedarse con el oxígeno; de este modo pudieron aislarse el silicio, el boro y el aluminio.
Abundancia
El potasio constituye del orden del 2,4 % en peso de la corteza terrestre siendo el séptimo más abundante. Debido a su solubilidad es muy difícil obtener el metal puro a partir de sus minerales. Aun así, en antiguos lechos marinos y de lagos existen grandes depósitos de minerales de potasio (carnalita, langbeinita, polihalita y silvina) en los que la extracción del metal y sus sales es económicamente viable.
Información general
Nombre: Potasio
Símbolo: K
Número: 19
Serie Química: Metales Alcalinos
Grupo: 1
Período: 4
Bloque: s
Masa Atómica: 39,0983 u
Configuración Electrónica: [Ar]4s1
Electrones por Nivel: 2, 8, 8, 1
Calcio
El calcio (del latín calx, calis, cal) es un elemento químico, de símbolo Ca y de número atómico 20. Su masa atómica es 40,078 u. El calcio es un metal blando, grisáceo, y es el quinto más abundante en masa de la corteza terrestre. También es el ion más abundante disuelto en el agua de mar, tanto como por su molaridad y como por su masa, después del sodio, cloruros, magnesio y sulfatos.
Se encuentra en el medio interno de los organismos como ion calcio (Ca2+) o formando parte de otras moléculas; en algunos seres vivos se halla precipitado en forma de esqueleto interno (huesos de los vertebrados) o externo (concha de los moluscos). Los iones de calcio actúan de cofactor en muchas reacciones enzimáticas, intervienen en el metabolismo del glucógeno y, junto al potasio y el sodio, regulan la contracción muscular. El porcentaje de calcio en los organismos es variable y depende de las especies, pero por término medio representa el 2,45 % en el conjunto de los seres vivos; en los vegetales, solo representa el 0,007 %.
Historia
El calcio fue descubierto en 1808 por Humphry Davy mediante electrólisis de una amalgama de mercurio y cal. Davy mezcló cal humedecida con óxido de mercurio que colocó sobre una lámina de platino, el ánodo, y sumergió una parte del mercurio en el interior de la pasta para que hiciera de cátodo; por electrólisis obtuvo una amalgama que, destilada, dejó un residuo sólido muy oxidable, aunque ni siquiera el mismo Davy estaba muy seguro de haber obtenido calcio puro; con posterioridad Bunsen en 1854 y Matthiessen en 1856 obtuvieron el metal por electrólisis del cloruro de calcio, y Henri Moissan obtuvo calcio con una pureza del 99 % por electrólisis del yoduro. A principios del siglo XX el calcio solo se obtenía en laboratorio.
Abundancia en la naturaleza
Es el quinto elemento en abundancia en la corteza terrestre (3,5 % en peso) pero no se encuentra solo sino formando compuestos con gran interés industrial como los carbonatos (minerales como calcita y dolomita o rocas como el mármol, la caliza y la dolomia) o el sulfato cálcico (yeso, alabastro) a partir de los cuales se obtienen la cal viva, la escayola, el cemento, etc.; otros minerales que lo contienen son fluorita (CaF2) y apatito (fosfato).
Aplicaciones
El calcio es un agente reductor en la extracción de otros metales como el uranio, circonio y torio, también es un desoxidante, desulfurizador, o decarburizador para varias aleaciones ferrosas y no ferrosas, es un agente de aleación utilizado en la producción de aluminio, berilio, cobre, plomo y magnesio y tiene aplicaciones en muchos productos lácteos o medicamentos para el refuerzo de los huesos. La falta de calcio en los huesos humanos facilita la aparición de enfermedades como la osteoporosis.
El óxido de calcio se produce por descomposición térmica de la caliza, roca rica en carbonato de calcio, en altos hornos, aplicando un proceso de lecho continuo. El óxido, llamado cal viva, es ampliamente usado en la construcción. También se utiliza en arcos de luz de alta intensidad (luz de cal) a causa de sus características espectrales poco usuales y como agente deshidratante industrial. La industria metalúrgica hace amplio uso del óxido durante la reducción de aleaciones ferrosas.
El hidróxido de calcio, llamado cal apagada, tiene muchas aplicaciones en donde el ion hidroxilo es necesario. En el proceso de apagado del óxido de calcio, el volumen de cal apagada se expande al doble que la cantidad de cal viva inicial, hecho que lo hace útil para romper roca o madera.
Información general
Nombre: Calcio
Símbolo: Ca
Número: 20
Serie Química: Metales Alcalinotérreos
Grupo: 2
Período: 4
Bloque: s
Masa Atómica: 40.078 u
Configuración Electrónica: [Ar]4s2
Electrones por Nivel: 2,8,8,2
Propiedades Atómicas
Radio Medio: 180 pm
Electronegatividad: 1.00
Radio Atómico (calc): 194 pm
Radio Covalente: 176 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 1550 kg/m3
Punto de fusión: 1115 K
Punto de ebullición: 1757 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-70-2
N° EINECS: 231-179-5
Velocidad del Sonido: 3810 m/s
Escandio
El escandio es un elemento químico de la tabla periódica cuyo símbolo es Sc y su número atómico es 21. Es un metal de transición que se encuentra en minerales de Escandinavia y que se clasifica con frecuencia entre los lantánidos por sus similitudes con ellos.
Historia
El escandio (del latín científico scandĭum, y éste de Scandio, Escandinavia) fue descubierto por Lars Fredrick Nilson en 1879 mientras trabajaba con su equipo en la búsqueda de metales tierras raras mediante análisis espectral de los minerales euxenita y gadolinita. Para aislar el elemento procesó 10 kg de exenita con otros residuos de tierras raras logrando aproximadamente 2 gramos de óxido de gran pureza.
En 1869 Dmitri Mendeleyev predijo, basándose en las leyes periódicas, que este metal debía tener propiedades similares a las del boro por lo que llamó al elemento aún por descubrir ekaboro (símbolo Eb). Aproximadamente en la misma época que Nilson, Per Theodor Cleve descubrió el óxido de escandio y confirmó que se trataba del ekaboro.
En 1937 se aisló por vez primera el metal por electrólisis de una solución eutéctica de potasio, litio y cloruros de escandio a 700-800 °C empleando como electrodos un filamento de wolframio y un baño de cinc líquido en un crisol de grafito. La primera libra de escandio del 99% de pureza se fabricó en 1960.
Abundancia en la naturaleza
Las únicas fuentes concentradas conocidas del metal, que no se encuentra en estado nativo, son minerales poco abundantes de Escandinavia y Madagascar como euxenita, gadolinita y thortveitita.
Es más abundante en el Sol y estrellas similares (23.º en abundancia) que en la Tierra (50.º) donde se encuentra muy repartido, apareciendo trazas del metal en más de 800 minerales. El color azul del aguamarina, variedad del berilo, se cree que se debe a la presencia de escandio y aparece entre los residuos de la wolframita tras la extracción del wolframio.
La thortveitita es la principal mena de escandio siendo otra fuente importante los residuos de la extracción del uranio donde se obtiene como subproducto. El metal se obtiene industrialmente por reducción del fluoruro de escandio con calcio.
Aplicaciones
El óxido de escandio, se utiliza en luces de alta intensidad y añadiendo yoduro de escandio en las lámparas de vapor de mercurio se consigue una luz solar artificial de muy alta calidad. El isótopo radiactivo Sc-46 se usa en el craqueo del petróleo como trazador.
La adición de escandio al aluminio limita el crecimiento excesivo del grano que se produce en la zona afectada por el calor en la soldadura de aleaciones de aluminio. Esto tiene dos efectos beneficiosos: El precipitado forma cristales menores que los que se forman en otras aleaciones de aluminio y el volumen de las zonas libres de precipitado que normalmente existen en los límites de grano de las aleaciones de aluminio endurecido por envejecimiento se reduce. Ambos efectos aumentan la utilidad de la aleación. Sin embargo, las aleaciones de titanio, que son similares en ligereza y resistencia, son más baratas y mucho más ampliamente utilizadas.
La aplicación principal del escandio en peso es en las aleaciones de aluminio-escandio para componentes menores de la industria aeroespacial. Estas aleaciones contienen entre 0,1 % y 0,5 % del escandio. Estas fueron utilizadas en los aviones militares rusos Mig 21 y Mig 29.
Información general
Nombre: Escandio
Símbolo: Sc
Número: 21
Serie Química: Metales de Transición
Grupo: 3
Período: 4
Bloque: d
Masa Atómica: 44.955910 u
Configuración Electrónica: [Ar]4s23d1
Electrones por Nivel: 2,8,9,2
Propiedades Atómicas
Radio Medio: 160 pm
Electronegatividad: 1.36
Radio Atómico (calc): 184 pm
Radio Covalente: 144 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 2985 kg/m3
Punto de fusión: 1814 K
Punto de ebullición: 3103 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-20-2
N° EINECS: 231-129-2
Titanio
El titanio es un elemento químico de símbolo Ti y número atómico 22 que se sitúa en el grupo 4 de la tabla periódica de los elementos. Es un metal de transición de color gris, baja densidad y gran dureza. Es muy resistente a la corrosión por agua del mar, agua regia y cloro.
En estado puro, presenta una elevada resistencia a la corrosión y la mayor proporción de dureza-densidad de todos los elementos metálicos.6 El titanio es tan fuerte como algunos aceros, pero su densidad es menor. Tiene dos formas alotrópicas y cinco isótopos naturales que van desde 46Ti hasta 50Ti, siendo 48Ti el más abundante de ellos.
El titanio puede formar aleaciones con el hierro, el aluminio, el vanadio y el molibdeno entre otros elementos, idóneas por sus propiedades de ligereza y resistencia para la construcción de maquinaria para aplicaciones aeroespaciales —motores de reacción, misiles y naves espaciales—, militares, industriales —almacenamiento y transporte de productos químicos y petroquímicos, y plantas de desalinización—, en la automoción, para prótesis médicas e implantes ortopédicos, instrumentos e implantes dentales, aparatos deportivos, joyería o teléfonos móviles.
Historia
El titanio fue descubierto dentro de un mineral en Cornualles, Gran Bretaña, en 1791 por el clérigo y geólogo aficionado William Gregor, que por aquel entonces era el pastor de la parroquia de Creed. Reconoció la presencia de un nuevo elemento en la ilmenita5 al encontrar una arena negra en un riachuelo en la parroquia de Manaccan y observó que la arena era atraída por un imán. Su análisis de la arena determinó la presencia de dos óxidos de metales: óxido de hierro (lo que provocaba la atracción magnética) y una proporción de un 45,25% de otro óxido metálico blanco que no fue capaz de identificar. Como este óxido sin identificar contenía un metal que no cumplía las propiedades de ninguno de los elementos conocidos, informó de su descubrimiento a la Royal Geological Society of Cornwall y a la revista científica alemana Crell's Annalen, dándole el nombre de manacanita.
Sobre el mismo tiempo, Franz-Joseph Müller von Reichenstein produjo una substancia semejante que tampoco fue capaz de identificar. El óxido fue descubierto de nuevo de forma independiente en 1795 por el químico prusiano Martin Heinrich Klaproth en un mineral de rutilo en la villa húngara de Boinik, en la actual Eslovaquia. Klaproth encontró que el mineral contenía un nuevo elemento y le dio el nombre de titanio por los titanes de la mitología griega. Tras saber del descubrimiento previo de Gregor, obtuvo una muestra de manacanita y confirmó que esta contenía titanio.
Aplicaciones
El titanio se emplea en las aleaciones de acero para reducir el tamaño del grano y como desoxidante, y en las de acero inoxidable para reducir su contenido de carbono.3 Son frecuentes también las aleaciones con aluminio, vanadio, cobre, hierro, manganeso, molibdeno y otros metales.
Información general
Titanio
Nombre: Titanio
Símbolo: Ti
Número: 22
Serie Química: Metales de Transición
Grupo: 4
Período: 4
Bloque: d
Masa Atómica: 47.867 u
Configuración Electrónica: [Ar]3d24s2
Electrones por Nivel: 2,8,10,2
Propiedades Atómicas
Radio Medio: 140 pm
Electronegatividad: 1.54
Radio Atómico (calc): 176 pm
Radio Covalente: 136 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 4507 kg/m3
Punto de fusión: 1941 K
Punto de ebullición: 3560 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-32-6
N° EINECS: 231-142-3
Velocidad del Sonido: 4140 m/s
Vanadio
El vanadio es un elemento químico de número atómico 23 situado en el grupo 5 de la tabla periódica de los elementos. Su símbolo es V. Es un metal dúctil pero duro, poco abundante. Se encuentra en distintos minerales y se emplea principalmente en algunas aleaciones. El nombre procede de la diosa de la belleza Vanadis en la mitología escandinava.
Es un metal, de color blanco agrisado, maleable y de transición dúctil. La formación de una capa de óxido del metal estabiliza al elemento contra la oxidación.
El elemento se encuentra naturalmente en minerales; hay cerca de sesenta y cinco diferentes tipos y en los depósitos de combustibles fósiles. Los más representativos son la patronita (un sulfuro complejo), la vanadinita y carnotita. Este último es más importante como mineral de uranio, pero también se puede recuperar el vanadio. Se produce en China y Rusia, otros países lo producen o bien por el polvo de combustión de aceite pesado, o como un subproducto de la minería de uranio. Se utiliza principalmente para producir aleaciones de aceros especiales, tales como aceros para herramientas de alta velocidad. El pentóxido de vanadio se utiliza como catalizador para la producción de ácido sulfúrico. El vanadio se encuentra en muchos organismos, y es utilizado por algunas formas de vida como un centro activo de las enzimas.
Historia
En 1801, al examinar muestras minerales procedentes de Zimapán en el actual Estado de Hidalgo en México, Andrés Manuel del Río llegó a la conclusión de que había encontrado un nuevo elemento metálico. Del Río extrajo el elemento de una muestra de plomo "marrón" de mineral mexicano, al que llamó "zimapanio", más tarde llamado "vanadinita".
Preparó varios compuestos con él y al observar la diversidad de colores que presentaban, lo denominó "pancromio" (muchos colores, en griego). Poco después, al observar que los compuestos calentados cambiaban su color al rojo, denominó al nuevo elemento como eritronio (eritros, significa rojo en griego).
Un año después, aprovechando la visita al país del ilustre Alexander von Humboldt, considerado el más importante científico de su tiempo, el investigador español le confió una muestra del mineral y las notas con su análisis, descubrimiento y el procedimiento empleado para ello a fin de que las llevase a Europa, para que se confirmase y certificase su descubrimiento y para la publicación del mismo en las revistas más prestigiosas. Sin embargo, el barco de equipaje en el que viajaba gran parte del material entregado a Humboldt, incluidas las notas de Del Río, naufragó. Humboldt sólo conservó la muestra, que entregó al químico francés Hippolyte Victor Collet-Descotils en París para su análisis. Collet-Descotils analizó las muestras e informó —equivocadamente— que el presunto nuevo elemento era en realidad cromo, descubierto apenas unos años antes, en 1797, lo que desacreditaba la investigación, por lo que von Humboldt, a su vez, rechazó la pretensión de Del Río sobre un nuevo elemento. Puesto en conocimiento de ello, aunque en un principio Del Río mostró su desacuerdo, al final se resignó a aceptar la declaración y resultados de Collet-Descotils, y se retractó de su afirmación. Reclamando que, al menos, fuese reconocido como el primero en descubrir cromo en América.
El elemento fue redescubierto en 1831 por el químico sueco Nils Gabriel Sefström, mientras trabajaba en un óxido obtenido de minerales de hierro. Más tarde, ese mismo año, Friedrich Wöhler confirmó los principios de la obra de Del Río. Sefström eligió un nombre que comenzase con V, ya que la letra no había sido asignada aún a ningún otro elemento. Lo llamó vanadio en honor a la diosa escandinava Vanadis, nombre que oficialmente mantiene hasta la fecha, debido a los numerosos compuestos químicos de colores que produce. En 1831, el geólogo George William Featherstonhaugh sugirió que el vanadio debería llamarse "rionium" en honor a Del Río, pero esta sugerencia no fue seguida.
El aislamiento del vanadio fue difícil. En 1831, Jöns Jacob Berzelius informó la producción del metal, pero Henry Enfield Roscoe demostró que en realidad había producido nitruro de vanadio (VN). Roscoe produjo finalmente el metal en 1867 por la reducción de vanadio (III), con el hidrógeno. En 1927, se produjo vanadio puro por la reducción de pentóxido de vanadio con calcio. El primer uso a gran escala industrial del vanadio en el acero se encontró en el chasis del Ford T, inspirado en los autos de carreras franceses. El acero de vanadio permitió reducir el peso y al mismo tiempo aumentar la fuerza de tracción.
Abundancia en la naturaleza
El vanadio no se encuentra nunca en estado nativo, pero está presente en unos 65 minerales diferentes, entre los que destacan la patronita, vanadinita, y la carnotita. También se encuentra en la bauxita, así como en depósitos que contienen carbono, como por ejemplo en carbón, petróleos, crudo y alquitrán. Está presente en el petróleo formando estructuras tipo porfirinas. Además, se obtiene pentóxido de vanadio, recuperándolo de la combustión del petróleo.
Los vanadatos se disuelven mediante una fusión alcalina. En medio ácido y tras otros procesos se obtiene el que se reduce parcialmente con carbono, y luego con calcio en atmósfera de argón para obtener vanadio metálico.
En el caso de que no se parta de un mineral que contenga el vanadato, sino un sulfuro, éste se oxida para obtener el vanadato y se realiza el mismo procedimiento para obtener vanadio.
Si se quiere obtener vanadio más puro, se emplea el método Van Arkel-de Boer (formación de un compuesto volátil y su posterior descomposición).
Aplicaciones
La mayor parte del vanadio se utiliza como ferrovanadio como aditivo para mejorar los aceros. El ferrovanadio se produce directamente por la reducción de una mezcla de óxido de vanadio, óxidos de hierro y de hierro en un horno eléctrico. El vanadio termina en arrabio producido a partir de la magnetita de vanadio. Durante la producción de acero, el oxígeno es soplado en la fundición de hierro, la oxidación del carbono y la mayoría de las otras impurezas, formando escoria. Dependiendo del mineral utilizado, la escoria contiene hasta un 25% de vanadio.
Información general
Nombre: Vanadio
Símbolo: V
Número: 23
Serie Química: Metales de Transición
Grupo: 5
Período: 4
Bloque: d
Masa Atómica: 50.9415 u
Configuración Electrónica: [Ar]4s23d3
Electrones por Nivel: 2,8,11,2
Propiedades Atómicas
Radio Medio: 135 pm
Electronegatividad: 1.63
Radio Atómico (calc): 171 pm
Radio Covalente: 125 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 6110 kg/m3
Punto de fusión: 2175 K
Punto de ebullición: 3682 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7440-62-2
N° EINECS: 231-171-1
Velocidad del Sonido: 4560 m/s
Cromo
El cromo es un elemento químico de número atómico 24 que se encuentra en el grupo 6 de la tabla periódica de los elementos. Su símbolo es Cr. Es un metal que se emplea especialmente en metalurgia. Su nombre cromo (derivado del griego chroma, ‘color’) se debe a los distintos colores que presentan sus compuestos.
Historia
En 1766, el mineralogista alemán Johann Gottlob Lehmann analizó un mineral de color anaranjado rojizo conocido como plomo rojo de Siberia. Pudo determinar que contenía plomo y algún otro elemento, que finalmente no pudo descubrir ya que murió al año siguiente. El mineral molido resultaba ser muy útil en pinturas debido a sus propiedades de estabilidad como pigmento. Esta aplicación se extendió con rapidez, por ejemplo, se puso de moda un amarillo brillante, el amarillo de cromo, obtenido a partir de la crocoíta. Además los ejemplares con cristales de buena calidad eran muy apreciados por los coleccionistas.
En 1797 el químico francés Louis Nicolas Vauquelin obtuvo muestras del mineral, y mediante tratamiento con carbonato potásico fue capaz de precipitar el plomo manteniendo en disolución una substancia desconocida que daba sales coloreados con otros metales. Posteriormente preparó el óxido de ese elemento, y en 1798 descubrió que se podía aislar cromo metálico calentando el óxido con carbón en polvo. Lo llamó cromo (del griego χρῶμα, chrōma, "color") debido a los distintos colores que presentan sus compuestos. También pudo detectar trazas de cromo en gemas preciosas, como por ejemplo, en rubíes y esmeraldas.
El cromo se empleó principalmente en pinturas y otras aplicaciones hasta que, a finales del siglo XIX, se empleó como aditivo en aceros. Este uso no se extendió hasta principios del siglo XX, cuando se comenzó a obtener cromo metálico mediante aluminotermia. Actualmente en torno a un 85% del cromo se utiliza en aleaciones metálicas.
Abundancia en la naturaleza
Se obtiene cromo a partir de la cromita. La cromita se obtiene comercialmente calentando a la cromadora en presencia de aluminio o silicio (mediante un proceso de reducción). Aproximadamente la mitad de las cromitas se extraen de Sudáfrica. También se obtienen en grandes cantidades en Kazajistán, India y Turquía.
Aplicaciones
- El cromo se utiliza principalmente en metalurgia para aportar resistencia a la corrosión y un acabado brillante.
- En aleaciones, por ejemplo, el acero inoxidable es aquel que contiene más del 12% de cromo, aunque las propiedades antioxidantes del cromo empiezan a notarse a partir del 5% de concentración. Además tiene un efecto alfágeno, es decir, abre el campo de la ferrita y lo fija.
- En procesos de cromado (depositar una capa protectora mediante electrodeposición). También se utiliza en el anodizado del aluminio.
- En pinturas cromadas como tratamiento antioxidante.
- Sus cromatos y óxidos se emplean en colorantes y pinturas. En general, sus sales se emplean, debido a sus variados colores, como mordientes.
- El dicromato de potasio es un reactivo químico que se emplea en la limpieza de material de vidrio de laboratorio y, en análisis volumétricos, como agente valorante.
- Es común el uso del cromo y de alguno de sus óxidos como catalizadores, por ejemplo, en la síntesis de amoníaco.
- El mineral cromita se emplea en moldes para la fabricación de ladrillos (en general, para fabricar materiales refractarios). Con todo, una buena parte de la cromita consumida se emplea para obtener cromo o aleaciones.
Información general
Nombre: Cromo
Símbolo: Cr
Número: 24
Serie Química: Metales de Transición
Grupo: 6
Período: 4
Bloque: d
Masa Atómica: 51.9961 u
Configuración Electrónica: [Ar]3d55s1
Electrones por Nivel: 2,8,13,1
Propiedades Atómicas
Radio Medio: 140 pm
Electronegatividad: 1.66
Radio Atómico (calc): 166 pm
Radio Covalente: 127 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7140 kg/m3
Punto de fusión: 2130 K
Punto de ebullición: 2945 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7440-47-3
N° EINECS: 231-157-5
Velocidad del Sonido: 5940 m/s
Manganeso
El manganeso es un elemento químico de número atómico 25 situado en el grupo 7 de la tabla periódica de los elementos y se simboliza como Mn. Se encuentra como elemento libre en la naturaleza, a menudo en combinación con el hierro y en muchos minerales. Como elemento libre, el manganeso es un metal con aleación de metales industriales con importantes usos, sobre todo en los aceros inoxidables.
El fosfatado de manganeso se utiliza como tratamiento para la prevención de la oxidación y corrosión del acero. Dependiendo de su estado de oxidación, los iones de manganeso tienen colores diferentes y se utilizan industrialmente como pigmentos. Los permanganatos alcalinos y de metales alcalinotérreos son oxidantes poderosos. El dióxido de manganeso se utiliza como cátodo.
Los iones de manganeso funcionan como cofactores de una serie de enzimas en los organismos superiores, donde son esenciales en la desintoxicación de los radicales libres de superóxido. El elemento es un mineral traza esencial para todos los seres vivos conocidos. En cantidades mayores, y al parecer con una actividad mucho mayor por la inhalación, el manganeso puede causar un síndrome de intoxicación en los mamíferos, con daños neurológicos que a veces son irreversibles.
Historia
Se ha encontrado dióxido de manganeso, en pinturas rupestres (dando un color negro). También se han utilizado a lo largo de la historia, por ejemplo por los egipcios y los romanos, compuestos de manganeso para decolorar el vidrio o bien darle color. Asimismo se ha encontrado manganeso en las minas de hierro utilizadas por los espartanos, y se piensa que tal vez sea debido a esto la especial dureza de sus aceros.
En el siglo XVII, el químico alemán Glauber, produjo por primera vez permanganato, un reactivo de laboratorio bastante utilizado. A mediados del siglo XVIII, el dióxido de manganeso se empleó para la producción de cloro. El químico sueco Scheele fue el primero en describir que el manganeso era un elemento, pero fue Johan Gottlieb Gahn quien lo aisló por reducción del dióxido con carbono (1774), unos años después de los experimentos realizados en Viena por Ignatius Gottfried Kaim (1770), descritos en su obra "De metalleis dubiis" y que, a pesar de su escasa difusión, le confirman como el primer científico en aislar el manganeso.
A principios del siglo XIX se comenzó a probar el manganeso en aleaciones de acero. En 1816 se comprobó que endurecía al acero, sin hacerlo más frágil.
Abundancia en la naturaleza
Es el duodécimo elemento más abundante en la corteza terrestre y está ampliamente distribuido.
Se encuentra en cientos de minerales, aunque solo una docena tiene interés industrial. Destacan: pirolusita, psilomelana, manganita, braunita, rodonita, rodocrosita, hübnerita, etc. En los fondos marinos también se ha encontrado en nódulos de manganeso, en donde el contenido en manganeso oscila entre un 15 y un 30%, y en donde sería posible extraerlo.
Los países con mayores yacimientos de minerales de manganeso son Sudáfrica, Ucrania, Bolivia y China.
El metal se obtiene por reducción de los óxidos con aluminio, y el ferromanganeso se obtiene también reduciendo los óxidos de hierro y manganeso con carbono.
Aplicaciones
- El traqueteo de los motores se reduce mediante el uso de un compuesto de manganeso que se añade a la gasolina sin plomo. Esto aumenta el octanaje del combustible.
- El manganeso se utiliza en las baterías desechables estándar.
- El manganeso es esencial para producir el acero y el hierro. El manganeso es un componente esencial para la fabricación de acero inoxidable de bajo costo.
- El manganeso es aleado con aluminio para producir una aleación que es más resistente a la corrosión. La mayoría de las latas de aluminio para bebidas contienen entre el 0,8 % y el 1,5 % de manganeso.
- En química, el óxido de manganeso se utiliza para oxidar el alcohol bencílico.
- La contaminación de hierro puede hacer que el vidrio se tinte de color verde. Ya desde tiempos antiguos se añade un compuesto de manganeso al vidrio para contrarrestar este efecto.
- El dioxígeno y el dicloro se procesan utilizando dióxido de manganeso. Este mismo compuesto es también un pigmento marrón que se puede utilizar para fabricar pinturas.
- El vidrio y la cerámica se pueden colorear mediante diversos compuestos de manganeso.
- En algunas partes del mundo, el manganeso se utiliza para fabricar monedas.
Información general
Nombre: Manganeso
Símbolo: Mn
Número: 25
Serie Química: Metales de Transición
Grupo: 7
Período: 4
Bloque: d
Masa Atómica: 54.938049 u
Configuración Electrónica: [Ar]3d54s2
Electrones por Nivel: 2,8,13,2
Propiedades Atómicas
Radio Medio: 140 pm
Electronegatividad: 1.55
Radio Atómico (calc): 161 pm
Radio Covalente: 139 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7430 kg/m3
Punto de fusión: 1519 K
Punto de ebullición: 2334 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7439-96-5
N° EINECS: 231-105-1
Velocidad del Sonido: 5150 m/s
Hierro
El hierro o fierro es un elemento químico de número atómico 26 situado en el grupo 8, periodo 4 de la tabla periódica de los elementos. Su símbolo es Fe (del latín fĕrrum) y tiene una masa atómica de 55,847 u.
Este metal de transición es el cuarto elemento más abundante en la corteza terrestre, representando un 5 % y, entre los metales, solo el aluminio es más abundante, y es el primero más abundante en masa planetaria, debido a que el planeta, en su núcleo, concentra la mayor masa de hierro nativo, equivalente a un 70 %. El núcleo de la Tierra está formado principalmente por hierro y níquel en forma metálica, generando al moverse un campo magnético. Ha sido históricamente muy importante, y un período de la historia recibe el nombre de Edad de Hierro. En cosmología, es un metal muy especial, pues es el metal más pesado que puede ser producido por la fusión en el núcleo de estrellas masivas; los elementos más pesados que el hierro solo pueden crearse en supernovas.
Historia
Se tienen indicios de uso del hierro desde el cuarto milenio antes de Cristo, por parte de los sumerios y egipcios.
En el segundo y tercer milenio antes de Cristo, van apareciendo cada vez más objetos de hierro (que se distingue del hierro procedente de meteoritos por la ausencia de níquel) en Mesopotamia, Anatolia y Egipto. Sin embargo, su uso parece ser ceremonial, siendo un metal muy caro, más que el oro. Algunas fuentes sugieren que tal vez se obtuviera como subproducto de la obtención de cobre.
Entre 1600 a. C. y 1200 a. C. va aumentando su uso en Oriente Medio, pero no sustituye al predominante uso del bronce.
Entre los siglos XII a. C. y X a. C. se produce una rápida transición en Oriente Medio desde las armas de bronce a las de hierro. Esta rápida transición tal vez fuera debida a la falta de estaño, antes que a una mejora en la tecnología en el trabajo del hierro. A este periodo, que se produjo en diferentes fechas según el lugar, se le denomina Edad de Hierro, sustituyendo a la Edad de Bronce. En Grecia comenzó a emplearse en torno al año 1000 a. C. y no llegó a Europa occidental hasta el siglo VII a. C. La sustitución del bronce por el hierro fue paulatina, pues era difícil fabricar piezas de hierro: localizar el mineral, luego fundirlo a temperaturas altas para finalmente forjarlo.
Hacia finales del siglo XVIII y comienzos del XIX se comenzó a emplear ampliamente el hierro como elemento estructural (en puentes, edificios, etc). Entre 1776 a 1779 se construye el primer puente de fundición de hierro, construido por John Wilkinson y Abraham Darby. En Inglaterra se emplea por primera vez en la construcción de edificios, por Mathew Boulton y James Watt, a principios del siglo XIX. También son conocidas otras obras de ese siglo, por ejemplo el Palacio de Cristal construido para la Exposición Universal de 1851 en Londres, del arquitecto Joseph Paxton, que tiene un armazón de hierro, o la Torre Eiffel, en París, construida en 1889 para la Exposición Universal, en donde se utilizaron miles de toneladas de hierro.
Abundancia en la naturaleza
El hierro es el metal de transición más abundante en la corteza terrestre, y cuarto de todos los elementos. También existe en el Universo, habiéndose encontrado meteoritos que lo contienen. Es el principal metal que compone el núcleo de la Tierra hasta con un 70%. Se encuentra formando parte de numerosos minerales, entre los que destacan la hematites, la magnetita, la limonita, la siderita, la pirita, la ilmenita, etcétera.
Se puede obtener hierro a partir de los óxidos con más o menos impurezas. Muchos de los minerales de hierro son óxidos, y los que no, se pueden oxidar para obtener los correspondientes óxidos.
Aplicaciones
El hierro es el metal duro más usado, con el 95% en peso de la producción mundial de metal. El hierro puro (pureza a partir de 99,5%) no tiene demasiadas aplicaciones, salvo excepciones para utilizar su potencial magnético. El hierro tiene su gran aplicación para formar los productos siderúrgicos, utilizando este como elemento matriz para alojar otros elementos aleantes tanto metálicos como no metálicos, que confieren distintas propiedades al material. Se considera que una aleación de hierro es acero si contiene menos de un 2,1% de carbono; si el porcentaje es mayor, recibe el nombre de fundición.
El acero es indispensable debido a su bajo precio y tenacidad, especialmente en automóviles, barcos y componentes estructurales de edificios.
Las aleaciones férreas presentan una gran variedad de propiedades mecánicas dependiendo de su composición o el tratamiento que se haya llevado a cabo.
Información general
Nombre: Hierro
Símbolo: Fe
Número: 26
Serie Química: Metales de Transición
Grupo: 8
Período: 4
Bloque: d
Masa Atómica: 55.847 u
Configuración Electrónica: [Ar]3d64s2
Electrones por Nivel: 2,8,14,12
Propiedades Atómicas
Radio Medio: 140 pm
Electronegatividad: 1.83
Radio Atómico (calc): 155.8 pm
Radio Covalente: 126 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7874 kg/m3
Punto de fusión: 1808 K
Punto de ebullición: 3023 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7439-89-6
N° EINECS: 231-096-4
Velocidad del Sonido: 4910 m/s
Cobalto
El cobalto (del alemán kobalt, voz derivada de kobolds, los "gnomos" que, según los mineros de Sajonia de la Edad Media, eran espíritus de la tierra que tenían embrujado el mineral, por lo que, aunque parecía mena de cobre, no producía este elemento con el tratamiento habitual) es un elemento químico de número atómico 27 y símbolo Co situado en el grupo 9 de la tabla periódica de los elementos.
Historia
Los compuestos de cobalto se han utilizado durante siglos para obtener un color azul intenso de vidrio, los esmaltes y cerámicas. Se ha detectado cobalto en esculturas egipcias y en joyas persas desde el tercer milenio aC, en las ruinas de Pompeya (destruida en el año 79 dC), y en China, en la dinastía Tang (618-907 dC) y la dinastía Ming (1368-1644 dC).
El cobalto se ha empleado para colorear el vidrio desde la Edad del Bronce. La excavación del naufragio Uluburun encontró un lingote de cristal azul, que fue confeccionado durante el siglo XIV AC.67 artículos de cristal azul de Egipto son de color con el cobre, el hierro o el cobalto. La más antigua de cobalto de color de cristal era de la época de la dinastía XVIII de Egipto (1550-1292 aC). Se desconoce el lugar donde se obtuvieron los compuestos de cobalto.
El elemento fue descubierto por el químico sueco George Brandt. La fecha del descubrimiento varía en las diversas fuentes entre 1730 y 1737. Mostrando que es un nuevo elemento hasta entonces desconocido diferente de bismuto y otros metales tradicionales, y decir que es un nuevo "semi-metal". Brandt fue capaz de demostrar que el cobalto era el responsable del color azul del vidrio que previamente se atribuía al bismuto. El cobalto se convirtió en el primer metal descubierto desde la época pre-histórica, en la que todos los metales conocidos (hierro, cobre, plata, oro, zinc, mercurio, estaño, plomo y bismuto) no tenían descubridores registrados.
Su nombre proviene del alemán kobalt de kobold, llamado así por los mineros por su color, toxicidad y los problemas que ocasionaba ya que al igual que el níquel contaminaba y degradaba los elementos que se deseaba extraer. Los primeros intentos de fundición de estas menas para obtener metales como el cobre o el níquel, fracasaban dando en su lugar simplemente un polvo. Además, debido a que los minerales primarios de cobalto siempre contienen arsénico, la fundición de estas menas oxidaba el contenido de arsénico para dar el altamente tóxico y volátil, óxido de arsénico, lo que también disminuye el aprecio de estas menas para los mineros.
Abundancia en la naturaleza
En 2005, los depósitos de cobre en la provincia de Katanga (antigua provincia de Shaba) de la República Democrática del Congo fueron el principal productor de cobalto con casi el 40% cuota mundial, según informa el Servicio Geológico Británico. La situación política en el Congo influye en el precio de cobalto de manera significativa.
Existen varios métodos para separar el cobalto del cobre y níquel. Dependen de la concentración de cobalto y la composición exacta del mineral utilizado. Una etapa de separación implica flotación por espuma, en el que los tensioactivos se unen a los diferentes componentes del mineral, dando lugar a un enriquecimiento de mena de cobalto. Tras el tostado se convierte la mena a sulfato de cobalto, mientras que el cobre y el hierro se oxida al óxido. La lixiviación con agua extrae el sulfato junto con los arseniatos. Los residuos están además lixiviado con ácido sulfúrico obteniéndose una solución de sulfato de cobre. El cobalto también puede ser lixiviado de la escoria de la fundición de cobre.
Aplicaciones
- Aleaciones entre las que cabe señalar superaleaciones usadas en turbinas de gas de aviación, aleaciones resistentes a la corrosión, aceros rápidos, y carburos cementados y herramientas de diamante. Herramientas de corte en procesos de fabricación para fresadoras.
- Imanes (Alnico, Fernico, Cunico, Cunife) y cintas magnéticas.
- Catálisis del petróleo e industria química.
- Recubrimientos metálicos por deposición electrolítica por su aspecto, dureza y resistencia a la oxidación.
- Secante para pinturas, barnices y tintas.
- Recubrimiento base de esmaltes vitrificados.
- Pigmentos (cobalto azul y cobalto verde).
- Electrodos de baterías eléctricas.
- Cables de acero de neumáticos.
Información general
Nombre: Cobalto
Símbolo: Co
Número: 27
Serie Química: Metales de Transición
Grupo: 9
Período: 4
Bloque: d
Masa Atómica: 58.9332 u
Configuración Electrónica: [Ar]3d74s2
Electrones por Nivel: 2,8,15,2
Propiedades Atómicas
Radio Medio: 135 pm
Electronegatividad: 1.88
Radio Atómico (calc): 152 pm
Radio Covalente: 126 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8900 kg/m3
Punto de fusión: 1768 K
Punto de ebullición: 3200 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-48-4
N° EINECS: 231-158-0
Velocidad del Sonido: 4720 m/s
Niquel
El níquel es un elemento químico cuyo número atómico es 28 y su símbolo es Ni, situado en el grupo 10 de la tabla periódica de los elementos.
Historia
El uso del níquel se remonta aproximadamente al siglo IV a. C., generalmente junto con el cobre, ya que aparece con frecuencia en los minerales de este metal. Bronces originarios de la actual Siria tienen contenidos de níquel superiores al 2%. Alrededor del año 190 a.C., durante los reinados de Euthydemus II, Agathocles y Pantaleon se utilizó en Bactriana para fabricar monedas una aleación de color blanco, semejante a la plata, formada por cobre con el 20% de níquel, semejante al cuproníquel actual. Manuscritos chinos sugieren que el «cobre blanco» se utilizaba en Oriente hacia 1700 al 1400 a. C.; sin embargo, la facilidad de confundir las menas de níquel con las de plata, y la existencia de otras aleaciones de color blanco induce a pensar que en realidad el uso del níquel fue muy posterior.
Los minerales que contienen níquel, como la niquelina, se han empleado para colorear el vidrio. En 1751 Axel Frederik Cronstedt, intentando extraer cobre de la niquelina, obtuvo un metal blanco que llamó níquel, ya que los mineros de Hartz atribuían al «viejo Nick» (el diablo) el que algunos minerales de cobre no se pudieran trabajar; y el metal responsable de ello resultó ser el descubierto por Cronstedt en la niquelina, o Kupfernickel, diablo del cobre, como se llama aún al mineral en idioma alemán.
Hoy en día es muy frecuente encontrarlo en las monedas de cualquier país, donde debido a su elevado coste se alea con cobre. Estas monedas suplantaron a las de plata alrededor de mediados del siglo XX, provocando en ocasiones confusión. Algunos ejemplos son los cinco céntimos de Estados Unidos o el disco interno de una moneda de un euro.
La primera moneda acuñada níquel puro fue la de 20 céntimos de Suiza, en 1881.
Abundancia en la naturaleza
El níquel aparece en forma de metal en los meteoritos junto con el hierro (formando las aleaciones kamacita y taenita). También se encuentra en el núcleo de la Tierra junto al hierro, iridio y osmio, formando con estos tres metales una aleación de estructura metálica.
Aplicaciones
Aproximadamente el 65 % del níquel consumido se emplea en la fabricación de acero inoxidable austenítico y otro 12 % en superaleaciones de níquel. El restante 23 % se reparte entre otras aleaciones, baterías recargables, catálisis, acuñación de moneda, recubrimientos metálicos y fundición.
Información general
Nombre: Níquel
Símbolo: Ni
Número: 28
Serie Química: Metales de Transición
Grupo: 10
Período: 4
Bloque: d
Masa Atómica: 58.6934 u
Configuración Electrónica: [Ar]4s23d8
Electrones por Nivel: 2,8,16,2
Propiedades Atómicas
Radio Medio: 135 pm
Electronegatividad: 1.91
Radio Atómico (calc): 149 pm
Radio Covalente: 121 pm
Radio de van der Waals: 163 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8908 kg/m3
Punto de fusión: 1728 K
Punto de ebullición: 2730 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-02-0
N° EINECS: 231-111-4
Velocidad del Sonido: 4970 m/s
Cobre
El cobre (del latín cuprum, y este del griego kypros, Chipre),5 cuyo símbolo es Cu, es el elemento químico de número atómico 29. Se trata de un metal de transición de color cobrizo, es decir, rojizo anaranjado de brillo metálico que, junto con la plata y el oro, forma parte de la llamada familia del cobre, se caracteriza por ser uno de los mejores conductores de electricidad (el segundo después de la plata). Gracias a su alta conductividad eléctrica, ductilidad y maleabilidad, se ha convertido en el material más utilizado para fabricar cables eléctricos y otros elementos eléctricos y componentes electrónicos.
El cobre forma parte de una cantidad muy elevada de aleaciones que generalmente presentan mejores propiedades mecánicas, aunque tienen una conductividad eléctrica menor. Las más importantes son conocidas con el nombre de bronces y latones. Por otra parte, el cobre es un metal duradero porque se puede reciclar un número casi ilimitado de veces sin que pierda sus propiedades mecánicas.
Historia
El cobre es uno de los pocos metales que pueden encontrarse en la naturaleza en forma de cobre nativo, es decir, sin combinar con otros elementos. Por ello fue uno de los primeros en ser utilizado por el ser humano. Los otros metales nativos son el oro, el platino, la plata y el hierro proveniente de meteoritos.
No se sabe cómo ni dónde surgió la idea de añadir estaño al cobre, produciendo el primer bronce. Se cree que fue un descubrimiento imprevisto, ya que el estaño es más blando que el cobre y, sin embargo, al añadirlo al cobre se obtenía un material más duro cuyos filos se conservaban más tiempo. El descubrimiento de esta nueva tecnología desencadenó el comienzo de la Edad del Bronce, fechado en torno a 3000 a. C. para Oriente Próximo, 2500 a. C. para Troya y el Danubio y 2000 a. C. para China. En el yacimiento de Bang Chian, en Tailandia, se han datado objetos de bronce anteriores al año 2000 a. C.18 Durante muchos siglos el bronce tuvo un papel protagonista y cobraron gran importancia los yacimientos de estaño, a menudo alejados de los grandes centros urbanos de aquella época.
El declive del bronce empezó hacia el 1000 a. C., cuando surgió en Oriente Próximo una nueva tecnología que posibilitó la producción de hierro metálico a partir de minerales férreos. Las armas de hierro fueron reemplazando a las de cobre en todo el espacio entre Europa y Oriente Medio. En zonas como China la Edad del Bronce se prolongó varios siglos más. Hubo también regiones del mundo donde nunca llegó a utilizarse el bronce. Por ejemplo, el África subsahariana pasó directamente de la piedra al hierro.
Sin embargo, el uso del cobre y el bronce no desapareció durante la Edad del Hierro. Reemplazados en el armamento, estos metales pasaron a ser utilizados esencialmente en la construcción y en objetos decorativos como estatuas. El latón, una aleación de cobre y zinc fue inventado hacia el 600 a. C. También hacia esta época se fabricaron las primeras monedas en el estado de Lidia, en la actual Turquía. Mientras que las monedas más valiosas se acuñaron en oro y plata, las de uso más cotidiano se hicieron de cobre y bronce.
La búsqueda de cobre y metales preciosos por el Mediterráneo condujo a los cartagineses a explotar el gran yacimiento de Río Tinto, en la actual provincia de Huelva. Tras las guerras púnicas los romanos se apoderaron de estas minas y las siguieron explotando hasta agotar todo el óxido de cobre. Debajo de él quedó una gran veta de sulfuro de cobre, el cual los romanos no sabían aprovechar eficazmente. A la caída del Imperio romano la mina había sido abandonada y solo fue reabierta cuando los andalusíes inventaron un proceso más eficaz para extraer el cobre del sulfuro.
Aplicaciones
Ya sea considerando la cantidad o el valor del metal empleado, el uso industrial del cobre es muy elevado. Es un material importante en multitud de actividades económicas y ha sido considerado un recurso estratégico en situaciones de conflicto.
Información general
Nombre: Cobre
Símbolo: Cu
Número: 29
Serie Química: Metales de Transición
Grupo: 11
Período: 4
Bloque: d
Masa Atómica: 63.546 u
Configuración Electrónica: [Ar]4d104s1
Electrones por Nivel: 2,8,18,1
Propiedades Atómicas
Radio Medio: 135 pm
Electronegatividad: 1.9
Radio Atómico (calc): 145 pm
Radio Covalente: 138 pm
Radio de van der Waals: 140 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8960 kg/m3
Punto de fusión: 1257.77 K
Punto de ebullición: 2835 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-50-8
N° EINECS: 231-159-6
Velocidad del Sonido: 3570 m/s
Zinc
El zinc (del alemán Zink), también escrito cinc, es un elemento químico esencial de número atómico 30 y símbolo Zn, situado en el grupo 12 de la tabla periódica de los elementos.
Historia
Las aleaciones de zinc se han utilizado durante siglos —piezas de latón datadas en 1000-1500 a. C. se han encontrado en Canaán y otros objetos con contenidos de hasta el 87% de zinc han aparecido en la antigua región de Transilvania— sin embargo, por su bajo punto de fusión y reactividad química el metal tiende a evaporarse por lo que la verdadera naturaleza del metal no fue comprendida por los antiguos.
Se sabe que la fabricación de latón era conocida por los romanos hacia 30 a. C. Plinio y Dioscórides describen la obtención de aurichalcum (latón) por el procedimiento de calentar en un crisol una mezcla de cadmia (calamina) con cobre; el latón obtenido posteriormente era fundido o forjado para fabricar objetos.
La fundición y extracción de zinc impuro se llevó a cabo hacia el año 1000 en la India —en la obra Rasarnava (c. 1200) de autor desconocido se describe el procedimiento— y posteriormente en China y a finales del siglo XIV los indios conocían ya la existencia del zinc como metal distinto de los siete conocidos en la Antigüedad, el octavo metal. En 1597 Andreas Libavius describe una «peculiar clase de estaño» que había sido preparada en la India y llegó a sus manos en pequeña cantidad a través de un amigo; de sus descripciones se deduce que se trataba del zinc aunque no llegó a reconocerlo como el metal procedente de la calamina.
Abundancia en la naturaleza
El zinc es el 23.º elemento más abundante en la corteza terrestre. Las menas más ricas contienen cerca de un 10% de hierro y entre el 40 y el 50% de zinc. Los minerales de los que se extrae son el sulfuro de zinc, conocido como esfalerita (y también como blenda, término que actualmente se considera obsoleto), la smithsonita (carbonato) y la hemimorfita, (silicato) , que reciben en conjunto el nombre industrial de "calaminas", y la franklinita, (óxido).
La producción del zinc comienza con la extracción del mineral, que puede realizarse tanto a cielo abierto como en yacimientos subterráneos. Los minerales extraídos se trituran con posterioridad y se someten a un proceso de flotación para obtener el concentrado.
Aplicaciones
La principal aplicación del zinc —cerca del 50% del consumo anual— es el galvanizado del acero para protegerlo de la corrosión, protección efectiva incluso cuando se agrieta el recubrimiento ya que el zinc actúa como ánodo de sacrificio. Otros usos son:
- Baterías de Zn-C usadas en la industria aeroespacial para misiles y cápsulas espaciales por su óptimo rendimiento por unidad de peso y baterías zinc-aire para computadoras portátiles.
- Piezas de fundición inyectada en la industria de automoción.
- Metalurgia de metales preciosos y eliminación de la plata del plomo.
- Utilizado en fabricación de pinturas al óleo, para fabricar el color blanco de zinc, utilizado para crear transparencias en la pintura.
- Aleaciones: latón, alpaca, cuproníquel-zinc, aluzinc, virenium, tombac, etc.
- Ánodos: utilizado como elemento de sacrificio para evitar la corrosión de otras partes metálicas en depósitos de agua, barcos, etc.
- El zinc también se usa para la galvanización y fabricación de láminas de construcción con tramado para evitar la sobre flexión, conocidas como acanaladas u onduladas, por ser un material de ínfima calidad su costo es bajo, lo cual implica que las láminas de dicho material se empleen en construcciones de viviendas improvisadas o criaderos de animales (llamadas ranchos o cobertizos).
Información general
Nombre: Zinc o Cinc
Símbolo: Zn
Número: 30
Serie Química: Metales de Transición
Grupo: 12
Período: 4
Bloque: d
Masa Atómica: 65.38 u
Configuración Electrónica: [Ar]4s23d10
Electrones por Nivel: 2,8,18,2
Propiedades Atómicas
Radio Medio: 135 pm
Electronegatividad: 1.6
Radio Atómico (calc): 142 pm
Radio Covalente: 131 pm
Radio de van der Waals: 139 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7140 kg/m3
Punto de fusión: 692.68 K
Punto de ebullición: 1180 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-66-6
N° EINECS: 231-175-3
Velocidad del Sonido: 3700 m/s
Galio
El galio es un metal blando, grisáceo en estado líquido y plateado brillante al solidificar, sólido deleznable a bajas temperaturas que funde a temperaturas cercanas a la del ambiente como, el cesio, mercurio y rubidio.
Historia
El galio (del latín Gallia, Francia) fue descubierto mediante espectroscopía por Lecoq de Boisbaudran en 1875 por su característico espectro (dos líneas ultravioletas) al examinar una blenda de zinc procedente de los Pirineos. Ese mismo año lo aisló por electrólisis del hidróxido en una solución de hidróxido potásico (KOH) y le dio el nombre de su país natal Gallia, y el suyo propio por un juego de palabras de los que gustaban a los científicos de finales del siglo XIX ya que gallus significa gallo, coq en francés como su nombre Lecoq.
Antes de su descubrimiento la mayoría de sus propiedades fueron predichas y descritas por Mendeleyev —que lo llamó eka-aluminio— basándose en la posición que debía ocupar el elemento en la tabla periódica.
Abundancia en la naturaleza
Se hallan trazas de este metal en minerales como la bauxita, carbón, diasporo, germanita y esfalerita y es subproducto en los procesos de obtención de varios metales.
Precauciones
Debido a la expansión al solidificar el líquido, no debe almacenarse en recipientes rígidos (metálicos o de vidrio) ni llenarse el recipiente totalmente con galio líquido, ya que podrían romperse con la expansión que presenta este metal.
Información general
Nombre: Galio
Símbolo: Ga
Número: 31
Serie Química: Metales del Bloque
Grupo: 13
Período: 4
Bloque: p
Masa Atómica: 69.723 u
Configuración Electrónica: [Ar]4s23d104p1
Electrones por Nivel: 2,8,18,3
Propiedades Atómicas
Radio Medio: 130 pm
Electronegatividad: 1.81
Radio Atómico (calc): 136 pm
Radio Covalente: 126 pm
Radio de van der Waals: 187 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 5904 kg/m3
Punto de fusión: 302.9146 K
Punto de ebullición: 2477 K
Varios
Estructura cristalina: Ortorrómbica
N° CAS: 7440-55-3
N° EINECS: 231-163-8
Velocidad del Sonido: 2740 m/s
Germanio
Es un semimetal, de color blanco grisáceo lustroso, quebradizo, que conserva el brillo a temperaturas ordinarias. Presenta la misma estructura cristalina que el diamante y resiste a los ácidos y álcalis.
Forma gran número de compuestos órganos metálicos y es un importante material semiconductor utilizado en transistores y foto detectores. A diferencia de la mayoría de semiconductores, el germanio tiene una pequeña banda prohibida (band gap) por lo que responde de forma eficaz a la radiación infrarroja y puede usarse en amplificadores de baja intensidad.
Historia
Las propiedades del germanio (del latín Germania, Alemania) fueron predichas en 1871 por Mendeleyev en función de su posición en la tabla periódica, elemento al que llamó eka-silicio. El alemán Clemens Winkler demostró en 1886 la existencia de este elemento, descubrimiento que sirvió para confirmar la validez de la tabla periódica, habida cuenta de las similitudes entre las propiedades predichas y las observadas.
Abundancia en la naturaleza
Se obtiene de yacimientos de plata, zinc y cobre. Los únicos minerales rentables para la extracción del germanio son la germanita (69% de Ge) y garnierita (7-8% de Ge); además está presente en el carbón, la argirodita y otros minerales. La mayor cantidad, en forma de óxido (GeO2), se obtiene como subproducto de la obtención del zinc o de procesos de combustión de carbón.
Aplicaciones
Las aplicaciones del germanio se ven limitadas por su elevado costo y en muchos casos se investiga su sustitución por materiales más económicos.
- Fibra óptica.
- Electrónica: radares y amplificadores de guitarras eléctricas usados para recrear sonidos de la primera época del rock and roll; aleaciones de Germanato de Silicio (SiGe) en circuitos integrados de alta velocidad. También se utilizan compuestos sandwich Si/Ge para aumentar la movilidad de los electrones en el silicio (streched silicon).
- Óptica de infrarrojos, en forma de metal, ya que es opaco en la zona de la luz visible, pero transparente en el infrarrojo, entre 2 y 25 micrómetros.3 Espectroscopios, sistemas de visión nocturna y otros equipos.
- Lentes, con alto índice de refracción, de ángulo ancho y para microscopios.
- En joyería se usa la aleación Au con 12% de germanio.
- Como elemento endurecedor del aluminio, magnesio y estaño.
- Quimioterapia.
- El tetracloruro de germanio es un ácido de Lewis y se usa como catalizador en la síntesis de polímeros (PET). Actualmente, este es su uso principal.
Información general
Nombre: Germanio
Símbolo: Ge
Número: 32
Serie Química: Metaloides
Grupo: 14
Período: 4
Bloque: p
Masa Atómica: 72.64 u
Configuración Electrónica: [Ar]3d104s24p2
Electrones por Nivel: 2,8,18,4
Propiedades Atómicas
Radio Medio: 125 pm
Electronegatividad: 2.01
Radio Atómico (calc): 125 pm
Radio Covalente: 122 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 5323 kg/m3
Punto de fusión: 1211.4 K
Punto de ebullición: 3093 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-56-4
N° EINECS: 231-164-3
Velocidad del Sonido: 5400 m/s
Arsénico
El arsénico es un elemento químico de la tabla periódica que pertenece al grupo de los metaloides, también llamados semimetales; se puede encontrar de diversas formas aunque raramente se encuentra en estado sólido.
Se conoce desde la antigüedad y se reconoce como extremadamente tóxico.
Historia
El arsénico (del griego άρσενιχόν, oropimente) se conoce desde tiempos remotos, lo mismo que algunos de sus compuestos, especialmente los sulfuros.
El primero que lo estudió con detalle fue Brandt en 1633 y Schroeder lo obtuvo en 1649 por la acción del carbón sobre el ácido arsénico. A Berzeliuss se deben las primeras investigaciones acerca de la composición de los compuestos del arsénico.
En el siglo XVIII los arsenicales consiguieron un puesto de primer orden en la terapéutica hasta que fueron sustituidos por las sulfamidas y los antibióticos.
Abundancia en la naturaleza
Es el 52.º elemento en abundancia de la corteza terrestre con 2 ppm y es uno de los 22 elementos conocidos que se componen de un solo núcleo estable. El arsénico se encuentra en forma nativa y, principalmente, en forma de sulfuro en una gran variedad de minerales que contienen cobre, plomo, hierro, níquel, cobalto y otros metales.
Aplicaciones
- Preservante de la madera (arseniato de plomo y cromo), uso que representa, según algunas estimaciones, cerca del 70 % del consumo mundial de arsénico.
- El arseniuro de galio es un importante material semiconductor empleado en circuitos integrados más rápidos, y caros, que los de silicio. También se usa en la construcción de diodos láser y LED.
- Aditivo en aleaciones de plomo y latones.
- Insecticida, herbicidas y venenos: a principios del siglo XX se usaban compuestos inorgánicos pero su uso ha desaparecido prácticamente en beneficio de compuestos orgánicos. Sin embargo, esas aplicaciones están declinando.
- El disulfuro de arsénico se usa como pigmento y en pirotecnia.
- Decolorante en la fabricación del vidrio.
Información general
Nombre: Arsénico
Símbolo: As
Número: 33
Serie Química: Metaloides
Grupo: 15
Período: 4
Bloque: p
Masa Atómica: 74.92160 u
Configuración Electrónica: [Ar]4s23d104p3
Electrones por Nivel: 2,8,18,5
Propiedades Atómicas
Radio Medio: 115 pm
Electronegatividad: 2.0
Radio Atómico (calc): 139 pm
Radio Covalente: 119 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 5727 kg/m3
Punto de fusión: 887 K
Punto de ebullición: 1090 K
Varios
Estructura cristalina: Romboédrica
N° CAS: 7440-38-2
N° EINECS: 231-148-6
Selenio
El selenio se puede encontrar en varias formas alotrópicas. El selenio amorfo existe en tres formas, la vítrea, negra, obtenida al enfriar rápidamente el selenio líquido, funde a 180 °C y tiene una densidad de 4,28 g/cm³; la roja, coloidal, se obtiene en reacciones de reducción; el selenio gris cristalino de estructura hexagonal, la forma más común, funde a 220,5 °C y tiene una densidad de 4,81 g/cm³; y la forma roja, de estructura monoclínica, funde a 221 °C y tiene una densidad de 4,39 g/cm³.
Es insoluble en agua y alcohol, ligeramente soluble en disulfuro de carbono y soluble en éter.
Presenta el efecto fotoeléctrico, convirtiendo la luz en electricidad, y, además, su conductividad eléctrica aumenta al exponerlo a la luz. Por debajo de su punto de fusión es un material semiconductor tipo p, y se encuentra en su forma natural.
Historia
El selenio (del griego σελήνιον,"selénion", resplandor de la Luna y por selene o artemisa la diosa griega de la luna y los animales) fue descubierto en 1817 por Jöns Jacob Berzelius. Al visitar la fábrica de ácido sulfúrico de Gripsholm observó un líquido pardo rojizo que calentado al soplete desprendía un olor fétido que se consideraba entonces característico y exclusivo del telurio —de hecho su nombre deriva de su relación con este elemento ya que telurio proviene del latín Tellus, la Tierra— resultando de sus investigaciones el descubrimiento del selenio. Más tarde, el perfeccionamiento de las técnicas de análisis permitió detectar su presencia en distintos minerales pero siempre en cantidades extraordinariamente pequeñas.
Abundancia en la naturaleza
El selenio se encuentra muy distribuido en la corteza terrestre en la mayoría de las rocas y suelos se halla en concentraciones entre 0,1 y 2,0 ppm. Raramente se encuentra en estado nativo obteniéndose principalmente como subproducto de la refinación del cobre ya que aparece en los lodos de electrólisis junto al telurio (5-25 % Se, 2-10 % Te). La producción comercial se realiza por tostación con cenizas de sosa o ácido sulfúrico de los lodos.
Información general
Nombre: Selenio
Símbolo: Se
Número: 34
Serie Química: No Metales
Grupo: 16
Período: 4
Bloque: p
Masa Atómica: 78.26 u
Configuración Electrónica: [Ar]3d104s24p4
Electrones por Nivel: 2,8,18,6
Propiedades Atómicas
Radio Medio: 115 pm
Electronegatividad: 2.48
Radio Atómico (calc): 103 pm
Radio Covalente: 116 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 4790 kg/m3
Punto de fusión: 494 K
Punto de ebullición: 957.8 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7782-49-2
N° EINECS: 231-957-4
Velocidad del Sonido: 3350 m/s
Bromo
El bromo (también llamado antaño fuego líquido) es un elemento químico de número atómico 35 situado en el grupo de los halógenos (grupo VII A) de la tabla periódica de los elementos. Su símbolo es Br.1
El bromo a temperatura ambiente es un líquido rojo, volátil y denso. Su reactividad es intermedia entre el cloro y el yodo. En estado líquido es peligroso para el tejido humano y sus vapores irritan los ojos y la garganta.
Historia
El bromo fue descubierto en 1826 por Antoine-Jérôme Balard, pero no se produjo en cantidades importantes hasta 1860.
Abundancia en la naturaleza
La mayor parte del bromo se encuentra en el mar en forma de bromuro
Información general
Nombre: Bromo
Símbolo: Br
Número: 35
Serie Química: Halógenos
Grupo: 17
Período: 4
Bloque: p
Masa Atómica: 79.904 u
Configuración Electrónica: [Ar]4s23d104p5
Electrones por Nivel: 2,8,18,7
Propiedades Atómicas
Radio Medio: 115 pm
Electronegatividad: 2.96
Radio Atómico (calc): 94 pm
Radio Covalente: 114 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 3119 kg/m3
Punto de fusión: 265.8 K
Punto de ebullición: 332 K
Varios
Estructura cristalina: Ortorrómbica
N° CAS: 7726-95-6
N° EINECS: 231-778-1
Velocidad del Sonido: 206 m/s
Kryptón
El kriptón es un gas noble inodoro e insípido de poca reactividad caracterizado por un espectro de líneas verde y rojo-naranja muy brillantes. Es uno de los productos de la fisión nuclear del uranio. El kriptón sólido es blanco, de estructura cristalina cúbica centrada en las caras al igual que el resto de gases nobles.
Historia
Su nombre proviene del adjetivo griego κρυπτός kryptos cuyo significado es oculto. Fue descubierto en 1898 por los químicos británicos Sir William Ramsay y Morris W. Travers. Ramsay y Travers licuaron aire en el año 1898 y lo sometieron a un proceso de destilación fraccionada. Encontraron el kriptón en el residuo dejado por dicho aire líquido justo por encima de su punto de ebullición.
Aplicaciones
Hay muchas formas de usar el kriptón, sin embargo, la de mayor riesgo se presenta al ser usado en anestesia, ya que si no se aplica apropiadamente puede causar daños fatales.
Otros usos:
- En la fotografía.
- Las lámparas de flash (usadas para fotografía a alta velocidad).
- Los proyectores, en especial si son de alta definición.
- Y al estar expuestos en la fabricación automática de circuitos integrados.
Información general
Nombre: Kryptón
Símbolo: Kr
Número: 36
Serie Química: Gases Nobles
Grupo: 18
Período: 4
Bloque: p
Masa Atómica: 83.80 u
Configuración Electrónica: [Ar]3d104s24p6
Electrones por Nivel: 2,8,18,8
Propiedades Atómicas
Electronegatividad: 3
Radio Atómico (calc): 88 pm
Radio Covalente: 110 pm
Propiedades Físicas
Estado Ordinario: Gas no magnético
Densidad: 3708 kg/m3
Punto de fusión: 115.79 K
Punto de ebullición: 119.93 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7439-90-9
N° EINECS: 231-098-5
Velocidad del Sonido: 1120 m/s
Rubidio
El rubidio es un elemento químico de la tabla periódica cuyo símbolo es el Rb y su número atómico es 37.
Características principales
El rubidio es un metal alcalino blando, de color plateado blanco brillante que empaña rápidamente al aire, muy reactivo. Al igual que los demás elementos del grupo 1 puede arder espontáneamente en aire con llama de color violeta amarillento, reacciona violentamente con el agua desprendiendo hidrógeno y forma amalgama con mercurio. Puede formar aleaciones con oro,los demás metales alcalinos, y alcalinotérreos, antimonio y bismuto.
Al igual que los demás metales alcalinos presenta un único estado de oxidación (+1) y reacciona con dióxido de carbono, hidrógeno, nitrógeno, azufre y halógenos.
Su obtención tiene el lugar 16 dentro de los metales más abundantes en la corteza terrestre.
Aplicaciones
El rubidio se puede ionizar con facilidad por lo que se ha estudiado su uso en motores iónicos para naves espaciales, aunque xenón y cesio han demostrado una mayor eficacia para este propósito. Se utiliza principalmente en la fabricación de cristales especiales para sistemas de telecomunicaciones de fibra óptica y equipos de visión nocturna. Otros usos son:
- Recubrimientos fotoemisores de telurio-rubidio en células fotoeléctricas y detectores electrónicos.
- Afinador de vacío, getter, (sustancia que absorbe las últimas trazas de gas, especialmente oxígeno) en tubos de vacío para asegurar su correcto funcionamiento.
- Componente de fotorresistencias (o LDR, Light dependant resistors, resistencias dependientes de la luz), resistencias en las que la resistencia eléctrica varía con la iluminación recibida.
- En medicina para la tomografía por emisión de positrones, el tratamiento de la epilepsia y la separación por ultracentrifugado de ácido nucleicos y virus.
- Fluido de trabajo en turbinas de vapor.
- El RbAg4I5 tiene la mayor conductividad eléctrica conocida a temperatura ambiente de todos los cristales iónicos y podría usarse en la fabricación de baterías en forma de delgadas láminas entre otras aplicaciones eléctricas.
- Se estudia la posibilidad de emplear el metal en generadores termoeléctricos basados en la magnetohidrodinámica de forma que los iones de rubidio generados a alta temperatura sean conducidos a través de un campo magnético generando una corriente eléctrica.
- Sirve para conseguir el color púrpura en los fuegos artificiales.
En muchas aplicaciones puede sustituirse por el cesio (o el compuesto de cesio correspondiente) por su semejanza química.
Historia
El rubidio (del latín rubidus, rojo oscuro) fue descubierto en 1861 por Robert Bunsen y Gustav Kirchhoff en la lepidolita utilizando un espectroscopio al detectar las dos rayas rojas características del espectro de emisión de este elemento y que son la razón de su nombre. Son pocas las aplicaciones industriales de este elemento que en 1920 empezó a usarse en células fotoeléctricas habiéndose usado sobre todo en actividades de investigación y desarrollo, especialmente en aplicaciones químicas y electrónicas.
Abundancia y Obtención
A pesar de no ser un elemento muy abundante en la corteza terrestre ya que se encuentra entre los 56 elementos que engloban conjuntamente un 0,05% del peso de la misma, no puede considerarse escaso. Representando del orden de 78 ppm en peso, es el 23. elemento más abundante y el 16.º de los metales superando a otros metales comunes como el cobre, el plomo y el zinc de los que se extraen miles de toneladas anuales frente a las tres del rubidio. Es además 30 veces más abundante que el cesio y 4 que el litio metales de cuya obtención se extrae como subproducto. La razón de tal disparidad estriba en que no se conocen minerales en los que el rubidio sea el elemento predominante y que su radio iónico es muy similar al del potasio (2000 veces más abundante) sustituyéndole —en ínfimas cantidades— en sus especies minerales donde aparece como impureza.
Se encuentra en diversos minerales como leucita, polucita y zinnwaldita. La lepidolita contiene un 1,5% de rubidio (puede superar en ocasiones el 3,15%) y es de donde se obtiene el metal en su mayoría; también otros minerales de potasio y cloruro de potasio contienen cantidades significativas de rubidio como para permitir su extracción rentable, así como los depósitos de polucita (que pueden contener hasta un 1,35% de rubidio) entre los que destacan los del lago Bernic en Manitoba, (Canadá).
El metal se obtiene, entre otros métodos, reduciendo el cloruro de rubidio con calcio en vacío, o calentando su hidróxido con magnesio en corriente de hidrógeno. Pequeñas cantidades pueden obtenerse calentando sus compuestos con cloro mezclados con óxido de bario en vacío. La pureza del metal comercializado varía entre 99 y 99,8%.
Información general
Nombre: Rubidio
Símbolo: Rb
Número: 37
Serie Química: Metales Alcalinos
Grupo: 1
Período: 5
Bloque: s
Masa Atómica: 85,4678 u
Configuración Electrónica: [Kr]5s1
Dureza Mohs: 0, 3
Electrones por Nivel: 2, 8, 18, 8, 1
Estroncio
El estroncio es un metal blando de color plateado brillante, algo maleable, también alcalino térreo, que rápidamente se oxida en presencia de aire adquiriendo un tono amarillento por la formación de óxido, por lo que debe conservarse sumergido en parafina. Debido a su elevada reactividad el metal se encuentra en la naturaleza combinado con otros elementos formando compuestos. Reacciona rápidamente con el agua liberando hidrógeno molecular para formar el hidróxido de estroncio.
Historia
El estroncio fue identificado en las minas de plomo de Estroncia (Escocia), de donde procede su nombre, en 1790 por Adair Crawford en el mineral estroncianita distinguiéndolo de otros minerales de bario. En 1798 Klaproth y Hope lo descubrieron de forma independiente. El primero en aislar el estroncio fue Humphry Davy, en 1808, mediante electrólisis de la estronciana —óxido de estroncio— de donde proviene el nombre del metal.
Abundancia en la naturaleza
Según el Servicio Geológico Británico, China fue el principal productor de estroncio en el año 2007, con más de dos tercios de la producción mundial, seguido por España, México, Turquía, Argentina e Irán. El estroncio es un elemento abundante en la naturaleza representando una media del 0,034% de todas las rocas ígneas y se encuentra mayoritariamente en forma de sulfato y carbonato.
Aplicaciones
Hoy en día el uso más destacado del estroncio dentro de la ciencia es el de la construcción de los relojes atómicos más modernos y precisos que se conocen, superando por varios "ceros" a los relojes atómicos de Cesio hasta ahora usados. Hasta hace unos años también se utilizaba en cristales para tubos de rayos catódicos de televisores en color debido a la existencia de regulaciones legales que obligan a utilizar este metal para filtrar los rayos X evitando que incidan sobre el espectador.
- Pirotecnia (nitrato).
- Producción de imanes de ferrita
- Otros compuestos de estroncio se utilizan en la fabricación de cerámicas, productos de vidrio, pigmentos para pinturas, lámparas fluorescentes y medicamentos.
Información general
Nombre: Estroncio
Símbolo: Sr
Número: 38
Serie Química: Metales Alcalinotérreos
Grupo: 2
Período: 5
Bloque: s
Masa Atómica: 87.62 u
Configuración Electrónica: [Kr]5s2
Electrones por Nivel: 2,8,18,8,2
Propiedades Atómicas
Electronegatividad: 0.95
Radio Atómico (calc): 219 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 2630 kg/m3
Punto de fusión: 1050 K
Punto de ebullición: 1655 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-24-6
N° EINECS: 231-133-4
Itrio
Es un metal plateado de transición, común en los minerales de tierras raras. Dos de sus compuestos se utilizan para hacer el color rojo de los diodos luminiscentes o ledes, usados en los visualizadores (como los televisores en color de rayos catódicos o CRT).
Historia
Johan Gadolin, químico, físico y mineralogista finlandés, descubrió en 1794 el itrio en un mineral encontrado en Ytterby, una aldea de Suecia, cerca de Vaxholm. El itrio fue la primera tierra rara aislada con éxito en 1828 por Friedrich Wöhler, un químico alemán que trabajó con varios elementos, además del itrio. Al pasar el tiempo se sintetizaron más elementos a partir de los minerales obtenidos en las canteras de Ytterby, como el escandio y los metales lantánidos pesados como el terbio. Después de sintetizar el itrio, a partir del mismo mineral se sintetizaron otros elementos que también deben su nombre a dicha aldea de Suecia, el erbio, el terbio y el iterbio.
Abundancia en la naturaleza
Los metales raros pueden ser extraídos por medio de disolventes o a partir de métodos de intercambio iónico. El itrio comercial se obtiene por reducción del fluoruro con calcio en forma de óxido de itrio Y2O3, obteniéndolo de la gadolinita, que también contiene gadolinio, erbio, europio, holmio y renio. Este mineral se puede hallar en Groenlandia, Suecia, Japón, Noruega y Colorado. El itrio también puede encontrarse en el mineral nuevita, común en Colorado, que contiene titanio, tantalio, hierro y cuarzo, y es similar al keilhauite, que se puede encontrar en Noruega.
Aplicaciones
El itrio se utiliza comercialmente en la industria metálica para aleaciones.
Información general
Nombre: Itrio
Símbolo: Y
Número: 39
Serie Química: Metales de Transición
Grupo: 3
Período: 5
Bloque: d
Masa Atómica: 88.90585 u
Configuración Electrónica: [Kr]4d15s2
Electrones por Nivel: 2,8,18,9,2
Propiedades Atómicas
Radio Medio: 180 pm
Electronegatividad: 1.22
Radio Atómico (calc): 212 pm
Radio Covalente: 162 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 4472 kg/m3
Punto de fusión: 1799 K
Punto de ebullición: 3609 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-65-5
N° EINECS: 231-174-8
Velocidad del Sonido: 3300 m/s
Circonio
Es un metal de transición brillante, de color blanco grisáceo, duro, resistente a la corrosión, de apariencia similar al acero. Los minerales más importantes en los que se encuentra son el circón y la badeleyita, aunque debido al gran parecido entre el circonio y el hafnio (no hay otros elementos que se parezcan tanto entre sí) realmente estos minerales son mezclas de los dos; los procesos geológicos no han sido capaces de separarlos. Se utiliza sobre todo en reactores nucleares (por su baja sección de captura de neutrones). También se emplea como refractario y opacificador, y en pequeñas cantidades como agente de aleación por su fuerte resistencia a la corrosión.
Historia
El circonio (del persa zargun, que significa «color dorado») fue descubierto en 1789 por Martin Heinrich Klaproth a partir del circón, que era una piedra preciosa conocida desde la antigüedad. En 1824 Jons Jakov Berzelius lo aisló en estado impuro; hasta 1914 no se preparó el metal puro.
Abundancia en la naturaleza
No se encuentra en la naturaleza como metal nativo, lo que refleja su inestabilidad intrínseca con respecto al agua. Pero forma parte de numerosos minerales. En la corteza terrestre el circonio se encuentra presente en una concentración de aproximadamente 130 mg/kg y alrededor de 0.026 mg/L en el agua de mar. En abundancias ocupa el puesto 18, pero a pesar de ser muy común, por lo general solo se encuentra en cantidades muy pequeñas y cristales muy pequeños (típicamente 0,1 mm), por lo que en otros tiempos se consideró un elemento escaso.
Aplicaciones
- Principalmente (en torno a un 90 % del consumido) se utiliza, Generalmente aleado, zircaloy, en reactores nucleares, debido su resistencia a la corrosión y su muy baja sección de captura de neutrones. La sección de captura del hafnio es alta, por lo que es necesario separarlos para esta aplicación (para otras, no es necesario), generalmente mediante un proceso de extracción con dos disolventes no miscibles, o bien empleando resinas de intercambio iónico.
- Se utiliza como aditivo en aceros obteniéndose materiales muy resistentes. También se emplean aleaciones con níquel en la industria química por su resistencia frente a sustancias corrosivas, especialmente para válvulas, bombas , tuberías e intercambiadores de calor.
- El óxido de circonio impuro se emplea para fabricar crisoles de laboratorio (que soportan cambios bruscos de temperatura), recubrimiento de hornos y como material refractario en industrias cerámicas y de vidrio.
- Con fines militares se emplea como agente incendiario, como el cartucho aliento de dragón.
- Aleado con niobio presenta superconductividad a bajas temperaturas, por lo que se puede emplear para hacer imanes superconductores. Por otra parte, la aleación con cinc es magnética por debajo de los 35 K.
- El óxido de circonio se usa en joyería; es una gema artificial denominada circonita que imita al diamante.
- Se utiliza como aditivo para fabricar arenas sintéticas.
Información general
Nombre: Circonio
Símbolo: Zr
Número: 40
Serie Química: Metales de Transición
Grupo: 4
Período: 5
Masa Atómica: 91.224 u
Configuración Electrónica: [Kr]4d25s2
Electrones por Nivel: 2,8,18,10,2
Propiedades Atómicas
Radio Medio: 155 pm
Electronegatividad: 1.33
Radio Atómico (calc): 206 pm
Radio Covalente: 148 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 6501 kg/m3
Punto de fusión: 2128 K
Punto de ebullición: 4644 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-67-7
Velocidad del Sonido: 3800 m/s
Niobio
Es un metal de transición dúctil, gris, blando y poco abundante. Se encuentra en el mineral niobita, también llamado columbita, y se utiliza en aleaciones. Se emplea principalmente aleado en aceros, a los cuales confiere una alta resistencia.
Historia
El niobio tiene propiedades físicas y químicas similares a las del elemento tantalio, y los dos son, por lo tanto, difíciles de distinguir. El químico inglés Charles Hatchett informó de un nuevo elemento similar al tántalo en 1801 y lo llamó columbio. En 1809, el químico William Hyde Wollaston inglés concluyó erróneamente que el tántalo y el columbio eran idénticos. El químico alemán Heinrich Rose determinó en 1846 que los minerales de tántalo contenían un segundo elemento, que él nombró niobio. En 1864 y 1865, una serie de descubrimientos científicos clarificó que el niobio y el columbio eran el mismo elemento (a diferencia de tantalio), y desde hace un siglo se utilizaron ambos nombres indistintamente. El niobio fue adoptado oficialmente como el nombre del elemento en 1949, pero el nombre de columbio sigue siendo de uso corriente en la metalurgia en los Estados Unidos.
Abundancia en la naturaleza
La mina más grande de niobio en el mundo se encuentra en Araxá, Minas Gerais, Brasil, propiedad del también productor más grande de Ferroniobio (FeNb) en el mundo, así como de otros productos derivados del niobio.
Blomstrand lo preparó por primera vez en 1864 por reducción: calentando el cloruro en atmósfera de hidrógeno. Hasta 1905 no se obtuvo puro. Nunca se encuentra en estado elemental y casi siempre aparece acompañado de tántalo.
Aplicaciones
- Producción de acero
- Imanes superconductores
- Aceleradores de partículas
- Lentes y pantallas de cristal
- Lámparas de vapor de sodio
- JoyeríaMonedas
Información general
Nombre:Niobio
Símbolo: Nb
Número: 41
Serie Química: Metales de Transición
Grupo: 5
Período: 5
Bloque: d
Masa Atómica: 92.90638 u
Configuración Electrónica: [Kr]4d45s1
Electrones por Nivel: 2,8,18,12,1
Propiedades Atómicas
Radio Medio: 145 pm
Electronegatividad: 1.6
Radio Atómico (calc): 198 pm
Radio Covalente: 137 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8570 kg/m3
Punto de fusión: 2570 K
Punto de ebullición: 5017 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7440-03-1
N° EINECS: 231-113-5
Velocidad del Sonido: 3480 m/s
Molibdeno
Es un metal plateado, tiene el sexto punto de fusión más alto de cualquier elemento. El molibdeno no se produce como el metal libre en la naturaleza, sino en varios estados de oxidación en los minerales. Industrialmente, los compuestos de molibdeno se emplean en aplicaciones de alta presión y alta temperatura, como pigmentos y catalizadores.
Historia
El molibdeno no se encuentra libre en la naturaleza y los compuestos que se pueden encontrar fueron confundidos con otros compuestos de otros elementos (carbono o plomo) hasta el siglo XVIII. En 1778 Carl Wilhelm Scheele hizo reaccionar el mineral molibdenita con ácido nítrico obteniendo un compuesto con propiedades ácidas al que llamó "acidum molibdenae" (la palabra molibdeno proviene del griego "molybdos" que quiere decir "como el plomo", puesto que era confundido con este elemento). En 1782 Hjelm aisló el metal impuro mediante la reducción del anterior compuesto con carbono. El molibdeno se usó muy poco, y solo dentro del laboratorio, hasta finales del siglo XIX, cuando una empresa lo utilizó como agente aleante y observó las buenas propiedades de estas aleaciones con molibdeno.
Abundancia en la naturaleza
El molibdeno es el 54.º elemento más abundante en la corteza terrestre y el 25.º elemento más abundante en los océanos, con un promedio de 10 ppm.
La principal fuente de molibdeno es el mineral molibdenita (MoS2). También se puede encontrar en otros minerales, como la wulfenita y la powellita. El molibdeno se obtiene de la minería de sus minerales y como subproducto de la minería del cobre, siendo esta última el principal modo de explotación comercial; el molibdeno está presente en las minas en un rango de entre un 0.01 y un 0.5%. Aproximadamente la mitad de la producción mundial de molibdeno se localiza en Estados Unidos.
Aplicaciones
Aproximadamente las dos terceras partes del molibdeno consumido se emplean en aleaciones. El uso del molibdeno se remonta a la Primera Guerra Mundial, cuando hubo una fuerte demanda de wolframio, que lo hizo escasear, y se necesitaban aceros muy resistentes. El molibdeno se utiliza pues en aleaciones de alta resistencia y que soporten temperaturas y corrosiones sumamente altas. Estas aleaciones se usan en la construcción y en piezas de aviones y automóviles.
- El molibdeno se usa como catalizador en la industria petrolera. En concreto, es útil para la eliminación de azufre.
- Se emplea en distintos pigmentos (con un color anaranjado), para pinturas, tintes, plásticos y compuestos de caucho.
Información general
Nombre: Molibdeno
Símbolo: Mo
Número: 42
Serie Química: Metales de Transición
Grupo: 6
Período: 5
Bloque: d
Masa Atómica: 95.94 u
Configuración Electrónica: [Kr]4d55s1
Electrones por Nivel: 2,8,18,13,1
Propiedades Atómicas
Radio Medio: 145 pm
Electronegatividad: 2.16
Radio Atómico (calc): 190 pm
Radio Covalente: 154 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 10280 kg/m3
Punto de fusión: 2896 K
Punto de ebullición: 4912 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7439-98-7
N° EINECS: 231-107-2
Tecnecio
El tecnecio es el más ligero de los elementos químicos que no cuentan con isótopos estables y el primer elemento sintético que se encuentra en la tabla periódica. Las propiedades químicas de este metal de transición cristalino de color gris plateado son intermedias a las del renio y las del manganeso. se usa como fuente de partículas beta libre de la emisión de rayos gamma. El anión pertecnetato (TcO4-) se emplea como inhibidor de corrosión anódica para aceros.
Abundancia en la naturaleza
Puesto que el tecnecio es inestable, solo existen pequeñísimas trazas en la corteza terrestre originadas por la fisión espontánea del uranio.
Aplicaciones
- Medicina nuclear
- Uso industrial
- Uso químico
Información general
Nombre: Tecnecio
Símbolo: Tc
Número: 43
Serie Química: Metales de Transición
Grupo: 7
Período: 5
Bloque: d
Masa Atómica: 98.9063 u
Configuración Electrónica: [Kr]4d55s2
Electrones por Nivel: 2,8,18,14,1
Propiedades Atómicas
Radio Medio: 135 pm
Electronegatividad: 1.9
Radio Atómico (calc): 183 pm
Radio Covalente: 156 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 11500 kg/m3
Punto de fusión: 2430 K
Punto de ebullición: 4538 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-26-8
N° EINECS: 231-136-0
Rutenio
Es un metal de transición, poco abundante, del grupo del platino. Se encuentra normalmente en minas de platino y se emplea como catalizador en algunas aleaciones de platino.
Historia
El rutenio fue descubierto por Karl Ernst Claus en 1844. Observó que el óxido de platino contenía un nuevo metal y obtuvo seis gramos de rutenio de la parte de platino que es insoluble en agua regia.
Jöns Berzelius y Gottfried Osann casi lo descubrieron en 1827. Examinaron los residuos que quedaban al disolver una muestra de platino procedente de los Urales con agua regia. Osann pensó que había encontrado tres nuevos metales, a los que dio nombre, siendo uno de ellos el rutenio.
Abundancia en la naturaleza
Se encuentra en pocos minerales y no son comerciales; en la laurita, la anduoita, la platarsita, y en pequeñas cantidades en la pentlandita. Este elemento se encuentra generalmente junto con otros del grupo del platino, en los Urales y en América, formando aleaciones.
Los elementos del grupo del platino, que normalmente están juntos, se separan entre sí mediante una serie de procesos químicos, distintos según cómo se encuentren, aprovechando las diferencias químicas existentes entre cada elemento.
Aplicaciones
- Debido a su gran efectividad para endurecer al paladio y al platino, se emplea en las aleaciones de estos metales que se usan en contactos eléctricos con una alta resistencia al desgaste.
- Se incorpora al titanio como elemento de aleación para aumentar la resistencia a la corrosión. Un 0,1% la mejora en unas cien veces.
- Al igual que otros elementos del grupo del platino, se puede emplear como catalizador en distintos procesos.
Información general
Nombre: Rutenio
Símbolo: ru
Número: 44
Serie Química: Metales de Transición
Grupo: 8
Período: 5
Bloque: d
Masa Atómica: 101.07 u
Configuración Electrónica: [Kr]4d75s1
Electrones por Nivel: 2,8,18,15,1
Propiedades Atómicas
Radio Medio: 130 pm
Electronegatividad: 2.2
Radio Atómico (calc): 178 pm
Radio Covalente: 126 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 12370 kg/m3
Punto de fusión: 2607 K
Punto de ebullición: 4423 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-18-8
N° EINECS: 231-127-1
Velocidad del Sonido: 5970 m/s
Rodio
Es un metal de transición, poco abundante, del grupo del platino. Se encuentra normalmente en minas de platino y se emplea como catalizador en algunas aleaciones de platino.
Abundancia en la naturaleza
No existen minas de Rodio: es un subsidiario de otras actividades mineras. En Sudáfrica, donde es subproducto del platino, se concentra el 80% de la producción. En Rusia, segundo productor, se lo obtiene como subproducto del níquel.2.
Se lo considera el metal más caro del mundo.
Aplicaciones
Típicamente, el oro blanco es galvanizado con una capa externa de rodio de 0,05 a 0,5 μm de espesor. Por el espesor tan reducido, los rayones en esta capa pueden permitir la oxidación y esto debilitará aún más la capa de rodio. Lo ideal sería una capa de 2.0 μm para que dure más tiempo. Una joya de oro blanco con rodio puede ser enchapada de nuevo en algunas joyerías.
Otro uso del Rodio es actuar como catalizador para la hidrogenación y es activo en la reformación catalítica de hidrocarburos.
El rodio se emplea también en aplicaciones para contactos eléctricos. Es galvanizado fácilmente para formar superficies duras, resistentes al desgaste y de brillo permanente, utilizadas tanto en contactos eléctricos estacionarios como corredizos, en espejos y reflectores, y como acabado en joyería.
Información general
Nombre: Rodio
Símbolo: Rh
Número: 45
Serie Química: Metales de Transición
Grupo: 9
Período: 5
Bloque: d
Masa Atómica: 102.90550 u
Configuración Electrónica: [Kr]5s14d8
Electrones por Nivel: 2,8,18,16,1
Propiedades Atómicas
Electronegatividad: 2.28
Radio Atómico (calc): 134 pm
Radio Covalente: 142 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 12450 kg/m3
Punto de fusión: 2237 K
Punto de ebullición: 3968 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-16-6
Velocidad del Sonido: 4700 m/s
Paladio
Es un metal de transición del grupo del platino, blando, dúctil, maleable y poco abundante. Se parece químicamente al platino y se extrae de algunas minas de cobre y níquel. Se emplea principalmente como catalizador y en joyería.
Historia
El paladio, como el resto de los elementos del grupo del platino, ha sido usado desde la antigüedad, pues se tiene constancia de que los antiguos egipcios y las civilizaciones precolombinas ya lo valoraban como metal precioso. Los conquistadores del Nuevo Mundo redescubrieron el mineral de platino en el siglo XVII, en la búsqueda de oro.
El descubrimiento científico del paladio lo debemos a William Hyde Wollaston, que consiguió aislarlo en 1803 y le puso un nombre basado en el asteroide Palas, descubierto dos meses antes. Wollaston disolvió mineral de platino en agua regia y neutralizó con hidróxido de sodio. Tras lograr la precipitación del platino con cloruro de amonio, añadió cianuro de mercurio, que forma el compuesto cianuro de paladio. Al calentar este último se obtiene paladio en estado metálico. Este método es la base de la obtención moderna del paladio.
Abundancia en la naturaleza
Rusia es el principal productor de paladio, con al menos el 50 por ciento de participación mundial, seguido por Sudáfrica, Canadá y los Estados Unidos
Se puede encontrar como metal libre aleado con el oro y otros metales del grupo del platino en los depósitos de los montes Urales, Australia, Etiopía, Sudáfrica y América del Norte. Es comercialmente producido a partir de depósitos de níquel-cobre, que se encuentran en Sudáfrica, Ontario, y Siberia; Se necesita tratamiento de muchas toneladas métricas de mineral para extraer una sola onza de paladio. Sin embargo, la producción de la mina aún podía ser rentable, dependiendo de los precios del metal actual, como otros metales se producen juntos: níquel, cobre, platino y rodio. Es posible además obtenerlo en mínimas cantidades desde barros anódicos proveniente de la electrodeposición del cobre.
Aplicaciones
- Catálisis
- Electrónica
- Tecnología
- Almacenamiento de hidrógeno
- Fotografía
- Arte
- Joyería
Información general
Nombre: Paladio
Símbolo: Pd
Número: 46
Serie Química: Metales de Transición
Grupo: 10
Período: 5
Bloque: d
Masa Atómica: 106.42 u
Configuración Electrónica: [Kr]4d10
Electrones por Nivel: 2,8,18,18
Propiedades Atómicas
Radio Medio: 140 pm
Electronegatividad: 2.20
Radio Atómico (calc): 137 pm
Radio Covalente: 131 pm
Radio de van der Waals: 163 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 12023 kg/m3
Punto de fusión: 1828.05 K
Punto de ebullición: 3236 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-115-6
N° EINECS: 231-175-3
Velocidad del Sonido: 3070 m/s
Plata
Es un metal de transición de color plateado (blanco metálico), brillante, blando, dúctil y maleable.
Historia
La plata es uno de los siete metales conocidos desde la antigüedad. Se menciona en el libro del Génesis; y los montones de escoria hallados en Asia Menor e islas del mar Egeo, indican que el metal comenzó a separarse del plomo al menos cuatro milenios antes de nuestra era.
Abundancia en la naturaleza
La plata se encuentra nativa, combinada con azufre, arsénico, antimonio o cloro, formando un numeroso grupo de minerales de plata. El metal se obtiene principalmente de minas de cobre, cobre-níquel, oro, plomo y plomo-cinc de México, Canadá, el Perú y los EE. UU..
Aplicaciones
Aproximadamente el 70% de la producción mundial de plata se utiliza con fines industriales, y el 30%, con fines monetarios; buena parte de este metal se emplea en orfebrería, pero sus usos más importantes se dan en la industria fotográfica y química.
Información general
Nombre: Plata
Símbolo: Ag
Número: 47
Serie Química: Metales de Transición
Grupo: 11
Período: 5
Bloque: d
Masa Atómica: 107.8683 u
Configuración Electrónica: [Kr]5s14d10
Electrones por Nivel: 2,8,18,18,1
Propiedades Atómicas
Radio Medio: 160 pm
Electronegatividad: 1.93
Radio Atómico (calc): 165 pm
Radio Covalente: 153 pm
Radio de van der Waals: 172 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 10490 kg/m3
Punto de fusión: 1234.93 K
Punto de ebullición: 2435 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-22-4
N° EINECS: 231-131-3
Velocidad del Sonido: 2600 m/s
Cadmio
Es un metal pesado, blando, blanco azulado, relativamente poco abundante. Es uno de los metales más tóxicos. Normalmente se encuentra en minas de zinc y se emplea especialmente en pilas.
Historia
El cadmio (en latín, cadmia, y en griego kadmeia, que significa "calamina", el nombre que recibía antiguamente el carbonato de zinc) fue descubierto en Alemania en 1817 por Friedrich Strohmeyer. Lo encontró como impureza de algunas muestras de carbonato de zinc. Strohmeyer observó que esas muestras, en particular, cambiaban de color al calentarlas, lo cual no le ocurría al carbonato de zinc puro. Strohmeyer fue lo suficientemente persistente para continuar la observación consiguiendo aislar el elemento mediante el tueste y posterior reducción del sulfuro.
Abundancia en la naturaleza
Las concentraciones de cadmio en los diferentes compartimentos de la naturaleza son las siguientes:
- Agua: En ríos la concentración de cadmio disuelto es relativamente alta (10 -500 mg/l) encontrándose por lo general unido a materia participada. En zonas oceánicas abiertas la concentración está entre 0,5 y 10 mg/l; estos niveles puede ser superiores en áreas marinas cerradas, especialmente en las desembocaduras de los ríos que están contaminados.
- Aire: El transporte a los diferentes compartimentos ambientales se realiza a través del aire, donde tiene poca persistencia (días o semanas). Las concentraciones en zonas rurales son de 0,1 mg. por m³ aumentando hasta cinco veces en zonas urbanas e industriales.
- Suelo: El suelo es el primero en ser objeto de inmisión del cadmio, por la caída de partículas difundidas en el aire por actividades industriales, actividades antropogénicas o por su acumulación después de los incendios. En suelos la concentración media de cadmio es de 0,06 a 0,5 mg. por kg. aumentando hasta cien veces en zonas contaminadas. Hay estudios basados en que con la aplicación de fertilizantes procedentes de rocas fosfatadas aumenta la concentración desde 0,3 a 38 g. por hectárea y año. La persistencia del cadmio en suelos es de hasta trescientos años y el 90 por ciento permanece sin transformarse. Estas concentraciones de cadmio en el suelo dependen en su mayor parte del pH de la tierra, que controla la solubilidad y movilidad del metal.El zinc es el 23.º elemento más abundante en la corteza terrestre. Las menas más ricas contienen cerca de un 10% de hierro y entre el 40 y el 50% de zinc. Los minerales de los que se extrae son el sulfuro de zinc, conocido como esfalerita (y también como blenda, término que actualmente se considera obsoleto), la smithsonita (carbonato) y la hemimorfita, (silicato) , que reciben en conjunto el nombre industrial de "calaminas", y la franklinita, (óxido).
Aplicaciones
- Se emplea en acumuladores eléctricos de níquel-cadmio recargables.
- Es componente de aleaciones de bajo punto de fusión. Se emplea en aleaciones de cojinetes, con bajo coeficiente de fricción y gran resistencia a la fatiga.
- Se utiliza mucho en electrodeposición: recubrimiento de rectificadores y acumuladores.
- Utilizado en barras de control del flujo de neutrones en los reactores atómicos.
- El hidróxido de cadmio se emplea en galvanotecnia y en la fabricación de electrodos negativos de baterías de níquel-cadmio.
- El óxido de cadmio se usa como catalizador para la hidrogenación y la síntesis de metano. Además, se emplea para fabricación de esmaltes y en sinterización.
- El cloruro de cadmio se utiliza en galvanotecnia, fotografía y tintorería.
- El sulfuro de cadmio se utiliza como pigmento amarillo.
Información general
Nombre:Cadmio
Símbolo: Cd
Número: 48
Serie Química: Metales de Transición
Grupo: 12
Período: 5
Bloque: d
Masa Atómica: 112.411 u
Configuración Electrónica: [Kr]4d105s2
Electrones por Nivel: 2,8,18,18,2
Propiedades Atómicas
Radio Medio: 155 pm
Electronegatividad: 1.69
Radio Atómico (calc): 161 pm
Radio Covalente: 148 pm
Radio de van der Waals: 158 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8650 kg/m3
Punto de fusión: 594.22 K
Punto de ebullición: 1041 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-43-9
N° EINECS: 231-152-8
Velocidad del Sonido: 2310 m/s
Indio
Es un metal poco abundante, maleable, fácilmente fundible, químicamente similar al aluminio y al galio, pero más parecido al zinc (de hecho, la principal fuente de obtención de este metal es a partir de los minerales de zinc). Su principal aplicación está en las pantallas táctiles, en forma de óxido de indio y de estaño.
Historia
El indio (nombre procedente de la línea de color índigo de su espectro atómico) fue descubierto por Ferdinand Reich y Theodor Richter en 1863 cuando estaban investigando la presencia de talio en unas minerales de zinc mediante un espectrógrafo. Fue aislado por Ritcher en 1867.
Abundancia en la naturaleza
Se produce principalmente a partir de los residuos generados durante el procesado de minerales de zinc. También se encuentra en cantidades menores en algunos sulfuros de cobre, apareciendo en los residuos de su purificación por electrolisis.
Se estima que en la corteza terrestre hay unos 0,24 ppm de indio (aproximadamente tan abundante como la plata). El principal productor de indio es China, que produjo 300 toneladas en 2002. Se espera que el indio se acabe antes de 2050, por lo que, teniendo en cuenta la situación que existía en 2011, es de importancia la inversión en investigación de materiales sustitutos para producir electrodos transparentes y conductores para dispositivos táctiles, tales como los presentes en teléfonos móviles, tabletas o pantallas didácticas.
Aplicaciones
Se empleó principalmente durante la Segunda Guerra Mundial como recubrimiento en motores aeronáuticos de alto rendimiento. Después de esto se ha destinado a nuevas aplicaciones en aleaciones, en soldadura y en la industria electrónica.
A mediados y finales de los años 1980 despertó interés el uso de sulfuros de indio semiconductores y películas delgadas de óxido de indio y estaño para el desarrollo de pantallas de cristal líquido (LID). Esto es debido a que el uso del indio permitió la obtención del color azul en los LED, que se había resistido durante años.
Información general
Nombre: Indio
Símbolo: In
Número: 49
Serie Química: Metales del bloque p
Grupo: 13
Período: 5
Bloque: p
Masa Atómica: 114.818 u
Configuración Electrónica: [Kr]4d105s25p1
Electrones por Nivel: 2,8,18,18,3
Propiedades Atómicas
Radio Medio: 155 pm
Electronegatividad: 1.78
Radio Atómico (calc): 156 pm
Radio Covalente: 144 pm
Radio de van der Waals: 193 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7310 kg/m3
Punto de fusión: 429.75 K
Punto de ebullición: 2345 K
Varios
Estructura cristalina: Tetragonal
N° CAS: 7440-74-6
N° EINECS: 231-180-0
Velocidad del Sonido: 1215 m/s
Estaño
Es un metal normalmente blanco (o gris, gracias a una variante alotrópica que se discute a continuación). Es maleable, y se oxida de forma superficial a temperatura ambiente. Este efecto lo hace resistente a la corrosión mediante pasivación. Por tanto se utiliza para recubrir otros metales, protegiéndolos así de la corrosión. Se encuentra además en muchas aleaciones. Al doblar una barra de este metal se produce un sonido característico llamado grito del estaño, producido por la fricción de los cristales que la componen. Una de sus características más llamativas es que bajo determinadas condiciones térmicas sufre la peste del estaño. El estaño puro tiene dos variantes alotrópicas: el estaño gris, polvo no metálico, semiconductor, de estructura cúbica y estable a temperaturas inferiores a 13,2 °C, que es muy frágil y tiene un peso específico más bajo que el blanco; y el estaño blanco, el normal, metálico, conductor eléctrico, de estructura tetragonal y estable a temperaturas por encima de 13,2 °C.
Historia
El uso del estaño comenzó en el Cercano Oriente y los Balcanes alrededor del 2000 a. d.C., utilizándose en aleación con el cobre para producir un nuevo material, el bronce, dando así origen a la denominada Edad de Bronce. La importancia de la nueva aleación, con la que se fabricaban armas y herramientas más eficaces que las de piedra o de hueso habidas hasta entonces, originó durante toda la Antigüedad un intenso comercio a largas distancias con las zonas donde existían yacimientos de estaño.
Abundancia en la naturaleza
El estaño se obtiene del mineral casiterita donde se presenta como óxido (óxido de estaño (IV) o dióxido de estaño). Dicho mineral se muele y se enriquece en dióxido de estaño por flotación, después se tuesta y se calienta con coque en un horno de reverbero con lo cual se obtiene el metal.
Aplicaciones
- Se usa como protector del hierro, del acero y de diversos metales usados en la fabricación de latas de conserva.
- También se usa para disminuir la fragilidad del vidrio.
- Los compuestos de estaño se usan para fungicidas, tintes, dentífricos y pigmentos.
- Se usa para realizar bronce, aleación de estaño y cobre.
- Se usa para la soldadura blanda, aleado con plomo.
- Se usa en aleación con plomo para fabricar la lámina de los tubos de los órganos musicales.
- Tiene utilidad en etiquetas.
Información general
Nombre: Estaño
Símbolo: Sn
Número: 50
Serie Química: Metales del bloque p
Grupo: 14
Período: 5
Bloque: p
Masa Atómica: 118.710 u
Configuración Electrónica: [Kr]4d105s25p2
Electrones por Nivel: 2,8,18,18,4
Propiedades Atómicas
Radio Medio: 145 pm
Electronegatividad: 1.96
Radio Atómico (calc): 145 pm
Radio Covalente: 180 pm
Radio de van der Waals: 217 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7365 kg/m3
Punto de fusión: 505.08 K
Punto de ebullición: 2875 K
Varios
Estructura cristalina: Tetragonal
N° CAS: 7440-31-5
N° EINECS: 231-141-8
Velocidad del Sonido: 2500 m/s
Antimonio
El antimonio en su forma elemental es un sólido cristalino, fundible, quebradizo, blanco plateado que presenta una conductividad eléctrica y térmica baja y se evapora a bajas temperaturas. Este elemento semimetálico se parece a los metales en su aspecto y propiedades físicas, pero se comportan químicamente como un no metal. También puede ser atacado por ácidos oxidantes y halógenos.
Historia
Estudios arqueológicos e históricos indican que el antimonio y sus sulfuros han sido usados por los humanos al menos durante los últimos 6 milenios. En la antigüedad la antimonita o estibina, la forma más común de sulfuro de antimonio fue el principal ingrediente del “kohl”, una pasta negra usada por los egipcios, entre otros, como maquillaje para los ojos. Los babilonios conocían la forma de obtener antimonio de sus compuestos y lo usaban como ornamento para vasijas.
Abundancia en la naturaleza
Las estimaciones sobre la abundancia de antimonio en la corteza terrestre van desde 0,2 a 0,5 ppm. El antimonio es calcófilo, presentándose con azufre y con otros elementos como plomo, cobre y plata.
Aplicaciones
El antimonio tiene una creciente importancia en la industria de semiconductores en la producción de diodos, detectores infrarrojos y dispositivos de efecto Hall. Usado en aleaciones, este semimetal incrementa mucho la dureza y resistencia a esfuerzos mecánicos de la aleación. También se emplea en distintas aleaciones como peltre, metal antifricción (aleado con estaño), metal inglés (formado por zinc y antimonio), etc. Algunas aplicaciones más específicas:
- Baterías y acumuladores
- Tipos de imprenta
- Recubrimiento de cables
- Cojinetes y rodamientos
Información general
Nombre: Antimonio
Símbolo: Sb
Número: 51
Serie Química: Metaloides
Grupo: 15
Período: 5
Bloque: p
Masa Atómica: 121.760 u
Configuración Electrónica: [Kr]4d105s25p3
Electrones por Nivel: 2,8,18,18,5
Propiedades Atómicas
Radio Medio: 145 pm
Electronegatividad: 2.05
Radio Atómico (calc): 133 pm
Radio Covalente: 138 pm
Radio de van der Waals: 206 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 6697 kg/m3
Punto de fusión: 903.78 K
Punto de ebullición: 1860 K
Varios
Estructura cristalina: Romboédrica
N° CAS: 7440-36-0
N° EINECS: 231-146-5
Telurio
El telurio es un elemento relativamente estable, insoluble en agua y ácido clorhídrico, pero soluble en ácido nítrico y en agua regia. Es un semimetal que se encuentra en el grupo 16 y el periodo 5 de la Tabla periódica de los elementos.
Historia
Fue descubierto en 1782 en minerales de oro por Franz-Joseph Müller von Reichenstein, inspector jefe de minas en Transilvania (Rumanía), denominándolo metallum problematicum. En principio se confundió el telurio con el antimonio. Fue Martin Heinrich Klaproth, en 1798, quien examinó el «metal problemático» de Müller y lo llamó telurio.
Abundancia en la naturaleza
En abril de 2017 se publicó el hallazgo del mayor yacimiento de telurio del mundo, en aguas de las Islas Canarias (España), en los montes submarinos situados dentro de las aguas canarias llamadas "las abuelas de Canarias" (Drago, Bimbache, Ico, Pelicar, Malpaso, Tortuga e Infinito y Las Abuelas). Se calcula que el yacimiento tiene un total de unas 2670 toneladas de Telurio, unas 50 000 veces más que el hallazgo más grande encontrado hasta ahora.
Información general
Nombre: Telurio
Símbolo: Te
Número: 52
Serie Química: Metaloides
Grupo: 16
Período: 5
Bloque: p
Masa Atómica: 127.6 u
Configuración Electrónica: [Kr]4d105s25p41
Electrones por Nivel: 2,8,18,18,6
Propiedades Atómicas
Radio Medio: 140 pm
Electronegatividad: 2.1
Radio Atómico (calc): 123 pm
Radio Covalente: 135 pm
Radio de van der Waals: 206 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 6240 kg/m3
Punto de fusión: 722.66 K
Punto de ebullición: 1261 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 13494-80-9
N° EINECS: 236-813-4
Velocidad del Sonido: 2610 m/s
Yodo
Este elemento puede encontrarse en forma molecular como yodo diatómico. Es un oligoelemento y se emplea principalmente en medicina, fotografía y como colorante. Químicamente, el yodo es el halógeno menos reactivo y electronegativo.
Historia
El yodo fue descubierto en 1811 por el químico francés y el fabricante de salitre Bernard Courtois en las cenizas de algas marinas. Fue nombrado por Gay Lussac en una publicación del 1 de agosto de 1814,2 a partir del iodes del griego clásico (con reflejos violetas) debido al color de su vapor cuando se calienta.
Abundancia en la naturaleza
El yodo se presenta en la corteza terrestre con una concentración de 0,14 ppm, mientras que en el agua de mar su abundancia es de 0,052 ppm.
Información general
Nombre: Yodo
Símbolo: I
Número: 53
Serie Química: Halógenos
Grupo: 7
Período: 5
Bloque: p
Masa Atómica: 126.90447 u
Configuración Electrónica: [Kr]4d105s25p5
Electrones por Nivel: 2,8,18,18,7
Propiedades Atómicas
Radio Medio: 140 pm
Electronegatividad: 2.66
Radio Atómico (calc): 115 pm
Radio Covalente: 133 pm
Radio de van der Waals: 198 pm
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 4930 kg/m3
Punto de fusión: 386.85 K
Punto de ebullición: 457.4 K
Varios
Estructura cristalina: Ortorrómbica
N° CAS: 7553-56-2
N° EINECS: 231-442-4
Xenón
El xenón es un miembro de los elementos de valencia ocho llamados gases nobles o inertes. La palabra "inerte" ya no se usa para describir esta serie química, dado que algunos elementos de valencia cero forman compuestos. En un tubo lleno de gas xenón, se emite un brillo azul cuando se le excita con una descarga eléctrica. Se ha conseguido xenón metálico aplicándole presiones de varios cientos de kilobares. El xenón también puede formar clatratos con agua cuando sus átomos quedan atrapados en un entramado de moléculas de oxígeno.
Historia
El xenón (del griego ξενόν xenos que significa "extraño") fue descubierto por William Ramsay y Morris Travers en 1898 en los residuos obtenidos al evaporar los componentes del aire líquido.
Abundancia en la naturaleza
Se encuentra en trazas en la atmósfera terrestre, apareciendo en una parte por veinte millones. El elemento se obtiene comercialmente por extracción de los residuos del aire licuado. Este gas noble se encuentra naturalmente en los gases emitidos por algunos manantiales naturales. Los isótopos Xe-133 y Xe-135 se sintetizan Mediante irradiación de neutrones en reactores nucleares refrigerados por aire.
Aplicaciones
El Xenón fue identificado por primera vez como anestésico en 1951. Su uso no está aprobado en Estados Unidos, siendo poco probable que llegue a gozar de un uso más extendido debido a que es un gas raro que no puede fabricarse y que debe extraerse del aire, convirtiéndose en un medicamento bastante costoso. A pesar de ello, el xenón presenta características cercanas al de un gas anestésico virtualmente ideal, el cual puede utilizarse en situaciones críticas.
Es muy insoluble en sangre y en tejidos corporales, lo que permite una rápida inducción y posterior recuperación. Es lo suficientemente potente como para generar anestesia quirúrgica cuando se administra con 30% de oxígeno. Presenta efectos adversos mínimos.
Información general
Nombre: Xenón
Símbolo: Xe
Número: 54
Serie Química: Gases Nobles
Grupo: 18
Período: 5
Bloque: p
Masa Atómica: 131.293 u
Configuración Electrónica: [Kr]5s24d105p6
Electrones por Nivel: 2,8,18,18,8
Propiedades Atómicas
Electronegatividad: 2.6
Radio Atómico (calc): 108 pm
Radio Covalente: 130 pm
Radio de van der Waals: 216 pm
Propiedades Físicas
Estado Ordinario: Gas
Densidad: 5.9 kg/m3
Punto de fusión: 161.4 K
Punto de ebullición: 165.1 K
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-63-3
N° EINECS: 231-172-7
Velocidad del Sonido: 1090 m/s
Cesio
El cesio es el elemento químico con número atómico 55 y peso atómico de 132,905 uma. Su símbolo es Cs, y es el más pesado de los metales alcalinos en el grupo IA de la tabla periódica, a excepción del francio (hasta febrero de 2007); se encuentran en componentes no orgánicos.
Historia
El cesio fue descubierto por Robert Bunsen y por Gustav Kirchhoff en el año 1860 mediante el uso del espectroscopio, al encontrar dos líneas brillantes de color azul en el espectro del carbonato de cesio y del cloruro de cesio. Dichas sales de cesio fueron aisladas por Robert Bunsen, precipitándolas en el agua mineral. A pesar de los intentos infructuosos de Bunsen por aislar el elemento en su forma metálica, hubo que esperar hasta 1862 para que Carl Setterberg pudiera aislarlo mediante electrólisis del cianuro de cesio fundido.
Como apunte, en el año 1967 se establece en la conferencia de pesos y medidas en París que un segundo es igual a 9 192 631 770 períodos de radiación correspondiente a la transición entre los dos niveles hiperfinos del estado fundamental del isótopo 133 del átomo de cesio (133Cs), medidos a 0 K.
Características
El cesio es un metal blando, ligero y de bajo punto de fusión. Es el segundo menos electronegativo de todos los elementos después del francio. El cesio reacciona en forma vigorosa con oxígeno para formar una mezcla de óxidos. En aire húmedo, el calor de oxidación puede ser suficiente para fundir y prender el metal. El cesio no reacciona con nitrógeno para formar nitruros, pero reacciona con el hidrógeno a temperaturas altas para producir un hidruro muy estable; reacciona en forma violenta con el agua y aun con hielo a temperaturas de hasta -116 °C (-177 °F) así como con los halógenos, amoníaco y monóxido de carbono. En general, con compuestos orgánicos el cesio experimenta los mismos tipos de reacciones que el resto de los metales alcalinos, pero es mucho más reactivo.
Abundancia y Obtención
El cesio no es muy abundante en la corteza terrestre, hay solo 7 partes por millón. Al igual que el litio y el rubidio, el cesio se encuentra como un constituyente de minerales complejos, y no en forma de halogenuros relativamente puros, como en el caso del sodio y del potasio. Es hallado frecuentemente en minerales lepidolíticos como los existentes en Rodesia.
Usos
El cesio metálico se utiliza en celdas fotoeléctricas, instrumentos espectrográficos, contadores de centelleo, bulbos de radio, lámparas militares de señales infrarrojas y varios aparatos ópticos y de detección. Los compuestos de cesio se usan en la producción de vidrio y cerámica, como absorbentes en plantas de purificación de dióxido de carbono, en microquímica. Las sales de cesio se han utilizado en medicina como agentes antishock después de la administración de drogas de arsénico. El isótopo cesio-137 se utiliza habitualmente en procedimientos de radioterapia interna también llamada braquiterapia para el tratamiento del cáncer.
Referencias
1. Cesio. Joaquín Recio Miñarro, Químicaweb.
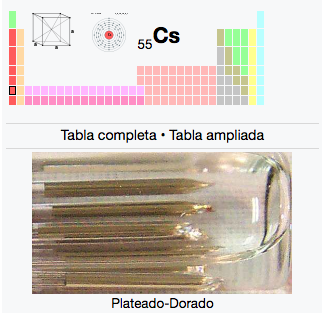
Información general
Nombre: Cesio
Símbolo: Cs
Número: 55
Serie Química: Metales Alcalinos
Grupo: 1
Período: 6
Bloque: s
Masa Atómica: 132,90545 u
Configuración Electrónica: [Xe]6s1
Dureza Mohs: 0, 2
Electrones por Nivel: 2, 8, 18, 18, 8, 1
Propiedades Atómicas
Radio medio: 260 pm
Electronegatividad: 0,79 (escala de Pauling)
Radio atómico (calc): 298 pm (radio de Bohr)
Radio covalente: 225 pm
Radio de van der Waals: 343 pm
Estado(s) de oxidación: 1
Óxido: base fuerte
1.ª Energía de ionización: 375,7 kJ/mol
2.ª Energía de ionización: 2234,3 kJ/mol
3.ª Energía de ionización: 3400 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 1879 kg/m3
Punto de fusión: 301,59 K (28 °C)
Punto de ebullición: 944 K (671 °C)
Entalpía de vaporización: 67,74 kJ/mol
Entalpía de fusión: 2,092 kJ/mol
Presión de vapor: 2,5 kPa
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N.º CAS: 7440-46-2
N.º EINECS: 231-155-4
Calor específico: 240 J/(K·kg)
Conductividad eléctrica: 4,89 × 106 S/m
Conductividad térmica: 35,9 W/(K·m)
Módulo elástico: 1,7 GPa
Módulo elástico: 1,6 GPa
Isótopos más estables
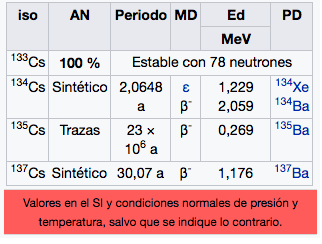
Francio
El francio, antiguamente conocido como eka-cesio y actinio K, es un elemento químico cuyo símbolo es Fr y su número atómico es 87. Su electronegatividad es la más baja conocida y es el segundo elemento menos abundante en la naturaleza (el primero es el astato). El francio es un metal alcalino altamente radiactivo y reactivo que se desintegra generando astato, radio y radón. Como el resto de los metales alcalinos, sólo posee un electrón en su capa de valencia.
Marguerite Perey descubrió este elemento en 1939. El francio fue el último elemento químico descubierto en la naturaleza antes de ser sintetizado. Fuera del laboratorio, el francio es extremadamente escaso, encontrándose en trazas en menas de uranio y de torio, donde el 223Fr está continuamente formándose y desintegrándose. La cantidad de 223Fr en la corteza terrestre en un momento dado posiblemente no exceda los 30 gramos; el resto de los isótopos son sintéticos. La mayor cantidad recuperada de cualquiera de sus isótopos fue un clúster de 10.000 millones de átomos (de 210Fr) sintetizado como un gas ultra frío en Stony Brook en 1996.
Propiedades Físicas y Químicas
El francio es menos estable que cualquier otro elemento más ligero que el nobelio (elemento 102); su isótopo más estable, el 223Fr, posee un período de semidesintegración menor de 22 minutos. El astato, que es el siguiente elemento menos estable, tiene período de semidesintegración máximo de 8,5 horas. Todos los isótopos del francio se desintegran generando astato, radio y radón.
El francio es un metal alcalino cuyas propiedades químicas son semejantes a las del cesio. Puesto que es un elemento muy pesado con un solo electrón de valencia, posee el mayor peso equivalente de todos los elementos químicos. El francio tiene la más baja electronegatividad de todos los elementos conocidos, con un valor de 0,7 en la escala de Pauling. Le sigue el cesio con un valor de 0,79. El francio líquido, en el supuesto de poder ser obtenido, tendría una tensión superficial de 0,05092 J·m–2 en el punto de fusión.
El francio coprecipita, junto con muchas sales de cesio, como el perclorato de cesio, formando pequeñas cantidades de perclorato de francio. Esta coprecipitación puede emplearse para aislar el francio, adaptando el método de precipitación del radiocesio de Glendenin y Nelson. También coprecipita con otras sales de cesio como el yodato, el picrato, el tartrato (también con el tartrato de rubidio), el cloroplatinato y el silicowolframato. Otras coprecipitaciones se producen con el ácido silicowolfrámico y con el ácido perclórico, sin necesidad de que otro metal alcalino esté presente como portador, lo que posibilita otros métodos de separación para el francio. Casi todas las sales de francio son solubles en agua.
Aplicaciones
No hay aplicaciones comerciales para el francio debido a su escasez y a su inestabilidad. Sólo ha sido usado en tareas de investigación, tanto en el campo de la biología como en el de la estructura atómica. Se pensó que el francio podría servir de ayuda para el diagnóstico de enfermedades relacionadas con el cáncer; sin embargo, finalmente esta aplicación se ha considerado impracticable.
La capacidad para sintetizar el francio, atraparlo y enfriarlo, junto con su estructura atómica relativamente simple, lo han convertido en sujeto de experimentación en espectroscopia especializada. Estos experimentos han conducido a la obtención de información más específica sobre los niveles energéticos y las constantes de acoplamiento entre partículas subatómicas. Estudios realizados sobre la luz emitida por iones de 210Fr atrapados por láser han arrojado datos precisos sobre las transiciones entre niveles energéticos atómicos. Se ha comprobado que estos resultados experimentales son bastante parecidos a los que predice la Teoría Cuántica.
Historia
Ya en 1870, los químicos pensaban que debía existir un metal alcalino más allá del cesio, con un número atómico de 87. Se le denominaba con el nombre provisional de eka-cesio. Algunos equipos de investigación intentaron localizar y aislar el elemento en cuestión y se tiene constancia de al menos cuatro anuncios públicos falsos que proclamaban haber descubierto dicho elemento antes de que fuera realmente descubierto.
Referencias
1. Price, Andy. «Francio». Consultado el 25 de marzo de 2007.
2. CRC Handbook of Chemistry and Physics. Volumen 4. Página 12. 2006. CRC. ISBN 0-8493-0474-1
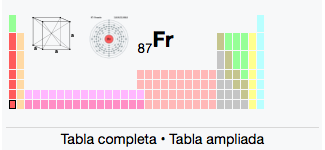
Información general
Nombre: Francio
Símbolo: Fr
Número: 87
Serie Química: Metales Alcalinos
Grupo: 1
Período: 7
Bloque: s
Masa Atómica: 223 u
Configuración Electrónica: [Rn]7s1
Dureza Mohs: -
Electrones por Nivel: 2, 8, 18, 32, 18, 8, 1
Propiedades Atómicas
Radio medio: Sin datos pm
Electronegatividad: 0,7 (Pauling) 0,9 (Allred y Rochow) (escala de Pauling)
Radio atómico (calc): 270 pm (radio de Bohr)
Radio iónico: 194 pm (Fr+, hexacoordinado)
Radio covalente: 260 pm
Radio de van der Waals: 348 pm
Estado(s) de oxidación: 1
Óxido: base fuerte
1.ª Energía de ionización: 380 kJ/mol
Propiedades Físicas
Estado ordinario: Líquido
Densidad: 1870 kg/m3
Punto de fusión: 300 K (27 °C)
Punto de ebullición: 950 K (677 °C)
Entalpía de vaporización: 65 kJ/mol
Entalpía de fusión: 2 kJ/mol
Presión de vapor: Sin datos
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
Calor específico: Sin datos J/(K·kg)
Conductividad eléctrica: 3 × 106/m O S/m
Conductividad térmica: 15 W/(K·m)
Velocidad del sonido: Sin datos m/s a 293,15 K (20 °C)
Isótopos más estables
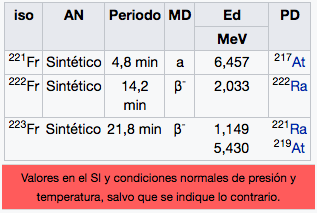
Bario
El bario es un elemento químico de la tabla periódica cuyo símbolo es Ba y su número atómico es 56. Metal alcalinotérreo, el bario es el 18.º elemento más común, ocupando una parte de 2000 de la corteza terrestre. Su masa atómica es 137,34. Su punto de fusión está a 725 °C, su punto de ebullición a 1.640 °C, y su densidad relativa es 3,5. Su principal mena es la baritina.
Propiedades químicas
Reacciona con el cobre y se oxida rápidamente en el agua. El elemento es tan reactivo que no existe en estado libre en la naturaleza, aunque también se presenta en forma de férricos o azufres no solubles en agua. Algunos de sus compuestos se consideran diamantes.
Características principales
El bario es un elemento metálico que es químicamente similar al calcio, pero más reactivo. Este metal se oxida con mucha facilidad cuando se expone al aire y es altamente reactivo con el agua o el alcohol, que produce gas hidrógeno. Se quema con el aire o el oxígeno, no sólo produce el óxido de bario (BaO), sino también el peróxido. Los compuestos de este elemento pesado se destacan por su alto peso específico. Este es el caso del mineral de bario más común, la barita (sulfato de bario, BaSO4), de elevada densidad (4,5 g/cm3).
Propiedades físicas
Punto de Ebullición: 1869,85 °C Punto de Fusión: 726,85 °C Densidad: 3,62 g/cm-3 Color: plateado. Olor: inodoro. Aspecto: sólido, frágil y blando. Cualquier sal de bario, expuesta al fuego del mechero de Bunsen (el más adecuado para este experimento), colorea la llama de un verde intenso, aún más que el del cobre. Se trata del tercer salto cuántico (precisamente el fenómeno de coloración del fuego) más bajo detrás del cesio y el rubidio.
Aplicaciones
- El bario se usa en pirotecnia, como muchos otros elementos de los grupos A.
- El bario metálico tiene pocas aplicaciones prácticas, aunque a veces se usa para recubrir conductores eléctricos en aparatos electrónicos y en sistemas de encendido de automóviles.
- El nitrato de bario se utiliza en fuegos artificiales, y el carbonato de bario en venenos para ratas (por medio de la ingesta).
- El sulfato de bario (BaSO4) se utiliza en conjunto con la lignina y el negro de humo como expansor para la fabricación de electrodos negativos de las baterías plomo-ácido, también se utiliza como material de relleno para los productos de caucho, en pintura y en el linóleo.
- También conocido como Barita o Baritina, debido a su alta densidad, se utiliza como lodo de perforación en los pozos de petróleo.
- Una forma de sulfato de bario, al ser opaca a los Rayos X, se usa como recubrimiento en las salas de rayos X o también diluida en agua como contraste radiológico para examinar estructuras por rayos X, especialmente en el sistema gastrointestinal.
- El óxido de bario (BaO) forma parte de las lentes de vidrio mineral de alta calidad, usadas, por ejemplo, en instrumentos ópticos.
Historia
Los alquimistas en la Edad Media ya conocían algunos minerales de bario. Guijarros del mineral barita, que se encuentran en Bolonia, Italia, se conocían como piedras de Bolonia. A los alquimistas les atraían porque después de su exposición a la luz, alumbraban durante años. Las propiedades fosforescentes de la barita calentada con compuestos orgánicos fueron descritas por V. Casciorolus en 1602.
Carl Scheele identificó que la barita (sulfato de bario) contenía un elemento nuevo en 1774, pero no pudo aislar el bario, solamente el óxido de bario. Johan Gottlieb Gahn también aisló el óxido de bario dos años más tarde en estudios similares. El bario oxidado fue en un principio llamado barota, por Guyton de Morveau, un nombre que fue cambiado por Antoine Lavoisier por el actual de baryta, que deriva del griego barys que significa «pesado», en atención a la gran densidad de muchos de sus compuestos. También en el siglo XVIII, el mineralogista inglés William Withering observó un mineral pesado en las minas de plomo de Cumberland, que ahora se sabe que era witerita. El bario fue aislado por vez primera mediante electrólisis de sales de bario fundidas en 1808, por sir Humphry Davy en Inglaterra.
Davy, por analogía con el calcio llamado barium por la barita, con el «-ium» final que significaba un elemento metálico. Robert Bunsen y Augustus Matthiessen obtuvieron bario puro por electrólisis a partir de una mezcla fundida de cloruro de bario y cloruro de amonio.
La producción de oxígeno puro en el proceso de Brin fue una aplicación a gran escala del peróxido de bario en la década de 1880, antes de ser reemplazado por la electrólisis y la destilación fraccionada del aire licuado a principios de los años 1900. En este proceso el óxido de bario reacciona a 700 C con el aire para formar peróxido de bario, que se descompone por encima de 500 C liberando oxígeno:
- 2 BaO + O2 ⇌ 2 BaO2
En 1908, el sulfato de bario se aplicó por primera vez como un agente de contraste radiológico en las imágenes de rayos X del sistema digestivo.
Referencias
1. Krebs, Robert E. (2006). The history and use of our earth's chemical elements: a reference guide. Greenwood Publishing Group. p. 80. ISBN 0-313-33438-2.
2. Kresse, Robert; Baudis, Ulrich; Jäger, Paul; Riechers, H. Hermann; Wagner, Heinz; Winkler, Jocher; Wolf, Hans Uwe (2007). «Barium and Barium Compounds». En Ullman, Franz, ed. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. doi:10.1002/14356007.a03_325.pub2.
Información general
Nombre: Bario
Símbolo: Ba
Número: 56
Serie Química: Metales alcalinotérreos
Grupo: 2
Período: 6
Bloque: s
Masa Atómica: 137,327 u
Configuración Electrónica: [Xe]6s2
Dureza Mohs: 1,25
Electrones por Nivel: 2, 8, 18, 18, 8, 2
Propiedades Atómicas
Radio Medio: 215 pm
Electronegatividad: 0,89 (escala de Pauling)
Radio Atómico (calc): 253 pm (radio de Bohr)
Radio Covalente: 198 pm
Estado(s) de oxidación: 2
Óxido: base fuerte
1.ª Energía de ionización: 502,9 kJ/mol
2.ª Energía de ionización: 965,2 kJ/mol
3.ª Energía de ionización: 3600 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido (paramagnético)
Densidad: 3620 kg/m3
Punto de fusión: 1000 K (727 °C)
Punto de ebullición: 2118 K (1845 °C)
Entalpía de vaporización: 142 kJ/mol
Entalpía de fusión: 7,75 kJ/mol
Presión de vapor: 98 Pa a 371 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7440-39-3
N° EINECS: 231-149-1
Calor Específico: 204 J/(K·kg)
Conductividad Eléctrica: 3·106 S/m
Conductividad Térmica: 18,4 W/(K·m)
Velocidad del Sonido: 1620 m/s a 293,15 K (20 °C)
Isótopos más estables
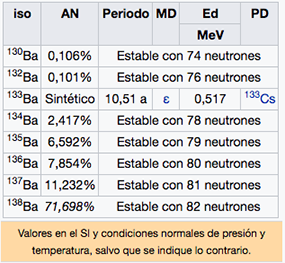
Radio
El radio es un elemento químico de la tabla periódica. Su símbolo es Ra y su número atómico es 88.
Es de color blanco inmaculado, pero se ennegrece con la exposición al aire. El radio es un alcalinotérreo que se encuentra a nivel de trazas en minas de uranio. Es extremadamente radiactivo, un millón de veces más que el uranio. Su isótopo más estable, Ra-226, tiene un periodo de semidesintegración de 1.602 años y se transmuta dando radón.
Características principales
El radio es el elemento más pesado de los metales alcalinotérreos, es intensamente radiactivo y se parece químicamente al bario. Los preparados de radio son destacables porque son capaces de mantenerse a más alta temperatura que su entorno y por sus radiaciones, que pueden ser de tres tipos: rayos alfa, rayos beta y rayos gamma. Además, el radio produce neutrones si se mezcla con berilio.
Cuando se prepara el metal radio puro es de color blanco brillante, pero se ennegrece cuando se expone al aire debido a la rápida oxidación del metal con el oxígeno. Es luminiscente (dando un color azul pálido), se corrompe en agua para dar hidróxido de radio y es ligeramente más volátil que el bario.
Aplicaciones
Radioisótopos descubiertos recientemente, como los de cobalto-60 y cesio-137, están reemplazando al radio, incluso en estos limitados usos, dado que son más potentes y más seguros de manipular. A nivel biológico se encuentra concentrado en los huesos y puede reemplazar al calcio. Como la exposición a la radiación de radio ocasiona la destrucción de tejidos malignos, este elemento es muy utilizado en terapias para detener el crecimiento del cáncer.
Otros usos son:
- Antiguamente se usaba en pinturas luminiscentes para relojes y otros instrumentos. Más de cien pintoras de esferas de reloj, que usaban sus labios para moldear el pincel, murieron a causa del envenenamiento por radiación. Años más tarde este caso daría notoriedad pública a los efectos adversos de la radiactividad. A finales de los sesenta aún se usaba el radio en las esferas de reloj. Los objetos pintados con estas pinturas son peligrosos y han de ser manipulados convenientemente. Hoy en día, se usan fosfatos con pigmentos que capturan la luz en vez de radio.
- Cuando se mezcla con berilio, es una fuente de neutrones para experimentos físicos.
- El cloruro de radio se usa en medicina para producir radón, que se usa en tratamientos contra el cáncer.
- Una unidad de radiactividad, el curio, está basada en la radiactividad del radio-226.
- El radio se empleaba a principios de siglo hasta los años 30 en medicinas, entre ellos el Radithor (agua destilada con radio), que lo describían como solución ante todos los males. También se mezclaba con pastas dentales, chicles, cremas y una infinidad de cosas más. Se brindaba con Radithor, y a menudo, este elemento se empleaba en los cristales, para darles una tonalidad verdosa brillante en la oscuridad. La razón de todo esto es que todo lo que contenía radio significaba avance.
Historia
El radio (del latín radius, rayo) fue descubierto en 1898 por Marie Skłodowska-Curie y su marido Pierre en una variedad de uraninita del norte de Bohemia. Mientras estudiaban el mineral, los Curie retiraron el uranio de él y encontraron que el material restante aún era radioactiva. Entonces produjeron una mezcla radioactiva hecha principalmente de bario que daba un color de llama rojo brillante y líneas espectrales que no se habían documentado anteriormente. En 1910 el radio fue aislado por Curie y Andre Debierne en su metal puro mediante la electrólisis de una solución de cloruro puro de radio usando un cátodo de mercurio y destilando en una atmósfera de hidrógeno.
Históricamente, los productos de desintegración del radio han sido conocidos como Radio A, B, C, etc. Hoy se sabe que son isótopos de otros elementos, del siguiente modo:
- Emanación del radio - radón-222
- Radio A - polonio-218
- Radio B - plomo-218
- Radio C - bismuto-218
- Radio C1 - polonio-214
- Radio C2 - talio-210
- Radio D - plomo-210
- Radio E - bismuto-210
- Radio F - polonio-210
El 4 de febrero de 1936 el Radio E fue el primer elemento radiactivo preparado sintéticamente.
Durante los años 1930 se descubrió que la exposición de los trabajadores a pinturas luminiscentes causaba serios daños a la salud como llagas, anemia o cáncer de huesos. Por eso posteriormente se frenó este uso del radio. Esto ocurre porque el radio es asimilado como calcio por el cuerpo y depositado en los huesos, donde la radiactividad degrada la médula ósea y puede hacer mutar a las células. Desde entonces se ha culpado a la manipulación del radio de la prematura muerte de Marie Curie.
Obtención
El radio es un producto de descomposición del uranio y por lo tanto se puede encontrar en todas las minas de uranio. Originalmente se obtenía de las minas de pechblenda de Joachimstal, Bohemia (con una concentración de unas siete partes por millón, siete gramos de radio por tonelada de pechblenda ). De las arenas de carnotita de Colorado se obtiene también este elemento, pero se han encontrado minas más ricas en la República Democrática del Congo (minas del Alto Katanga) y el área de los Grandes Lagos en Canadá, además de poder obtenerse de los residuos radiactivos de uranio. Hay grandes depósitos de uranio en Ontario, Nuevo México, Utah y Australia, entre otros lugares.
Referencias
1. Guide to the Elements - Revised Edition, Albert Stwertka, (Oxford University Press; 1998) ISBN 0-19-508083-1
2. Los Alamos National Laboratory - Radium.
Información general
Nombre: Radio
Símbolo: Ra
Número: 88
Serie Química: Metales alcalinotérreos
Grupo: 2
Período: 7
Bloque: s
Masa Atómica: (226,0254) u
Configuración Electrónica: [Rn]7s2
Dureza Mohs: 1,25
Electrones por Nivel: 2, 8, 18, 32, 8, 2
Propiedades Atómicas
Electronegatividad: 0,9 (escala de Pauling)
Radio Atómico (calc): 215 pm (radio de Bohr)
Radio Covalente: 221 ± 2 pm
Radio de van der Waals: 283 pm
Estado(s) de oxidación: 2 (base fuerte)
1.ª Energía de ionización: 509,3 kJ/mol
2.ª Energía de ionización: 979,0 kJ/mol
Propiedades Físicas
Estado Ordinario: sólido (no magnético)
Densidad: 5500 kg/m3
Punto de fusión: 973 K (700 °C)
Punto de ebullición: 2010 K (1737 °C)
Entalpía de fusión: 37 kJ/mol
Presión de vapor: 327
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7440-14-4
Calor Específico: 94 J/(K·kg)
Conductividad Térmica: 18,6 W/(K·m)
Isótopos más estables
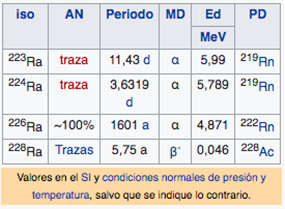
Lantano
El lantano es un elemento químico de la tabla periódica cuyo símbolo es La y su número atómico es 57.
Es el primer elemento de la serie de los lantánidos.
Historia
Fue descubierto por el químico sueco Carl Gustaf Mosander en el año 1839. Debe su nombre al verbo griego lanthaneîn (λανθανεῖν), que significa "escondido", ya que el metal se encontraba "escondido" en un mineral de cerio. Mosander descubrió el elemento lantano en el nitrato de cerio impuro. Se extrajo de la tierra (óxido insoluble en agua) lantana (óxido de lantano), tratándola con un ácido fuerte. (Otros elementos lantánidos fueron descubiertos en impurezas de minerales de itrio y de cerio).
Métodos de obtención y química
El lantano, como las otras tierras raras, existe solo en minerales a causa de su reactividad química.
Mediante reducción del fluoruro de lantano anhidro con calcio:
- 2 LaFO3 + 3Ca → 3CaF2 + 2La
Aplicaciones especiales
- Aleado con cerio, neodimio, praseodimio, gadolinio e iterbio forma la aleación llamada mischmetal, utilizada para fabricar piedras de encendedor.
- El óxido de lantano confiere al vidrio resistencia a las bases y se emplea para la fabricación de vidrios ópticos especiales.
- Se están produciendo esponjas de hidrógeno con aleaciones que contienen lantano. Dichas aleaciones admiten hasta 400 veces su volumen de gas y el proceso es reversible. Cada vez que toman gas se libera energía calorífica, por lo que tienen la posibilidad de convertirse en sistemas de conservación de energía.
- Es utilizado como componente de las pantallas intensificadoras de las unidades de rayos X.
- El carbonato de lantano es utilizado en el tratamiento de la insuficiencia Renal Crónica por su capacidad de formar complejos insolubles con fosfatos, reduciendo así la hiperfosfemia.
Efectos del lantano sobre la salud
El lantano resulta peligroso debido a que se puede inhalar con el aire. Este puede causar embolia de pulmón, especialmente en exposiciones de largo periodo. El lantano puede dañar al hígado cuando se acumula en el cuerpo humano.
Efectos ambientales del lantano
En animales acuáticos el lantano causa daño en las células de membranas, lo cual tiene bastante influencias negativas en la reproducción y las funciones del sistema nervioso.
Referencias
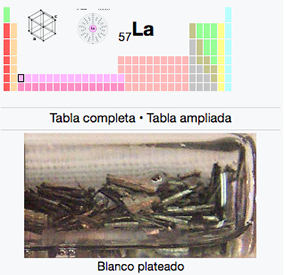
Información general
Nombre: Lantano
Símbolo: La
Número: 57
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: 138,9055 u
Configuración Electrónica: [Xe]5d16s2
Dureza Mohs: 2,5
Electrones por Nivel: 2, 8, 18, 18, 9, 2
Propiedades Atómicas
Radio Medio: 195 pm
Electronegatividad: 1,1 (escala de Pauling)
Radio Covalente: 169 pm
Estado(s) de oxidación: 3
Óxido: base fuerte
1.ª Energía de ionización: 509,3 kJ/mol
2.ª Energía de ionización: 1067 kJ/mol
3.ª Energía de ionización: 1850,3 kJ/mol
4.ª Energía de ionización: 4819 kJ/mol
Propiedades Físicas
Estado Ordinario: sólido
Densidad: 6146 kg/m3
Punto de fusión: 1193 K (920 °C)
Punto de ebullición: 3730 K (3457 °C)
Entalpía de vaporización: 414 kJ/mol
Entalpía de fusión: 6,2 kJ/mol
Presión de vapor: 1,33 × 10-7 Pa a 1193 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7439-91-0
N.º EINECS: 231-099-0
Calor Específico: 190 J/(K·kg)
Conductividad eléctrica: 1,26·106 S/m
Conductividad Térmica: 13,5 W/(K·m)
Velocidad del sonido: 2475 m/s a 293,15 K (20 °C)
Isótopos más estables
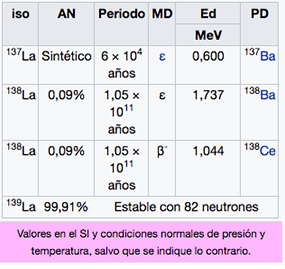
Actinio
El actinio (del griego ακτις, ακτινoς, rayo luminoso) es un elemento químico de símbolo Ac y número atómico 89, perteneciente al grupo IIIB, periodo 7 y bloque F de la tabla periódica de los elementos. Es una de las tierras raras y da nombre a una de las series, la de los actínidos. Es un metal radiactivo blando que reluce en la oscuridad. Se conocen los isótopos con número másico entre 209 y 234, siendo el más estable el 227Ac que tiene una vida media de 21,7 años. El 227Ac se encuentra en el uranio natural en una proporción del orden del 0,175% y el 228Ac también se encuentra en la naturaleza. Hay otros 22 isótopos artificiales del actinio, todos radiactivos y todos con vidas medias muy cortas. Descubierto por André-Louis Debierne en 1899, su principal aplicación es como fuente de partículas alfa.
Características principales
El actinio es un elemento metálico, radiactivo como todos los actínidos y de color plateado. Debido a su intensa radiactividad brilla en la oscuridad con una luz azulada. El isótopo 227Ac, que se encuentra sólo en trazas en los minerales de uranio, es un emisor de partículas α y β con un periodo de semidesintegración de 21,773 años. Una tonelada de mineral de uranio contiene cerca de 0,1 g de actinio. Su comportamiento químico es muy similar al del resto de las tierras raras y particularmente al del lantano, el elemento justo encima de él en la tabla periódica. El actinio es también similar al radio, el elemento que le precede. Sin embargo, el actinio no tiene electrones en el orbital 5f como el resto de los actínidos, sino que su configuración electrónica es 6d17s2. Su radio iónico, al encontrarse relacionado con un número de coordinación de 4, es 126.0 pm.
Historia
El actinio fue descubierto en 1899 por el químico francés André-Louis Debierne que lo obtuvo de la pechblenda, y lo caracterizó como una sustancia similar al titanio en 1899, y al torio en 1900. En 1902 fue descubierto, de forma independiente, por Friedrich Oscar Giesel como una sustancia muy similar al lantano, y lo denominó «emanium» en 1904. Luego de realizadas las comparaciones entre estas sustancias en 1904 se determinó que eran idénticas y el nombre propuesto por Debierne fue retenido debido a que tenía prioridad. Otros tres elementos fueron descubiertos entre 1898 y 1900: el polonio y el radio (por Marie y Pierre Curie) y el radón, un gas desprendido durante la desintegración radiactiva de algunos elementos más pesados descubierto en 1900 por el químico alemán Friedrich Ernst Dorn (1848–1916).
El descubrimiento de los isótopos radiactivos comenzó con la demostración en 1912–1913 que uno de los productos del actinio, denominado entonces actinio B, era químicamente idéntico al plomo. De la misma manera, otro producto del actinio, llamado actinio C, era químicamente idéntico al bismuto. Esos hallazgos llevaron a la conclusión de que algunos elementos contenían átomos que diferían en actividad química, aunque tuvieran el mismo número atómico: un radioisótopo.
Abundancia y obtención
Solo existe una corta lista de compuestos con actinio, por ejemplo AcF3, AcCl3, AcBr3, AcOF, AcOCl, AcOBr, Ac2S3, Ac2O3 y AcPO4. Todas esas moléculas tienen configuraciones muy similares a los compuestos correspondientes del lantano, por lo que se estima que en ellos el actinio ocurre con un número de oxidación de +3.
Se encuentran trazas de actinio (227Ac) en minerales de uranio, pero comúnmente se obtienen pequeñas cantidades (del orden de miligramos) bombardeando 226Ra con neutrones en un reactor nuclear seguido de una desintegración β- del isotopo 227Ra resultante.
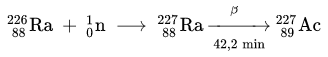
Los tiempos son de semivida.
Isótopos
Los isótopos radiactivos 227Ac son los únicos que se encuentran en la naturaleza y son los más estables de la treintena de isótopos identificados, con un periodo de semidesintegración de 21,773 años, seguido del 225Ac (10 días), 226Ac (29,37 horas) y el 228Ac (6,13 horas). El resto de isótopos tienen periodos de semidesintegración inferiores a las 10 horas y la mayoría de ellos menores de un minuto.
El 227Ac alcanza el equilibrio con sus productos de desintegración transcurridos 185 días, transmutándose posteriormente con arreglo a un periodo de semidesintegración de 21,773 años.
Aplicaciones
El uso del actinio es casi exclusivo para investigaciones científicas. La radiactividad del actinio es del orden de 150 veces la del radio, haciéndolo útil como fuente de neutrones; al margen de ello, no tiene aplicaciones industriales significativas.
El francio, elemento 87 de la tabla periódica, es un metal alcalino radiactivo caracterizado en 1939, el cual se obtiene en pequeñas cantidades como resultado de un decaimiento específico del 227Ac en la serie radiactiva que tiene inicio con el 235U.
Precauciones
El 227Ac es extremadamente radiactivo y, teniendo en cuenta sus potenciales efectos sobre la salud, es tan peligroso como el plutonio. La ingesta, incluso en pequeñas cantidades, puede causar daños muy graves.
Referencias
1. Vázquez, Domingo Agustín (2000). Diccionario de Ciencias. Editorial Complutense, Oxford. p. 14. ISBN 8489784809. Archivado desde el original el 15 de mayo de 2013.
2. Iupac.org.«Atomic Weights of the elements» (en inglés). Consultado el 23 de septiembre de 2007.
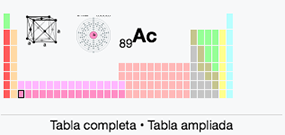
Información general
Nombre: Actinio
Símbolo: Ac
Número: 89
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 227 u
Configuración Electrónica: Rn 6d17s2
Electrones por Nivel: 2, 8, 18, 32, 18, 9, 2
Propiedades Atómicas
Radio Medio: 195 pm
Electronegatividad: 1,1 (escala de Pauling)
Estado(s) de oxidación: 3 (neutro)
1.ª Energía de ionización: 499 kJ/mol
2.ª Energía de ionización: 1170 kJ/mol
Propiedades Físicas
Estado Ordinario: sólido
Densidad: 10,070 kg/m3
Punto de fusión: 1323 K (1050 °C)
Punto de ebullición: 3471 K (3198 °C)
Entalpía de fusión: 62 kJ/mol
Varios
Estructura cristalina: cúbica centrada en las caras
N° CAS: 7440-34-8
Conductividad Térmica: 12 W/(K·m)
Isótopos más estables
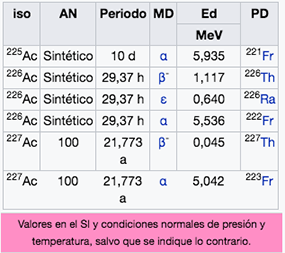
Hafnio
El hafnio es un elemento químico de número atómico 72 que se encuentra en el grupo 6 de la tabla periódica de los elementos y se simboliza como Hf.
Es un metal de transición, brillante, gris-plateado, químicamente muy parecido al circonio, encontrándose en los mismos minerales y compuestos, y siendo difícil separarlos. Se usa en aleaciones con wolframio en filamentos y en electrodos. También se utiliza como material de barras de control de reactores nucleares debido a su capacidad de absorción de neutrones. Recientemente, se ha convertido en el material utilizado para fabricar los transistores de los procesadores de la conocida marca Intel.
Principales propiedades
Es un metal dúctil, brillante, plateado y resistente a la corrosión; químicamente muy similar al circonio. Estos dos elementos tienen el mismo número de electrones en sus capas exteriores y sus radios iónicos son muy similares debido a la contracción de los lantánidos. Por eso son muy difíciles de separar (los procesos geológicos no los han separado y en la naturaleza se encuentran juntos) y no hay otros elementos químicos que se parezcan más entre sí. Las únicas aplicaciones para las cuales es necesario separarlos es en aquellas en las que se utilizan por sus propiedades de absorción de neutrones, en reactores nucleares.
El carburo de hafnio (HfC) es el compuesto binario más refractario conocido, con un punto de fusión de 3.890 °C, y el nitruro de hafnio (HfN) es el más refractario de todos los nitruros metálicos conocidos, con un punto de fusión de 3.310 °C. El carburo mixto de hafnio y tántalo (Ta4HfC5) es el compuesto múltiple con más alto punto de fusión conocido, 4.215 °C.
El hafnio es resistente a las bases concentradas, pero los halógenos pueden reaccionar con él para formar tetrahaluros de hafnio (HfX4). A temperaturas altas puede reaccionar con oxígeno, nitrógeno, carbono, boro, azufre y silicio.
Aplicaciones
El hafnio se utiliza para fabricar barras de control empleadas en reactores nucleares, como las que se pueden encontrar en submarinos nucleares, debido a que la sección de captura de neutrones del hafnio es unas 600 veces la del circonio, con lo cual tiene una alta capacidad de absorción de neutrones, y además tiene unas propiedades mecánicas muy buenas, así como una alta resistencia a la corrosión. Otras aplicaciones:
- En lámparas de gas e incandescentes.
- En catalizadores para polimerización metalocénica.
- Para eliminar oxígeno y nitrógeno de tubos de vacío.
- En aleaciones de hierro, titanio, niobio, tántalo y otras aleaciones metálicas.
- En enero de 2007, se anunció como parte fundamental de una nueva tecnología de microprocesadores, desarrollada separadamente por IBM e Intel, en reemplazo del silicio pero únicamente en el dieléctrico de compuerta del transistor, en el resto del dispositivo se sigue utilizando silicio que es el material de base tradicional.
- Uno de sus derivados, en concreto el óxido de hafnio posee un índice de refracción intermedio entre el silicio y el aire. Este compuesto se emplea en la transición entre estos dos interfaces en los dispositivos fotónicos de silicio, reduciendo de esta manera las pérdidas debidas a reflexiones.
Historia
Se llamó hafnio por el nombre de Copenhague en latín, Hafnia, la ciudad danesa en donde fue descubierto por Dirk Coster y George Hevesy en 1923. Poco después se predijo, usando la teoría de Bohr, que estaría asociado con el circonio, y finalmente se encontró en el circón mediante unos análisis con espectroscopia de rayos X en Noruega.
Obtención
Se encuentra siempre junto al circonio en sus mismos compuestos, pero no se encuentra como elemento libre en la naturaleza. Está presente, como mezclas, en los minerales de circonio, como el circón (ZrSiO4) y otras variedades de éste (como la albita), conteniendo entre un 1 y un 5% de hafnio.
Debido a la química casi idéntica que presentan el circonio y el hafnio, es muy difícil separarlos. Aproximadamente la mitad de todo el hafnio metálico producido se obtiene como subproducto de la purificación del circonio. Esto se hace reduciendo el tetracloruro de hafnio (HfCl4) con magnesio o sodio en el proceso de Kroll.
Precauciones
Es necesario tener cuidado al trabajar el hafnio pues cuando se divide en partículas pequeñas es pirofórico y puede arder espontáneamente en contacto con el aire. Los compuestos que contienen este metal raramente están en contacto con la mayor parte de las personas y el metal puro no es especialmente tóxico, pero todos sus compuestos deberían manejarse como si fueran tóxicos (aunque las primeras evidencias no parecen indicar un riesgo muy alto).
Referencias
1. WebElements.com - Hafnium
2. EnvironmentalChemistry.com - Hafnium

Información general
Nombre: Hafnio
Símbolo: hf
Número: 72
Serie Química: Metales de transición
Grupo: 4
Período: 6
Bloque: d
Masa Atómica: 178,49 U
Configuración Electrónica: [Xe54]6s2 4f14 5d2
Dureza Mohs 5,5
Electrones por Nivel: 2, 8, 18, 32, 10, 2
Propiedades Atómicas
Radio Medio: 155 pm
Electronegatividad: 1,3 (escala de Pauling)
Radio atómico (calc): 208 pm (radio de Bohr)
Radio covalente: 150 pm
Estado(s) de oxidación: 4, 3, 2
Óxido: Anfótero
1.ª Energía de ionización: 658,5 kJ/mol
2.ª Energía de ionización: 1440 kJ/mol
3.ª Energía de ionización: 2250 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido (paramagnético)
Densidad: 13310 kg/m3
Punto de fusión: 2506 K (2233 °C)
Punto de ebullición: 4876 K (4603 °C)
Entalpía de vaporización: 575 kJ/mol
Entalpía de fusión: 24,06 kJ/mol
Presión de vapor: 0,00112 Pa a 2500 K
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-58-6
N.º EINECS: 231-166-4
Calor específico: 140 J/(K·kg)
Conductividad eléctrica: 3,12·106 S/m
Conductividad Térmica: 23 W/(K·m)
Módulo elástico: 78 GPa
Coeficiente de Poisson: 0,37
Velocidad del sonido: 3010 m/s a 293,15 K (20 °C)
Isótopos más estables
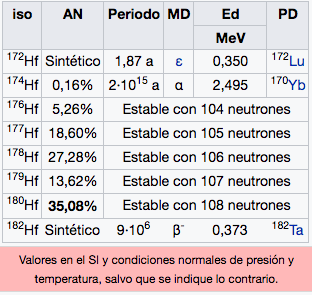
Rutherfordio
El rutherfordio (anteriormente llamado kurchatovio) es un elemento químico de la tabla periódica cuyo símbolo es Rf y su número atómico es 104. Su nombre fue elegido en honor del Barón Ernest Rutherford, científico colaborador del modelo atómico y física nuclear. Este es un elemento sintético altamente radiactivo cuyo isótopo más estable es el 261Rf con una vida media de aproximadamente 13 horas.
Historia
El rutherfordio fue sintetizado por primera vez en 1964 en el Instituto Conjunto para la Investigación Nuclear en Dubna (Rusia). Los investigadores bombardearon plutonio con iones de neón acelerados a 113 - 115 MeV, y sostuvieron haber encontrado trazas de fisión nuclear sobre un vidrio de tipo especial, con un microscopio, que indicaban la presencia del nuevo elemento.
En 1969 los investigadores de la Universidad de California, Berkeley, sintetizaron el elemento sobreponiendo 249Cf y 12C en colisiones a alta energía. El grupo de Berkeley afirmó también no haber podido reproducir el método usado por los investigadores soviéticos.
Este hecho llevó a una controversia sobre el nombre del elemento; puesto que los soviéticos sostenían haberlo sintetizado en Dubna propusieron Dubnio (Db), y también Kurchatovio (Ku) para el elemento 104, en honor de Ígor Vasílievich Kurchátov (1903-1960), exjefe de la investigación nuclear soviética. Los estadounidenses en cambio, propusieron Rutherfordio (Rf) en honor de Ernest Rutherford un famoso físico nuclear neozelandés. La International Union of Pure and Applied Chemistry (IUPAC) adoptó temporalmente el nombre Unnilquadium (Unq), según la denominación sistemática de elementos, hasta que en 1997 la disputa se resolvió con la adopción del nombre actual.
Aplicaciones
Su uso sólo es de estudio pues al ser un elemento Transfermio, es muy inestable.
Referencias
1. «Nombres y símbolos en español acordados por la RAC, la RAE, la RSEQ y la Fundéu». 1 de marzo de 2017. Consultado el 4 de abril de 2017.
Información general
Nombre: Rutherfordio
Símbolo: Rf
Número: 104
Serie Química: Metales de transición
Grupo: 4
Período: 7
Bloque: d
Masa Atómica: [261] u
Configuración Electrónica: Probablemente [Rn]5f14 6d2 7s2
Propiedades Físicas
Estado Ordinario: Presuntamente sólido
Tantalio
Es un elemento químico de número atómico 73, que se sitúa en el grupo 5 de la tabla periódica de los elementos. Su símbolo es Ta. Se trata de un metal de transición raro, azul grisáceo, duro, que presenta brillo metálico y resiste muy bien la corrosión. Se encuentra en el mineral tantalita. Es fisiológicamente inerte, por lo que entre sus variadas aplicaciones, se puede emplear para la fabricación de instrumentos quirúrgicos y en implantes. El tántalo es una elección razonable cuando se requiere una alta resistencia a la corrosión. Aunque el tántalo no sea un metal noble, es comparable a estos en lo que respecta a la resistencia química. Además, el tántalo es muy fácil de conformar, incluso netamente por debajo de la temperatura ambiente, a pesar de su estructura cristalina cúbica centrada en el espacio.La resistencia a la corrosión del tántalo lo convierte en un material valioso en un gran número de aplicaciones químicas. Utilizamos nuestro material «inflexible», por ejemplo, para producir intercambiadores de calor para el sector de la construcción de aparatos, carros de carga para la construcción de hornos, implantes para la tecnología médica y componentes de capacitores para la industria electrónica
Características principales
El tántalo es un metal gris, brillante, pesado, dúctil, de alto punto de fusión, buen conductor de la electricidad y del calor y muy duro. Es muy resistente al ataque por ácidos; se disuelve empleando ácido fluorhídrico o mediante fusión alcalina. Es muy parecido al niobio y se suele extraer del mineral tantalita, que en la naturaleza aparece generalmente formando mezclas isomorfas con la columbita que se conocen con el nombre de coltán.
Alcanza el máximo estado de oxidación del grupo +5.
Su nombre recuerda a Tántalo, hijo de Júpiter y padre de Níobe. Sufrió un castigo mítico por entregarles la bebida de los dioses (la ambrosía) a los humanos. Zeus lo condenó a la sed eterna y así, sumergido, cuando intentaba beber, las aguas se apartaban. Se relaciona este fenómeno con la cualidad del metal de no ser atacado por los ácidos.
Fue descubierto por el sueco Anders Gustaf Ekeberg en 1802.
Usos
Se utiliza casi exclusivamente en la fabricación de condensadores electrolíticos de tántalo; por tanto, es un componente esencial de los dispositivos electrónicos muy compactos: teléfonos móviles, GPS, satélites artificiales, armas teledirigidas, televisores de plasma, videoconsolas, ordenadores portátiles, PDAs, MP3, MP4, etc.
El Ta2O5-SiO2 es utilizado como catalizador en la síntesis de butadieno a partir de etano.
En los últimos años el tántalo se ha introducido también en el mercado numismático de la moneda de colección, siendo Kazajistán el primer país del mundo en acuñar monedas realizadas con tántalo tanto en su estado natural como coloreado mediante diferentes métodos de oxidación que logran alterar su color original.
También se utiliza en implantes de rodilla, cadera y columna, siendo la Compañía Zimmer Biomet (Warsaw, IN, USA) el fabricante con mucha masa.
Producción
El tántalo se extrae del coltán (columbita + tantalita), cuyo mayor productor es la República Democrática del Congo, con cerca del 9 % de las reservas mundiales estimadas. Venezuela pasa a ser el país con mayor reserva estimada del mundo con el 60%.
El ejecutivo venezolano oficializó a través de tres decretos presidenciales la creación de tres empresas mixtas para la exploración y explotación de tántalo (coltan) cuya creación había sido acordada el 5 de agosto de 2016, cuando el presidente Nicolás Maduro se reunió con directivos de las trasnacionales.
En los decretos N° 2.538, 2.539 y 2.540, publicados en la Gaceta Oficial n.º 41.0265 se establece que las tres compañías mixtas, en las que la Corporación Venezolana de Minería (CVM) tendrá 55% de participación accionaria, estarán adscritas al Ministerio de Desarrollo Minero Ecológico.
La primera asociación es la Empresa Mixta Minera Metales del Sur, integrada por la Corporación Venezolana de Minería y la canadiense Energold Minerals, Inc., con participación accionaria de 55% y 45%, respectivamente.
Referencias
1. «Nombres y símbolos en español acordados por la RAC, la RAE, la RSEQ y la Fundéu». 1 de marzo de 2017. Consultado el 4 de abril de 2017.
Información general
Nombre: Tántalo o tantalio
Símbolo: Ta
Número: 73
Serie Química: Metales de transición
Grupo: 5
Período: 6
Bloque: d
Masa Atómica: 180,9479 U
Configuración Electrónica: [Xe]4f14 5d3 6s2
Dureza Mohs 6,5
Electrones por Nivel: 2, 8, 18, 32, 11, 2
Propiedades Atómicas
Radio Medio: 145 pm
Electronegatividad: 1,5 (escala de Pauling)
Radio atómico (calc): 200 pm (radio de Bohr)
Radio covalente: 138 pm
Estado(s) de oxidación: 5, 4, 3, 2, -1
Óxido: Óxido de tántalo
1.ª Energía de ionización: 761 kJ/mol
2.ª Energía de ionización: 1500 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 16650 kg/m3
Punto de fusión: 3290 K (3017 °C)
Punto de ebullición: 5731 K (5458 °C)
Entalpía de vaporización: 743 kJ/mol
Entalpía de fusión: 31,6 kJ/mol
Presión de vapor: 0,776 Pa a 3269 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7440-25-7
N.º EINECS: 231-135-5
Calor específico: 140 J/(K·kg)
Conductividad eléctrica: 7,61 × 106 S/m
Conductividad Térmica: 57,5 W/(K·m)
Módulo elástico: 186 GPa
Coeficiente de Poisson: 0,34
Isótopos más estables
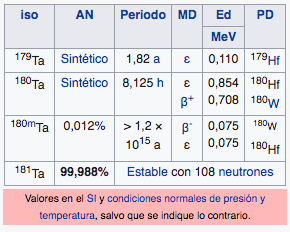
Dubnio
El dubnio es un elemento químico de la tabla periódica de los elementos cuyo símbolo es Db y su número atómico 105. El elemento fue nombrado en honor a la ciudad de Dubna, Rusia, donde fue producido por primera vez. Es un elemento sintético y radiactivo; y su isótopo más estable conocido, dubnio-268, tiene un período de semidesintegración de aproximadamente veintiocho horas.
En la tabla periódica de los elementos, es un elemento del bloque d y es un elemento transactínido. Es un miembro del séptimo período y pertenece al grupo 5 de elementos. Experimentos químicos confirmaron que dubnio se comporta como el homólogo más pesado que tantalio en el grupo 5. Las propiedades químicas del dubnio se conocen parcialmente. El elemento es similar a otros del grupo 5.
En los años sesenta, se produjeron cantidades microscópicas de dubnio en laboratorios de la Unión Soviética y California. Fue descubierto por el ruso Georgii Flerov en 1967-1970, y por el estadounidense Albert Ghiorso en 1970. Cuando se descubrió, la prioridad del descubrimiento y por lo tanto el nombramiento del elemento, se disputó entre los científicos soviéticos y estadounidenses, que unos propusieron llamarlo Nielsbohrio y los otros Hahnio, aunque estos nombres no fueron reconocidos internacionalmente. Desde entonces el elemento se pasó a llamar temporalmente unnilpentio, hasta que en 1997 la Unión Internacional de Química Pura y Aplicada —IUPAC por sus siglas en inglés— estableció como el nombre oficial del elemento a dubnio.
Historia
La existencia del dubnio fue indicada por primera vez en 1968 por científicos rusos del Instituto Central de Investigaciones Nucleares (ICIN) en Dubna, Unión Soviética (actualmente Rusia). Allí los investigadores bombardearon un blanco de americio-243 con iones de neón-22. Se informó la medición de emisiones de actividad alfa de 9,40 MeV y 9,70 MeV y determinaron que los decaimientos provenían de los isótopos 260Db o 261Db:
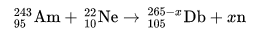
Dos años después el equipo de Dubna separó sus productos de reacción mediante el uso de cromatografía de gradiente térmico después de la conversión a cloruros por la interacción con NbCl5. El equipo observó una actividad de fisión espontánea de 2,2 segundos contenida en un cloruro volátil que poseía propiedades eka-tantalio, probablemente pentacloruro de dubnio-261, 261DbCl5.
A finales de abril de 1970 un grupo de investigadores liderados por Albert Ghiorso de la Universidad de California, publicaron los detalles de la síntesis de 260Db mediante el bombardeo de un blanco de californio-249 con iones de nitrógeno-15, y midieron la desintegración alfa de 260Db con un período de semidesintegración de 1,6 segundos y una energía de desintegración de 9,10 MeV, correlacionada con el producto de desintegración de lawrencio-256:
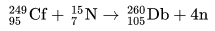
Estos resultados de los científicos de Berkeley no confirmaron los hallazgos soviéticos con respecto a la desintegración alfa de 9,40 MeV o 9,70 MeV de dubnio-260, dejando solo al dubnio-261 como el isótopo posiblemente producido. En 1971, el equipo de Dubna repitió su reacción con una mejor puesta en marcha y fueron capaces de confirmar los datos de desintegración para 260Db con la reacción:
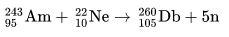
En 1976 el equipo de Dubna continuó su estudio de la reacción mediante la cromatografía de gradiente térmico, y lograron identificar el producto como pentabromuro de dubnio-260, 260DbBr5.
En 1992 el IUPAC/IUPAP Transfermium Working Group evaluó las pretensiones de los dos grupos y concluyó que la confianza en el descubrimiento creció a partir de los resultados de ambos laboratorios, y por lo tanto, la pretensión del descubrimiento debería ser compartida.
Aplicaciones
Al igual que otros transfermios, su uso es meramente científico.
Referencias
1. Barber, R. C.; Greenwood, N. N.; Hrynkiewicz, A. Z.; Jeannin, Y. P.; Lefort, M.; Sakai, M.; Ulehla, I.; Wapstra, A. P.; Wilkinson, D. H. (1993). «Discovery of the transfermium elements. Part II: Introduction to discovery profiles. Part III: Discovery profiles of the transfermium elements». Pure and Applied Chemistry (en inglés) 65 (8): 1757. doi:10.1351/pac199365081757
Información general
Nombre: Dubnio
Símbolo: Db
Número: 105
Serie Química: Metales de transición
Grupo: 5
Período: 7
Bloque: d
Masa Atómica: [262] u
Configuración Electrónica: Probablemente [Rn]5f14 6d3 7s2
Propiedades Atómicas
Radio atómico (calc): 139 (estimado) pm (radio de Bohr)
Radio covalente: 149 (estimado) pm
Estado(s) de oxidación: 5, 4, 3 (previstos)
Propiedades Físicas
Estado Ordinario: Presuntamente sólido
Varios
N° CAS: 53850-35-4
Isótopos más estables
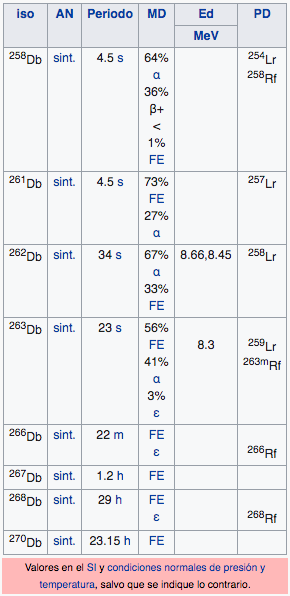
Wolframio
El wolframio o volframio, también conocido como wólfram o tungsteno, es un elemento químico de número atómico 74 que se encuentra en el grupo 6 de la tabla periódica de los elementos. Su símbolo es W.
Es un metal escaso en la corteza terrestre, pero se encuentra en determinados minerales en forma de óxidos o sales. Es de color gris acerado, muy duro y denso, tiene el punto de fusión más elevado de todos los metales y el punto de ebullición más alto de todos los elementos conocidos. Se usa en la fabricación de aparejos para pesca, en los filamentos de las lámparas incandescentes, en electrodos no consumibles de soldaduras, en resistencias eléctricas, y aleado con el acero, en la fabricación de aceros especiales.
Su variedad de carburo de wolframio sinterizado se emplea para fabricar herramientas de corte. Esta variedad absorbe más del 60 % de la demanda mundial de wolframio.
El wolframio es un material estratégico y ha estado en la lista de productos más codiciados desde la Segunda Guerra Mundial. Por ejemplo, el gobierno de Estados Unidos mantiene unas reservas nacionales de seis meses junto a otros productos considerados de primera necesidad para su supervivencia.
Historia
En 1779, Peter Woulfe, mientras estudiaba una muestra del mineral wolframita, (Mn, Fe) (WO4), predijo que debía contener un nuevo elemento. Dos años después, en 1781, Carl Wilhelm Scheele y Torbern Bergman sugirieron que se podía encontrar un nuevo elemento reduciendo un ácido (denominado «ácido túngstico») obtenido a partir del mineral scheelita (CaWO4). En 1783, en España, los hermanos Juan José Elhúyar y Fausto Elhúyar encontraron un ácido, a partir de la wolframita, idéntico al ácido túngstico; el primero trajo el mineral consigo de su periplo por las minas y universidades europeas. En Upsala (Suecia) tomó clases con Bergman el cual le habló de sus intuiciones respecto del wolframio. Así, consiguieron aislar el nuevo elemento mediante una reducción con carbón vegetal, en el Real Seminario de Vergara donde tenía su laboratorio la Real Sociedad Bascongada de Amigos del País. Más tarde, publicaron Análisis químico del wolfram y examen de un nuevo metal que entra en su composición describiendo este descubrimiento.
En 1820 el químico sueco Berzelius obtuvo wolframio mediante una reducción con hidrógeno. El método, empleado todavía actualmente, comenzó a abrir las posibilidades de uso de este metal extraordinario, pero su desarrollo fue muy lento. La necesidad constante de nuevos materiales para alimentar las guerras del siglo XIX hizo que los aceristas austríacos e ingleses empezaran a investigar las propiedades del wolframio como elemento de aleación. En la Universidad de Viena se experimentó con aleaciones a base de wolframio.
Etimología
La palabra «tungsteno» procede del sueco; tung se traduce como «pesado» y sten, «piedra», es decir, «piedra pesada». El vocablo se debe al mineralogista sueco Axel Fredrik Cronstedt, descubridor del níquel, quien incluyó una descripción de este mineral desconocido en su libro Ensayos de Mineralogía de 1758. En la versión inglesa, de renombrado prestigio académico en la época, se mantuvo la palabra tungsten, lo que explica su popularidad en el mundo anglosajón.
La palabra «wolframio» procede de las alemanas wolf y rahm, pudiendo significar «poco valor» También se traduce como «Baba de Lobo» en referencia a las supersticiones de los mineros medievales sajones que creían que el diablo se aparecía en forma de lobo y habitaba las profundidades de las minas corroyendo la casiterita con sus fauces babeantes. Este metal aparecía mezclado con el ácido de otro desconocido —wolframio— que actuaba corroyéndolo.
Wolframio o tungsteno
La IUPAC denomina al elemento 74, de símbolo W, como tungsten (en español, tungsteno). El nombre wolfram fue suprimido en la última edición de su Libro rojo (Nomenclatura de Química Inorgánica. Recomendaciones de la IUPAC de 2005). Sin embargo, dicha eliminación no ha sido aceptada por los miembros españoles de la IUPAC ni por organismos de la lengua española, que siguen considerando el nombre original wolfram (wolframio) como el nombre correcto. En Latinoamérica el elemento 74 suele ser conocido como tungsteno.
El nombre de wolfram ya había sido adoptado oficialmente, en lugar de tungsten por la IUPAC en su 15ª conferencia, celebrada en Ámsterdam en 1949.
Características
Propiedades físicas
En forma natural, el wolframio es un metal gris acero que es a menudo frágil y difícil de trabajar, pero si es puro, se puede trabajar con facilidad. Se trabaja por forjado, trefilado, extrusión y sinterización. De todos los metales en forma pura, el wolframio tiene el más alto punto de fusión (3410 °C, 6170 °F), menor presión de vapor (a temperaturas superiores a 1650 °C, 3002 °F) y la mayor resistencia a tracción. Además, tiene el coeficiente de dilatación térmica más bajo de cualquier metal puro, y se detecta fácilmente con reactivo de Arnulphi en medio básico (KOH), tornándose este mismo incoloro. La expansión térmica es baja, su punto de fusión es alto y la fuerza se debe a fuertes enlaces covalentes que se forman entre los átomos de wolframio en el orbital 5d. Cabe señalarse que la aleación de pequeñas cantidades con el acero aumenta su resistencia. Tiene una muy buena combinación de ventajas entre las que destacan su gran fuerza y resistencia calórica, además de una aceptable resistencia química, ya que no es fácilmente atacable por los ácidos. El metal suele trabajarse por sinterización. El método consiste en aglomerarlo en forma de polvo de diminutos granos en una matriz metálica. Aunque la mejor opción es el cobalto, se puede encontrar también el níquel e incluso el hierro en estos casos. Todas sus aleaciones se distinguen por su enorme dureza y su resistencia. El metal se comporta excelentemente incluso a altas temperaturas, cosa que el renio no, por ejemplo, pese a que ambos metales comparten un punto de fusión similar. El wolframio es el metal más abundante de los metales de transición del grupo 6 de la tabla periódica. En caso de escasear, el molibdeno suele sustituirle. Una de sus características es que al exponerse a luz ultravioleta este tiene un brillo azulado muy brillante
Propiedades químicas
El wolframio resiste las reacciones redox, casi todos los ácidos comunes (incluyendo el fluorhídrico) y álcalis, pero solo en su estado de máxima pureza, aunque se oxida rápidamente expuesto a peróxido de hidrógeno (comúnmente conocido como agua oxigenada). El wolframio a temperatura ambiente sostiene el ataque de casi todos los ácidos importantes en cualquier concentración aunque puede corroerse con facilidad en ácido nítrico y agua oxigenada. Con el ácido fluorhídrico ocurre el fenómeno de pasivación, formándose fluoruros en su superficie. No obstante la capa de óxido del wolframio no es estable por encima de 400 ºC y el metal queda expuesto. Los compuestos de wolframio más usados (p. ej.: carburo de wolframio) mejoran algo su ya alta resistencia a la corrosión, y de hecho les cuesta disolverse en agua regia, en estos casos, el metal es adecuado para su uso como joya, especialmente en anillos de última generación. Pese a que resiste bien los ácidos, puede irónicamente oxidarse incluso con sal de cocina común, de hecho el agua pura lo oxida (aunque dicho óxido no avanzará más allá de la superficie). Es un metal difícil de alear, solo lo hace con los metales refractorios, los ferrosos y algunas excepciones. No se amalgama con el mercurio a ninguna temperatura. El wolframio se disuelve en aluminio fundido, y es uno de los pocos metales que pese a no asemejarse nada al wolframio se alea perfectamente. El estado de oxidación más común del wolframio es +6, pero presenta todos los estados de oxidación, desde –2 hasta +6. Normalmente se combina con el oxígeno para formar el óxido wolfrámico amarillo (WO3) que se disuelve en soluciones de alcalino acuoso para formar iones de wolframio (WO42-).
Los carburos de wolframio (W2C y WC) se producen por el calentamiento en polvo de carbón y son algunos de los carburos más duros, con un punto de fusión de 2.770 °C para WC y 2.780 °C para el W2C, el WC es un conductor eléctrico eficiente, pero el W2C no, el carburo se comporta de manera similar al mismo elemento sin alear, y es resistente al ataque químico, aunque reacciona fuertemente con el cloro para formar hexacloruro de wolframio (WCl6).
Las soluciones acuosas se caracterizan por la formación de ácido heteropoliácido y aniones de polioxometalato en condiciones neutras y ácidas, además produce la acidificación del anión del metatungstato muy soluble, después de lo cual se alcanza el equilibrio. Muchos aniones de polioxometalato existen en otras especies metaestables, la inclusión de un átomo de diferentes características, como el fósforo, en lugar de dos hidrógenos centrales, en el metatungstato produce una gran variedad de ácidos heteropoliácidos, como el ácido fosfotúngstico.El ácido fosfotúngstico soportado puede usarse como catalizador.
Aplicaciones
En estado puro se utiliza en la fabricación de filamentos para lámparas eléctricas, resistencias para hornos eléctricos con atmósfera reductoras o neutras, contactos eléctricos para los distribuidores de automóviles, también como proyectil anticarro (flecha) por su elevado punto de fusión y densidad, ánodos para tubos de rayos X y de televisión.
Tiene usos importantes en aleaciones para herramientas de corte a elevada velocidad, como las fresas para instrumentos odontológicos (W2C), en la fabricación de bujías y en la preparación de barnices (WO3) y mordientes en tintorería, en las puntas de los bolígrafos y en la producción de aleaciones de acero duras y resistentes.
El wolframio y su aleación más popular, el carburo de wolframio son en ambos casos, excelentes reflectores de neutrones. Los cristales de wolframio con la estructura BCC están tan comprimidos que resultan ser eficaces escudos contra la radiación de todas las clases. Barras y planchas de wolframio o carburo de wolframio pueden resistir emisiones incluso de partículas gamma, rayos de neutrones. Es un poderoso escudo, superior al plomo y que además ofrece una toxicidad nula, cosa que el plomo no. Repele los neutrones y la energía nuclear debido a su gran densidad y estabilidad atómica.
Los wolframatos de calcio y magnesio se utilizan en la fabricación de tubos fluorescentes.
El carburo de wolframio, estable a temperaturas del orden de 500 °C, también se usa como lubricante seco.
El gas hexafluoruro de wolframio se emplea en la fabricación de circuitos integrados.
Referencias
1. «Nombres y símbolos en español acordados por la RAC, la RAE, la RSEQ y la Fundéu». 1 de marzo de 2017. Consultado el 4 de abril de 2017.
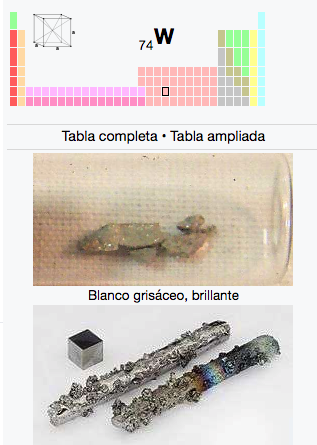
Información general
Nombre: Wolframio o tungsteno
Símbolo: W
Número: 74
Serie Química: Metales de transición
Grupo: 6
Período: 6
Bloque: d
Masa Atómica: 183,84 u
Configuración Electrónica: [Xe] 4f14 5d4 6s2
Dureza Mohs: 7,5
Electrones por nivel: 2, 8, 18, 32, 12, 2
Propiedades Atómicas
Radio medio: 135 pm
Electronegatividad: 2,36 (escala de Pauling)
Radio atómico (calc): 193 pm (radio de Bohr)
Radio covalente: 146 pm
Estado(s) de oxidación: 6, 5, 4, 3, 2 (levemente ácido)
1.ª Energía de ionización: 770 kJ/mol
2.ª Energía de ionización: 1700 kJ/mol
Propiedades Físicas
Estado Ordinario: sólido
Densidad: 19600 kg/m3
Punto de fusión: 3695 K (3422 °C)
Punto de ebullición: 6203 K (5930 °C)
Entalpía de vaporización: 82456 kJ/mol
Entalpía de fusión: 35,4 kJ/mol
Presión de vapor: 4,27 Pa a 3680 K
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
Calor específico: 130 J/(K·kg)
Conductividad térmica: 174 W/(K·m)
Módulo elástico: 411 GPa
Velocidad del sonido: 5174 m/s a 293,15 K (20 °C)
Isótopos más estables
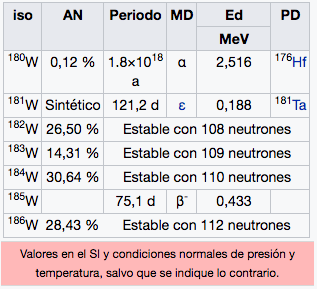
Seaborgio
El seaborgio es un elemento químico de la tabla periódica cuyo símbolo es Sg y su número atómico es 106. Es un elemento sintético cuyo isótopo más estable es el 271Sg que tiene una vida media de 2,4 minutos. Su naturaleza química es similar a la del wolframio.
Historia
El elemento 106 fue descubierto casi simultáneamente por dos laboratorios. En junio de 1974, un grupo de investigadores estadounidenses liderado por Albert Ghiorso en el laboratorio Lawrence Berkeley de la Universidad de California, Berkeley reportó la creación de un isótopo de número de masa 263 y una vida media de 1,0 s. En septiembre de 1974, un equipo soviético liderado por Georgii Flerov en el Instituto Conjunto para la Investigación Nuclear en Dubna reportó que había producido un isótopo de número de masa 259 y una vida media de 0,48 s.
Debido a que el trabajo del equipo estadounidense fue confirmado por un grupo independiente primero, estos sugirieron el nombre de seaborgio en honor al químico estadounidense Glenn T. Seaborg destacado miembro del equipo estadounidense junto con Albert Ghiorso, J. M. Nitschke, Jose R. Alonso, C. T. Alonso, Matti Nurmia, E. Kenneth Hulet, y R. W. Lougheed en reconocimiento a su participación en el descubrimiento de varios actínidos. El nombre seleccionado por los investigadores fue motivo de controversia. Un comité internacional decidió en 1992 que los laboratorios de Berkeley y Dubna deberían compartir el crédito por el descubrimiento.
Surgió una controversia como consecuencia de que la IUPAC adoptó el nombre unnilhexio (símbolo Unh) de manera temporal, según la denominación sistemática de elementos. En 1994 un comité de la IUPAC recomendó que el elemento 106 fuese nombrado rutherfordio y adoptó la regla de que ningún elemento podría ser nombrado en honor a una persona viva. Esta decisión fue duramente criticada por la American Chemical Society. Los críticos hicieron notar que ya existía un precedente ya que el elemento einstenio fue nombrado así durante la vida de Albert Einstein. En 1997 el nombre seaborgio fue reconocido internacionalmente para el elemento 106, como parte de un compromiso sobre los nombres de los elementos del 104 a 108.
Isótopos
Existen 12 isótopos conocidos del seaborgio, el de mayor vida media es el 271Sg que decae por desintegración alfa y fisión espontánea. Tiene una vida media de 2,4 minutos. El isótopo encontrado de menor vida media es el 258Sg que también sufre desintegración alfa y fisión espontánea. Su vida media es de 2,9 ms.
Aplicaciones
Debido a sus inestables Isótopos, y al igual que otros transfermios, su uso es meramente científico.
Referencias
Información general
Nombre: Seaborgio
Símbolo: Sg
Número: 106
Serie Química: Metales de transición
Grupo: 6
Período: 5
Bloque: d
Masa Atómica: 269 u
Configuración Electrónica: [Rn] 7s2 5f14 6d4
Electrones por nivel: 2, 8, 18, 32, 32, 12, 2
Propiedades Atómicas
Radio covalente: 143 (estimado) pm
Estado(s) de oxidación: 6
Propiedades Físicas
Estado Ordinario: Probablemente sólido
Varios
N.º CAS: 54038-81-2
Renio
—de Rhenus, nombre latino del Rin— es un elemento químico, de número atómico 75, que se encuentra en el grupo 7 de la tabla periódica de los elementos y cuyo símbolo es Re, descubierto en 1925 por tres científicos alemanes. Es un metal de transición de color blanco-plata, sólido, refractario y resistente a la corrosión, muy utilizado en joyería y como catalizador. Sus propiedades químicas son muy parecidas a las del manganeso, es muy escaso en la corteza terrestre y se obtiene principalmente a partir de minerales de molibdeno.
Existen 35 isótopos y 26 radioisótopos de este elemento, de los cuales los más estables son el 185Re y el 187Re. Los principales yacimientos de renio se encuentran en América y Asia, destacando los de Chile y Kazajistán.
Características principales
En su forma natural el renio es un elemento sólido, de color blanco plateado y grisáceo, y pertenece a la serie química de los metales de transición. Es uno de los metales con punto de fusión más elevado, solo superado por el wolframio y el carbono. Tiene estados de oxidación -1, 0, +1, +2, +3, +4, +5, +6 y +7. Es capaz de formar aniones complejos, tales como el pentacloruro de renio, que son capaces de crear sales diferentes debido al efecto de oxidación que produce este elemento cuando recibe el contacto del aire a elevadas temperaturas.
El renio es uno de los metales más densos que existen, ya que su densidad de 21 020 kg/m3 solo es superada por el iridio, el osmio y el platino. Es un elemento escaso en la corteza terrestre (solo 0,001 ppm), mientras que en el aire es estable a temperaturas superiores a los 400°C, punto a partir del cual comienza a arder y produce heptaóxidos. También hay que destacar que hay pocos picómetros (pm) de diferencia entre los radios medio (135 pm), atómico (137 pm) y covalente (159 pm).
Historia
El descubrimiento del renio se le atribuye a los científicos alemanes Ida Eva Tacke, Walter Karl Friedich Noddack y Otto Carl Berg, debido a que en 1925 publicaron que lo habían detectado en minerales de tantalita, wolframita y columbita mediante análisis espectrográficos con rayos X, en las cercanías del Rin —de donde deriva su nombre en latín—. Anteriormente, Dmitri Mendeléyev estuvo cerca de haberlo descubierto, pues al tratar de deducir las propiedades de un mineral de alto contenido en renio, pensaba que era un derivado del manganeso, por lo que lo denominó como «dvi-manganeso». Posteriormente Henry Moseley, en 1914, extrapoló cálculos acerca del hipotético elemento. En 1928 se consiguió extraer 1 g del elemento de 660 kg de molibdenita, y cuarenta años más tarde, en 1968, se estimó que el 75% de las extracciones de este elemento en los Estados Unidos fueron destinadas a la fabricación de aleaciones para metales refractarios. En 1971 Chile abrió las puertas a su propia industria metalúrgica, que trabajaba principalmente con el renio. En el periodo comprendido entre 1984 y 1986 se empezaron a diseñar complejos y sofisticados catalizadores basados en este elemento.
En 1908 el químico japonés Masataka Ogawa afirmó haber hallado un nuevo elemento, al que bautizó como «Niponio» —símbolo Np— en honor a su país natal; pero posteriormente se descubrió que el supuesto elemento llevaba pequeñas cantidades de renio, por lo que el símbolo que se le había asignado se empleó para nombrar al neptunio cuando se descubriese. En 2005, la NASA afirmó haber descubierto que el renio contribuyó a la creación del sistema solar. Por ello los científicos de esta organización piensan que puede existir la posibilidad de que elementos como este o el osmio procedan de pequeñas estrellas con elevada densidad de neutrones.
Abundancia y obtención
Los países con mayor producción de renio son Chile y Kazajistán, con 22 900 y 8000 toneladas respectivamente, extraídas en 2007. Otros países involucrados en la producción de renio son Estados Unidos, Armenia, Canadá, Perú y Rusia. La suma de extracciones de renio entre estos siete países es superior a 49 000 toneladas, cantidad que ha aumentado de 2006 a 2007 con una diferencia de más de 2000 kilogramos.
Existen dos métodos de obtención de renio. El primero sería mediante el procesado del molibdeno, que una vez extraído debe ser tratado con ácido nítrico o sulfúrico. La segunda manera es la reducción de perrenato amónico (NH4ReO4) con hidrógeno a una temperatura muy alta. También se puede obtener óxido de renio mediante el tratamiento de algunas sustancias generadas en la tostación de molibdenita, que se reducen con hidrógeno obteniéndose el compuesto en forma de polvo. Es uno de los elementos más escasos en la corteza terrestre, concretamente el número 79 en abundancia.
Aplicaciones
El renio, al ser un elemento metálico refractario y resistente a la corrosión, es usado principalmente en joyería, en la construcción de filamentos para espectrómetros de masas y como catalizador de reacciones de hidrogenación y deshidrogenación en la industria química. En menor escala se utiliza en aleaciones de wolframio y molibdeno, como conductor eléctrico, en la fabricación de flashes fotográficos y para la construcción de los plumines de las estilográficas. Recientemente científicos chilenos han desarrollado un compuesto derivado del renio que ataca a las células cancerosas, pasando a ser utilizado en medicina para el diagnóstico y tratamiento del cáncer.
Compuestos
Los compuestos de renio son de color blanco-plata y fácilmente solubles en agua. Varían entre los nueve estados de oxidación que tiene este elemento, —de -1 a 7—, aunque los estados de oxidación más comunes son 2, 4, 6 y 7. Normalmente se comercializa en forma de perrenatos, especialmente como perrenato sódico o perrenato de amonio.
Cloruros y oxicloruros
Los cloruros de renio más comunes son el ReCl6, el ReCl5, el ReCl4 y el ReCl3. Las estructuras de estos compuestos a menudo cuentan con una amplia red de unión característica de este metal en los estados de oxidación inferiores a 7. Las sales [Re2Cl8]2- cuentan con un enlace cuádruple metal-metal. También son muy conocidos los bromuros, los yoduros y los fluoruros. De estos últimos el más conocido es el ReF7, y el estado de oxidación de estos compuestos es +7. Por otra parte, al igual que el wolframio y el molibdeno, con el que comparte muchas de sus características químicas, forma unos compuestos llamados oxihalogenuros. Los más destacados son los oxicloruros, como el ReOCl4 o el ReO3Cl.
Óxidos y sulfuros
Los óxidos más conocidos y comunes de renio son el ReO2, el Re2O5 y el Re2O7. Este último es un óxido volátil que está contenido en una ceniza que si se reduce mediante compresión forma un óxido menor: el ReO2. Por otra parte, este elemento forma dos sulfuros muy conocidos completamente diferenciados: Re2S7 y ReS2. Con estos compuestos hay que tener especial cuidado ya que muchos son fácilmente inflamables al entrar en contacto con el aire, como el Re2S7.
Isótopos
Se han descubierto un total de 35 isótopos de renio. En la naturaleza existen dos isótopos estables, 185Re y 187Re, de los cuales el 187Re es el más abundante —62,6% de abundancia natural— y tiene una vida media de 4,35 x 1010 años. Este tiempo de vida se ve afectado en gran parte por la carga de sus átomos. La desintegración beta de los 187Re se utiliza para la datación de minerales de este elemento y de osmio, cuya energía disponible para este decaimiento es de 2,6 ev, una de las energías más bajas conocidas entre todos los radionucleidos. En medicina, son muy utilizados los radioisótopos 186Re y 188Re, que tienen una vida media muy corta. En total, hay 26 radioisótopos.
Precauciones
Se sabe muy poco acerca de la toxicidad que pueden tener el renio y sus compuestos, ya que estos se utilizan en cantidades muy pequeñas. Las sales solubles que contienen este elemento, como perrenatos y haluros, sí pueden ser peligrosas. Se ha demostrado que algunos de estos compuestos tienen una toxicidad aguda en ratas. Los perrenatos de renio tienen DL50 de 2800 mg/kg —una toxicidad bastante baja—, mientras que el tricloruro de renio mostró DL50 de 280 mg/kg, una toxicidad diez veces mayor. En algunos casos, al ser un elemento radionucleido, manifiesta radiación de partículas alfa y rayos X.
Sus efectos en animales engloban irritación en ojos, piel e incluso en vías respiratorias en caso de inhalación, provocando fibrosis pulmonar y mareos en caso de recibir el contacto de un vapor derivado de este elemento. El impacto ambiental del renio se reduce a la expulsión de gases tóxicos en la industria una vez utilizado. Los compuestos de renio más peligrosos son el ReS7, que se inflama al contactar con el aire, y el hexametilrenio —quizás el más problemático ya que presenta un grave riesgo de explosión—.
Referencias
1. «Renio». La Química de Referencia. Archivado desde el original el 7 de julio de 2012. Consultado el 11 de junio de 2012.
2. Holleman y Wiberg, 1985, p. 1118.
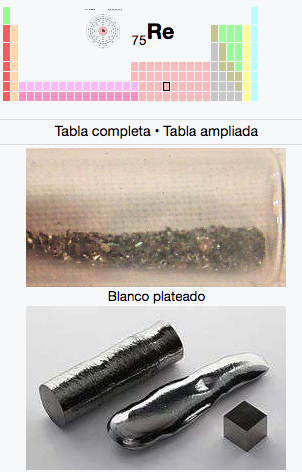
Información general
Nombre: Renio
Símbolo: Re
Número: 75
Serie Química: Metales de transición
Grupo: 7
Período: 6
Bloque: d
Masa Atómica: 186,207 u
Configuración Electrónica: [Xe] 4f14 5d5 6s2
Dureza Mohs: 7,0
Electrones por nivel: 2, 8, 18, 32, 13, 2
Propiedades Atómicas
Radio medio: 135 pm
Electronegatividad: 1,9 (escala de Pauling)
Radio atómico (calc): 137 pm (radio de Bohr)
Radio covalente: 159 pm
Estado(s) de oxidación: -1, 0, +1, +2, +3, +4, +5, +6, +7
Óxido Levemente ácido
1.ª Energía de ionización: 760 kJ/mol
2.ª Energía de ionización: 1260 kJ/mol
3.ª Energía de ionización: 2510 kJ/mol
Propiedades Físicas
Densidad: 21020 kg/m3
Punto de fusión: 3459 K (3186 °C)
Punto de ebullición: 5869 K (5596 °C)
Varios
Estructura cristalina: Hexagonal
N.º CAS: 7440-15-5
N.º EINECS: 231-124-5
Calor específico: 137 J/(K·kg)
Conductividad eléctrica: 5,42 x 106 S/m
Conductividad térmica: 47,9 W/(K·m)
Módulo elástico: 463 GPa GPa
Velocidad del sonido: 4700 m/s m/s a 293,15 K (20 °C)
Isótopos más estables
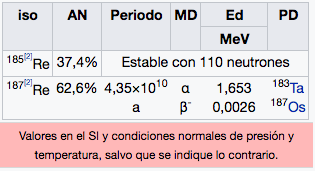
Bohrio
El bohrio (anteriormente llamado Nielsbohrio o Unnilseptio con símbolo provisional Uns o Gerphanio con símbolo Gp) es un elemento químico de la tabla periódica cuyo símbolo es Bh y su número atómico es 107. Su nombre le fue dado en honor al científico danés Niels Bohr.
Elemento químico que se espera que tenga propiedades químicas semejantes a las del elemento renio. Fue sintetizado e identificado sin ambigüedad en 1981 por un equipo de Darmstadt, Alemania, equipo dirigido por P. Armbruster y G. Müzenberg. La reacción usada para producir el elemento fue propuesta y aplicada en 1976 por un grupo de Dubna (cerca de Moscú), que estaba bajo la guía de Yuri Oganesián. Un blanco de 209Bi fue bombardeado por un haz de proyectiles de 54Cr.
La mejor técnica par identificar un nuevo isótopo es su correlación genética con isótopos conocidos a través de una cadena de desintegración radiactiva. En general, estas cadenas de decaimiento se interrumpen por fisión espontánea. Con el fin de aplicar el análisis de cadena de decaimiento deberían producirse aquellos isótopos que son más estables frente a la fisión espontánea, es decir, isótopos con números impares de protones y neutrones. Para hacer que estas pérdidas por fisión se mantengan pequeñas, debe producirse un núcleo con la mínima energía de excitación posible. En este aspecto, son ventajosas las reacciones en las que se utilizan compañeros de colisión relativamente simétricos y núcleos estrechamente enlazados de capa cerrada como el 209Bi y el 208Pb como blancos, y el 48Ca y el 50Ti como proyectiles. En el experimento de Darmstadt se encontraron seis cadenas de decaimiento. Todos los decaimientos pueden atribuirse al 262Bh, un núcleo impar producido en una reacción de un neutrón. El isótopo 262Bh decae por decaimiento de partícula alfa, con una vida media de unos 5ms. Ciertos experimentos de Dubna, llevados a cabo en 1983, establecieron la producción de 262Bh en la reacción 209Bi + 54Cr.
Efectos del Bohrio sobre la salud
Al ser tan inestable, cualquier cantidad formada se descompondrá en otros elementos con tanta rapidez que no existe razón para estudiar sus efectos en la salud humana.tambien que hasia gases tóxicos.
Efectos ambientales del Bohrio
Debido a su vida media tan extremadamente corta (0,44 s), no existe razón para considerar los efectos del bohrio en el ambiente.
Efectos especiales del Bohrio
Al ser un elemento inestable, puede servir de señalización, pero solo si se manipula correctamente o si se agrega a un componente más estable.
Referencias
1. «UNNILSEPTIO». Etimologías de Chile - Diccionario que explica el origen de las palabras. Consultado el 13 de febrero de 2019.
2. Los Alamos National Laboratory - Bohrium
Información general
Nombre: Bohrio
Símbolo: Bh
Número: 107
Serie Química: Metales de transición
Grupo: 7
Período: 7
Bloque: d
Masa Atómica: 264 u
Configuración Electrónica: [Rn] 5f14 6d5 7s2
Propiedades Atómicas
Radio medio: 128 (estimado) pm (radio de Bohr)
Electronegatividad: 1,9 (escala de Pauling)
Radio atómico (calc): 137 pm (radio de Bohr)
Radio covalente: 141 (estimado) pm
Estado(s) de oxidación: 7,6,4,2,3
1.ª Energía de ionización: 742,9 (predicción) kJ/mol
2.ª Energía de ionización: 1688,5 (predicción) kJ/mol
3.ª Energía de ionización: 2566,5 (predicción) kJ/mol
Propiedades Físicas
Estado ordinario Sólido
Isótopos más estables
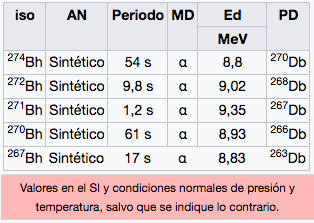
Osmio
El osmio es un elemento químico de número atómico 76 que se encuentra en el grupo 8 de la tabla periódica de los elementos. Su símbolo es Os.
Se trata de un metal de transición blanco grisáceo, frágil y sólido. Se clasifica dentro del grupo del platino, y se emplea en algunas aleaciones con platino e iridio. Se encuentra aleado en menas de platino y su tetróxido, OsO4. El osmio es el elemento natural más pesado a igual volumen (es decir, más denso) que existe, con una densidad de 22.59 g/cm3.
Se emplea en síntesis orgánica (como oxidante) y en el proceso de tinción de tejidos (como fijador) para su observación mediante microscopía electrónica, y en otras técnicas biomédicas. Las aleaciones de osmio se emplean en contactos eléctricos, puntas de bolígrafos y otras aplicaciones en las que es necesaria una gran dureza y durabilidad.
El osmio fue descubierto en 1803 por Smithson Tennant, a partir del residuo que quedaba al disolver platino nativo en agua regia. Es un elemento muy escaso en la naturaleza y que se halla en la corteza terrestre en una concentración de 0.0015 ppm. Previamente, los químicos franceses Antoine-François de Fourcroy y Louis Nicolas Vauquelin identificaron un material en el residuo del platino, al que llamaron ptène, pero no pudieron caracterizarlo correctamente al no contar con una cantidad suficiente para aislarlo.
Características
En su forma metálica es de color blanco grisáceo, duro y brillante, incluso a altas temperaturas, aunque es difícil encontrarlo en esta forma. Es más fácil obtener osmio en polvo, aunque expuesto al aire tiende a la formación del tetraóxido de osmio, OsO4, compuesto tóxico (peligroso para los ojos), oxidante enérgico, de un olor fuerte, y volátil. En la corteza terrestre se encuentra junto con otros metales del grupo del platino, generalmente aleado con iridio (y otros en menor cantidad). El osmio es otro de los metales aleados al hierro, níquel e iridio y al igual que estos, la mayor cantidad de osmio nativo se encuentra en el núcleo del planeta que por su alta densidad se hundió y pasó a formar parte de sus componentes. Las aleaciones de osmio e iridio en las que hay mayor cantidad de osmio se conocen como osmiridio, contra las que tienen más iridio, llamadas iridiosmio.
Se conoce también el dióxido de osmio, OsO2, los fluoruros OsF4, OsF5 y OsF6 y los cloruros OsCl2, OsCl3 y OsCl4. Forma asimismo diversos oxoaniones. El osmio en forma pura no se utiliza, se emplea en aleaciones como endurecedor del platino y como catalizador.
Alcanza el estado de oxidación +8, al igual que el rutenio, estado que no alcanza el hierro, que es el elemento cabecera de este grupo. Puede presentar variados estados de oxidación, desde el 0 al +8. Son muy resistentes al ataque por ácidos, disolviéndose mejor por fusión alcalina.
Es el elemento natural de mayor densidad (a presión ambiente) de la Tierra, siendo ligeramente superior a la del iridio, y tiene una de las energías cohesivas y una de las temperaturas de fusión más altas.
Propiedades
Propiedades físicas
El osmio tiene un tinte azul grisáceo y es el elemento estable más denso; es aproximadamente dos veces más denso que el plomo y ligeramente más denso que iridio. Los cálculos de densidad a partir de los datos obtenidos con cristalografía de rayos X permiten obtener los resultados más fiables para estos elementos, dando un valor de 22,587±0,009 g/cm3 para el osmio, ligeramente más denso que el valor de 22,562±0,009 g/cm3 obtenido para el iridio. Ambos metales son casi 23 veces más densos que el agua, y 1 1⁄6 veces más densos que el oro.
El osmio es un metal duro pero quebradizo que permanece con brillo incluso a altas temperaturas. Tiene una compresibilidad muy baja. En consecuencia, su módulo de compresibilidad es extremadamente alto, con valores entre 395 y 462 GPa, comparable a la del diamante, de (443 GPa). La dureza del osmio es moderadamente alta, con un valor de 4 GPa. Debido a su dureza y fragilidad, presenta una baja presión de vapor (la más baja de los metales del grupo del platino) y un punto de fusión muy alto (el tercero más alto de todos los elementos, después del wolframio y del renio). El osmio sólido es difícil de mecanizar para darle forma.
Propiedades químicas
El osmio forma compuestos con estados de oxidación que van desde −2 a +8. Los estados de oxidación más comunes son +2, +3, +4 y +8. El estado de oxidación +8 es notable por ser el más alto alcanzado por cualquier elemento químico aparte del +9 de iridio y se encuentra solo en xenón, rutenio, hasio, y iridio. Los estados de oxidación −1 y −2 representados por dos compuestos reactivos Na2[Os4(CO)13] y Na2[Os(CO)4] se utilizan en la síntesis clústeres de osmio.
El compuesto más común que exhibe el estado de oxidación +8 es el tetróxido de osmio. Este compuesto tóxico se forma cuando el osmio en polvo se expone al aire. Es un sólido cristalino muy volátil, soluble en agua, amarillo pálido y con un fuerte olor. El polvo de osmio tiene el olor característico del tetróxido de osmio. Este óxido forma osmiatos rojos OsO4(OH)2−2 al reaccionar con una base. Con amoníaco, forma el nitro-osmiato OsO3N−.El tetróxido de osmio hierve a 130° C y es un poderoso agente oxidante. Por el contrario, el dióxido de osmio (OsO2) es negro, no volátil y mucho menos reactivo y tóxico.
Solo dos compuestos de osmio tienen aplicaciones importantes: el tetróxido de osmio para la tinción de tejidos orgánicos en microscopía electrónica y para la oxidación de alquenos en síntesis orgánica, y los osmiatos no volátiles para reacciones de oxidación orgánicas.
Isótopos
El osmio tiene siete isótopos naturales, seis de los cuales son estables: 184Os, 187Os, 188Os, 189Os, 190Os y (el más abundante) 192Os. El 186Os se somete a desintegración alfa con un periodo de semidesintegración muy largo de (2,0±1,1) 1015 años, aproximadamente 140 000 veces la edad del universo, que para fines prácticos puede considerarse estable. Se predice la desintegración alfa para los siete isótopos naturales, pero se ha observado solo para el 186Os, presumiblemente debido a sus vidas medias muy largas. Se predice que el 184Os y el 192Os pueden sufrir doble desintegración beta pero esta radioactividad aún no se ha observado.
El 187Os se deriva del 187Re (4,56 1010 años de semivida) y se usa ampliamente en la datación terrestre y de rocas meteoríticas (véase datado por renio-osmio).
Historia
El osmio fue descubierto en 1803 por Smithson Tennant y William Hyde Wollaston en Londres, Inglaterra. El descubrimiento del osmio está entrelazado con el del platino y los otros metales del grupo del platino. El platino llegó a Europa como platina ("pequeña plata"), habiendo sido encontrado por primera vez a finales del siglo XVII en las minas de plata situadas alrededor de Chocó, en Colombia. El descubrimiento de que este metal no era una aleación, sino un elemento nuevo y distinto, fue publicado en 1748.
Los químicos que estudiaron el platino lo disolvieron en agua regia (una mezcla de ácido clorhídrico y ácido nítrico) para crear sales solubles, y siempre observaban una pequeña cantidad de un residuo oscuro e insoluble. Louis Proust pensó que el residuo era grafito. Hippolyte Victor Collet-Descotils, Antoine-François de Fourcroy y Louis Nicolas Vauquelin también observaron iridio en el residuo de platino negro en 1803, pero no obtuvieron suficiente material para más experimentos. Más tarde, los dos químicos franceses Antoine-François Fourcroy y Nicolas-Louis Vauquelin identificaron un metal en un residuo de platino que llamaron "ptène".
Referencias
1. Mager Stellman, J. (1998). «Osmium». Encyclopaedia of Occupational Health and Safety. International Labour Organization. pp. 63.34. ISBN 978-92-2-109816-4. OCLC 35279504.
2. Haynes, 2011, p. 4.25.

Información general
Nombre: Osmio
Símbolo: Os
Número: 76
Serie Química: Metales de transición
Grupo: 8
Período: 6
Bloque: d
Masa Atómica: 190,23 u
Configuración Electrónica: [Xe] 4f14 5d6 6s2
Dureza Mohs: 7
Electrones por nivel: 2, 8, 18, 32, 14, 2
Propiedades Atómicas
Radio medio: 130 pm
Electronegatividad: 2,2 (escala de Pauling)
Radio atómico (calc): 185 pm (radio de Bohr)
Radio covalente: 128 pm
Estado(s) de oxidación: 8, 7, 6, 5, 4, 3, 2, 1, 0, -1, -2
Óxido: Levemente ácido
1.ª Energía de ionización: 840 kJ/mol
2.ª Energía de ionización: 1600 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 22610 kg/m3
Punto de fusión: 3306 K (3033 °C)
Punto de ebullición: 5285 K (5012 °C)
Entalpía de vaporización: 627,6 kJ/mol
Entalpía de fusión: 31,8 kJ/mol
Presión de vapor: 2,52 Pa a 3300 K
Volumen molar: 8,42·10-6 m3/mol
Módulo de compresibilidad: 462 GPa
Varios
Estructura cristalina: Hexagonal
N.º CAS: 7440-04-2
N.º EINECS: 231-114-0
Calor específico: 130 J/(K·kg)
Conductividad eléctrica: 10,9·106 S/m
Conductividad térmica: 87,6 W/(K·m)
Módulo de cizalladura: 222 GPa
Velocidad del sonido: 4940 m/s a 293,15 K (20 °C)
Isótopos más estables
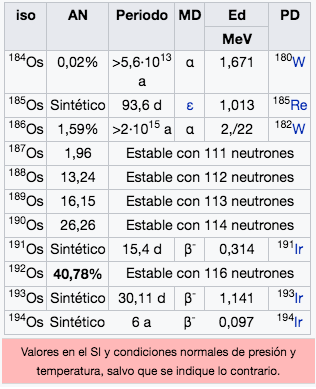
Hassio
El hasio, anteriormente conocido provisionalmente como unniloctio,, es un elemento sintético de la tabla periódica cuyo símbolo es Hs y su número atómico es 108. Su isótopo más estable es el Hs-269, que tiene un periodo de semidesintegración de 9,7 segundos.
Hubo una controversia acerca del nombre de los elementos 101 a 109. Inicialmente la IUPAC adoptó el nombre unniloctio (de símbolo Uno) como un nombre temporal y sistemático para este elemento. En 1994 la IUPAC recomendó el nombre hahnio para el elemento 108, pero finalmente se adoptó internacionalmente el nombre hassio en 1997. En 2017 los organismos de denominación en español eliminaron la secuencia gráfica —ss—, incluso como variante, por ser ajena al sistema ortográfico del español.
Historia
El hasio fue sintetizado por primera vez en 1984 por el grupo de investigación alemán Gesellschaft für Schwerionenforschung localizado en Darmstadt. El nombre hasio propuesto por el grupo se debe al estado alemán de Hesse en el que se encuentra el GSI.
Hubo una controversia acerca del nombre de los elementos 101 a 109. Inicialmente la IUPAC adoptó el nombre unniloctio (de símbolo Uno) como un nombre temporal y sistemático para este elemento. En 1994 la IUPAC recomendó el nombre hahnio para el elemento 108, pero finalmente se adoptó internacionalmente el nombre hassio en 1997. En 2017 los organismos de denominación en español eliminaron la secuencia gráfica —ss—, incluso como variante, por ser ajena al sistema ortográfico del español.
Aplicaciones
Al igual que otros transfermios, su uso es meramente científico.
Referencias
1. Chemical Data. Hassium - Hs, Royal Chemical Society
2. «Nombres y símbolos en español acordados por la RAC, la RAE, la RSEQ y la Fundéu». 1 de marzo de 2017. Consultado el 4 de abril de 2017.
Información general
Nombre: Hassio
Símbolo: Hs
Número: 108
Serie Química: Metales de transición
Grupo: 8
Período: 7
Bloque: d
Masa Atómica: 269 u
Configuración Electrónica: [Rn] 5f14 6d6 7s2 (predicción)
Electrones por nivel: 2, 8, 16, 32, 32, 16, 2 (predicción)
Propiedades Atómicas
Radio covalente: 134 (estimado) pm
Estado(s) de oxidación: 8
Propiedades Físicas
Estado ordinario: Probablemente sólido
Varios
Estructura cristalina: Desconocida
N.º CAS: 54037-57-9
Iridio
El iridio es un elemento químico de número atómico 77 que se sitúa en el grupo 9 de la tabla periódica. Su símbolo es Ir. Se trata de un metal de transición, del grupo del platino, duro, frágil, pesado, de color blanco plateado. Es el segundo elemento más denso (después del osmio) y es el elemento más resistente a la corrosión, incluso a temperaturas tan altas como 2000 °C. Solo algunos halógenos y sales fundidas son corrosivas para el iridio en estado sólido. El iridio en polvo es mucho más reactivo y puede llegar a ser inflamable.
Fue descubierto en 1803 entre las impurezas insolubles del platino natural. Smithson Tennant, el primer descubridor, llamó al metal iridio en honor a la diosa Iris, la personificación del arcoíris, debido a los diversos y llamativos colores de sus sales. El iridio es uno de los elementos más raros en la corteza terrestre, con una extracción y consumo anual de tan solo tres toneladas. El 191Ir y el 193Ir son los dos isótopos naturales del iridio y también sus únicos isótopos estables; el 193Ir es el más abundante de los dos.
Los compuestos de iridio más importantes son las sales y ácidos que forma junto con el cloro, aunque el iridio también forma una serie de compuestos organometálicos, utilizados en la catálisis industrial y en investigación. El iridio metálico es usado cuando se necesita alta resistencia a la corrosión a altas temperaturas, como en las bujías de gama alta, crisoles para la recristalización de los semiconductores a altas temperaturas, y los electrodos para la producción de cloro mediante el proceso de cloro-álcali. Los radioisótopos de iridio se usan en algunos generadores de radioisótopos.
El iridio se encuentra en meteoritos en una abundancia mucho mayor que en la corteza terrestre. Por esta razón, la abundancia inusualmente alta de iridio en la capa de arcilla en el límite Cretáceo-Paleógeno dio lugar a la hipótesis de Álvarez de que el impacto de un objeto extraterrestre masivo causó la extinción de los dinosaurios y muchas otras especies hace 65 millones de años. Del mismo modo, una anomalía de iridio en muestras de núcleos del Océano Pacífico sugirió el impacto Eltanin de hace aproximadamente 2,5 millones de años.
El iridio también se emplea en aleaciones de alta resistencia que pueden soportar altas temperaturas. Es un elemento poco abundante y se encuentra en la naturaleza en aleaciones con platino y osmio. Se emplea en contactos eléctricos, aparatos que trabajan a altas temperaturas, y como agente endurecedor del platino.
Características
Características principales
Es de color blanco, parecido al platino, pero presenta una ligera coloración amarilla. Es difícil trabajar este metal, pues es muy duro y quebradizo. Es el metal más resistente a la corrosión. No es atacado por los ácidos, ni siquiera por el agua regia. Para disolverlo se emplea ácido clorhídrico, HCl, concentrado con clorato de sodio, NaClO3 a temperaturas altas.
El iridio es considerado comúnmente un metal extraterrestre, ya que abunda en los meteoritos y es raro en la corteza terrestre, con solo una pequeña concentración de 0,001 ppm. Es el metal más denso después del osmio. Se sabe que en el núcleo de la Tierra se encuentra este metal junto al hierro y al níquel, sus componentes más importantes.
Propiedades físicas
Pertenece a los metales del grupo del platino. Debido a su dureza, fragilidad y su alto punto de fusión (el noveno más alto de todos los elementos), es difícil dar forma o trabajar sobre el iridio sólido como se haría con otros metales, por lo que se prefiere trabajarlo en forma de polvo metálico. Es el único metal que mantiene buenas propiedades mecánicas por encima de los 1600 °C. El iridio tiene un punto de ebullición muy alto (el décimo entre todos los elementos) y se convierte en superconductor a temperaturas debajo de los 0.14 K.
El módulo de elasticidad del iridio es el segundo más alto de todos los elementos, superado únicamente por el del osmio; esto, junto con un alto módulo de rigidez y un bajo coeficiente de Poisson, indica el alto grado de rigidez y resistencia a la deformación que han hecho que su manipulación sea una cuestión de gran dificultad. A pesar de estas limitaciones y del alto costo del iridio, es muy valioso para aplicaciones donde la resistencia mecánica es un factor esencial y se usa en algunas tecnologías modernas que operan en condiciones extremas.
La densidad medida del iridio es ligeramente inferior (0,1%) a la del osmio, el cual es el elemento más denso conocido. Anteriormente existía una ambigüedad respecto a qué elemento era más denso, debido a la pequeña diferencia de densidades entre estos dos elementos y la dificultad para medir con precisión dicha diferencia. Con la mayor precisión en los factores utilizados para calcular la densidad cristalográfica mediante rayos X se pudieron calcular sus densidades como 22,56 g/cm3 para el iridio y 22,59 g/cm3 para el osmio.
Propiedades químicas
El iridio es el metal más resistente a la corrosión conocido: no es atacado por casi ningún ácido, el aqua regia (aunque si pulverizado), metales fundidos o silicatos a altas temperaturas. Puede, sin embargo, ser atacado por algunas sales fundidas, tales como el cianuro sódico y cianuro potásico, como también por el oxígeno y los halógenos (particularmente el flúor) a altas temperaturas.
Compuestos
El iridio forma compuesto en estados de oxidación entre -3 hasta +6, los más comunes son +3 y +4. Los estados de oxidación mayores son poco comunes, pero incluyen al IrF6 y a dos óxidos mixtos, el Sr2MgIrO6 y el Sr2CaIrO6. El dióxido de iridio, un polvo marrón, es el único óxido de iridio bien caracterizado, un sesquióxido de iridio, el Ir2O3, ha sido descrito como un polvo de color azul-negro el cual se oxida a IrO2 por exposición al HNO3. También se han encontrado compuestos de iridio y Azufre, como el IrS3. El iridio también forma compuestos con estados de oxidación +4 y +5, como K2IrO3 y KIrO3, que puede ser preparado a partir de la reacción del óxido de potasio o del superóxido de potasio con iridio a altas temperaturas. Actualmente no se conocen hidruros binarios de iridio (IrxHy), pero se conocen hidruros complejos como el IrH-45 y IrH-36, donde el iridio posee un número de oxidación +1 y +3 respectivamente. El hidruro ternario Mg6Ir2H11 se cree que contienen tanto el anión IrH-45 como al IrH-36. No se conocen monohaluro o dihaluro de iridio, sin embargo, se conocen trihaluros (IrX3) de iridio con todos los hálogenos. Para estados de oxidación +4 y superiores, únicamente se conocen el tetrafluoruro, el pentafluoruro y el hexafluoruro. El hexafluoruro de iridio, es un sólido amarillo volátil y altamente reactivo, compuesto de moléculas octaédricas. Se descompone en agua y se reduce a IrF4, un sólido cristalino de iridio negro. El pentafluoruro de iridio tiene propiedades similares pero en realidad es un tetrámero, Ir4F20, formado por cuatro octaedros que comparten esquinas.
Isótopos
El iridio tiene dos isotopos naturales estables, el 191Ir y el 193Ir, con una abundancia natural de 37.3% y 62.7%, respectivamente. Al menos 34 radioisótopos han sido sintetizados variando entre números másicos de 164 a 199. El 192Ir, el cual se desintegra en los dos isótopos estables, es el radioisótopo más estable con una semivida de 73.827 días. Otros tres isótopos, el 188Ir, 189Ir, 190Ir, tienen una semivida de al menos un día. Isótopos con número de masa debajo de 191 decaen mediante una combinación de desintegración ß, desintegración α y emisión de protones, con la excepción del 189Ir, que decae por medio de captura electrónica, y el 190Ir, el cual decae por medio de emisión de positrones. Isótopos sintéticos con una masa atómica mayor a 191 decaen mediante desintegración β–, aunque el 192Ir también puede decaer en menor medida mediante captura de electrones. Todos los isotopos conocidos de iridio fueron descubiertos entre 1934 y 2001, el más reciente de ellos es el 171Ir.
Historia
El descubrimiento del iridio data de la misma época en que se descubrió el platino y el resto de metales de su grupo. El platino elemental fue usado por los antiguos etíopes y por las culturas sudamericanas, las cuales siempre tuvieron acceso a una pequeña cantidad de metales del grupo del platino, incluyendo el iridio. El platino llegó a Europa con el nombre de "platina" (pequeña plata), descubierto en el siglo XVII por españoles en la región que hoy se conoce como Departamento de Chocó en Colombia. Pero el descubrimiento de que este metal era un elemento nuevo y no una aleación de elemento conocidos no se produjo hasta 1748.
Los químicos que estudiaron el platino encontraron que este se disolvía en aqua regia, creando sales solubles. Estos químicos siempre notaban una pequeña cantidad de un residuo de color oscuro insoluble. Joseph Louis Proust pensó que este residuo se debía a grafito. Los químicos franceses Victor Collet-Descotils, Antoine François, el conde de Fourcroy, y Louis Nicolas Vauquelin también observaron el residuo oscuro en 1803, sin embargo, no obtuvieron suficiente como para realizar experimentos. Ese mismo año un científico británico, Smithson Tennant analizó el residuo insoluble y concluyó que este debía de contener un nuevo metal. Vauquelin expuso el residuo en polvo a álcalis y ácidos y obtuvo un nuevo óxido volátil, el cual él creía que se trataba del nuevo metal que llamó "ptene", que provenía de la palabra griega πτηνος (ptènos) y significaba "Alado". Tennant, que contaba con una cantidad mucho más grande del residuo, continuó su investigación e identificó dos nuevos elementos dentro del residuo negro, el iridio y el osmio. Obtuvo cristales de color rojo oscuro (probablemente de Na2[IrCl6]•nH2O)por una serie de reacciones con hidróxido de sodio y ácido clorhídrico. Llamó a uno de los elemento iridio en honor a la diosa griega Iris, debido a los colores de sus sales. El descubrimiento de los nuevos elementos fue documentado en una carta a la Royal Society el 21 de junio de 1804.
El científico británico John George Children fue el primero en fundir una muestra de iridio en 1813 con la ayuda de la "mejor batería galvánica que jamás se haya construido" (hasta esa época).
El primero en obtener iridio puro fue Robert Hare en 1842. Encontró que la densidad del iridio rondaba los 21.8 g/cm3 y notó que el metal no era maleable y era extremadamente duro.
La primera fundición de una cantidad significativa del metal fue realizada por Henri Sainte-Claire Deville y Jules Henri Debray en 1860. Para fundir el metal, se necesitó más de 300 litros de O2 puro y H2 por cada kilogramo de iridio. Estas dificultades extremas para fundir el metal han limitado las posibilidades de manejar el iridio.
Referencias
1. J. W. Arblaster: Densities of Osmium and Iridium, in: Platinum Metals Review, 1989, 33, 1, S. 14–16; Volltext
2. «Metales: Propiedades químicas y toxicidad, Iridio, revisado el 3 de septiembre de 2011». Archivado desde el original el 24 de septiembre de 2015. Consultado el 4 de septiembre de 2011.
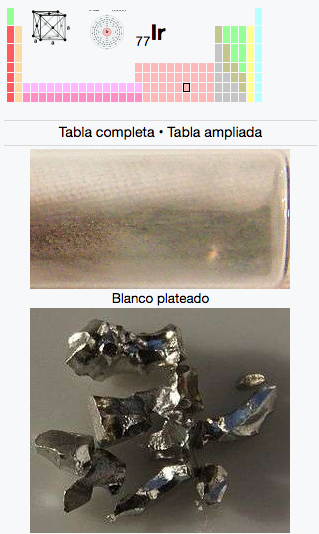
Información general
Nombre: Iridio
Símbolo: Ir
Número: 77
Serie Química: Metales de transición
Grupo: 9
Período: 6
Bloque: d
Masa Atómica: 192,217 u
Configuración Electrónica: [Xe] 4f14 5d7 6s2
Electrones por nivel: 2, 8, 18, 32, 15, 2
Propiedades Atómicas
Electronegatividad: 2,20 (escala de Pauling)
Radio atómico (calc): 136 pm (radio de Bohr)
Radio covalente: 141±6 pm
Estado(s) de oxidación: −3,−1, 0, 1, 2, 3, 4, 5, 6, 9
1.ª Energía de ionización: 880 kJ/mol
2.ª Energía de ionización: 1600 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 22560 kg/m3
Punto de fusión: 2739 K (2466 °C)
Punto de ebullición: 4701 K (4428 °C)
Entalpía de vaporización: 563 kJ/mol
Entalpía de fusión: 41,12 kJ/mol
Varios
Estructura cristalina: Cúbica centrada en las caras
N.º CAS: 7439-88-5
Conductividad térmica: 147 W/(K·m)
Módulo elástico: 528 GPa
Velocidad del sonido: 4825 m/s a 293,15 K (20 °C)
Isótopos más estables
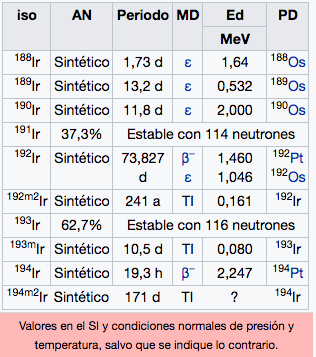
Platino
El platino es un elemento químico de número atómico 78, situado en el grupo 10 de la tabla periódica de los elementos. Su símbolo es Pt. Se trata de un metal de transición blanco grisáceo, precioso, pesado, maleable y dúctil. Es resistente a la corrosión y se encuentra en distintos minerales, frecuentemente junto con níquel y cobre. Se emplea en joyería, equipamiento de laboratorio, contactos eléctricos, empastes y catalizadores de automóviles.
Características principales
El platino es relativamente resistente al ataque químico, tiene buenas propiedades físicas a temperaturas altas, y también buenas propiedades eléctricas. Esto ha hecho que se utilice en distintas aplicaciones industriales. Cuando está puro, es de color blanco grisáceo, maleable y dúctil. Es resistente a la corrosión y no se disuelve en la mayoría de los ácidos, aunque es posible disolverlo usando agua regia.
Aplicaciones
El platino se utiliza en múltiples y esenciales aplicaciones, mientras que nuevos usos para el platino se desarrollan constantemente.
- Joyería
- Catalizadores para vehículos
- Eléctrica y electrónica
- Química
- Vidrio
- Petróleo
- Bujías
Obtención
Actualmente, Sudáfrica cuenta con las reservas de platino más grandes del mundo (más del 70% del total mundial), por lo que se ha convertido en su mayor productor y exportador. Rusia y Canadá cuentan con modestas reservas de este metal, y Estados Unidos cuenta con una producción mínima a pesar de sus yacimientos (casi la mitad de los yacimientos canadienses). Solo entre Sudáfrica y Rusia se genera el 90% de la producción mundial de platino.
Referencias

Información general
Nombre: Platino
Símbolo: Pt
Número: 78
Serie Química: Metales de Transición
Grupo: 10
Período: 6
Bloque: d
Masa Atómica: 195.084 u
Configuración Electrónica: [Xe]4f145d96s1
Electrones por Nivel: 2, 8, 18, 32, 17, 1
Propiedades Atómicas
Electronegatividad: 2.28 (escala de Pauling)
Radio Atómico (calc): 139 pm (radio de Bohr)
Radio Covalente: 136 pm
Estado(s) de oxidación: 6, 5, 4, 3, 2, 1, -1, -2
1.ª Energía de ionización: 870 kJ/mol
2.ª Energía de ionización: 1791 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 21450 kg/m3
Punto de fusión: 2042.15 K (700 °C)
Punto de ebullición: 4098 K (1737 °C)
Entalpía de fusión: 22.17 kJ/mol
Presión de vapor: 0.0312
Varios
Estructura cristalina: Cúbica centrada en las caras
Calor Específico: 130 J/(K·kg)
Conductividad Térmica: 71.6 W/(K·m)
Isótopos más estables
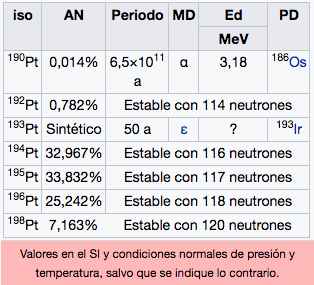
Oro
Es un metal precioso blando de color dorado. Es uno de los metales más apreciados en joyería por sus propiedades físicas, al tener baja alterabilidad, ser muy maleable, dúctil y brillante, y valorado por su rareza, al ser un metal difícil de encontrar en la naturaleza.
Características principales
El oro exhibe un color amarillo en bruto. Es considerado como el metal más maleable y dúctil que se conoce. Además, es un buen conductor del calor y de la electricidad, y no le afecta el aire ni la mayoría de los agentes químicos. Tiene una alta resistencia a la alteración química por parte del calor, la humedad y la mayoría de los agentes corrosivos, y así está bien adaptado a su uso en la acuñación de monedas y en la joyería.
Aplicaciones
De la producción mundial de oro el 70 % se utiliza en joyería, el 20 % en reservas e inversiones y solo al 10 % se le da usos industriales. El oro puro o de 24 kt (quilates) es demasiado blando para ser usado normalmente y se endurece aleándolo con plata y/o cobre, con lo cual podrá tener distintos tonos de color o matices.
- Medicina
- Oro como valor especulativo
- El oro ejerce funciones críticas en comunicaciones, naves espaciales, motores de aviones de reacción y otros muchos productos.
- Su alta conductividad eléctrica y su resistencia a la oxidación han permitido un amplio uso como capas delgadas electrodepositadas sobre la superficie de conexiones eléctricas para asegurar una conexión buena, de baja resistencia.
Obtención
Debido a que es relativamente inerte, se suele encontrar como metal, a veces como pepitas grandes, pero generalmente se encuentra en pequeñas inclusiones en algunos minerales, vetas de cuarzo, pizarra, rocas metamórficas y depósitos aluviales originados de estas fuentes. El oro está ampliamente distribuido y a menudo se encuentra asociado a los minerales cuarzo y pirita, y se combina con teluro en los minerales calaverita, silvanita y otros. Los romanos extraían mucho oro de las minas españolas, pero hoy en día muchas de las minas de este país están agotadas.
El oro puede encontrarse en la naturaleza en los ríos. Algunas piedras de los ríos contienen pepitas de oro en su interior. La fuerza del agua separa las pepitas de la roca y las divide en partículas minúsculas que se depositan en el fondo del cauce.
Los buscadores de oro localizan estas partículas de oro de los ríos mediante la técnica del bateo. El utensilio utilizado es la batea, un recipiente con forma de sartén. La batea se llena con arena y agua del río y se va moviendo provocando que los materiales de mayor peso, como el oro, sean depositados en el fondo y la arena superficial se desprenda.
Referencias
1. U.S. Geological Survey (Mineral Commodity Summaries). 2021. Oro
2. Origen del Oro en la Tierra.

Información general
Nombre: Oro
Símbolo: Au
Número: 79
Serie Química: Metales de Transición
Grupo: 11
Período: 6
Bloque: d
Masa Atómica: 196.9666 u
Configuración Electrónica: [Xe]4f145d106s1
Electrones por Nivel: 2, 8, 18, 32, 18, 1
Propiedades Atómicas
Electronegatividad: 2.54 (escala de Pauling)
Radio Atómico (calc): 174 pm (radio de Bohr)
Radio Covalente: 144 pm
Estado(s) de oxidación: 3, 1
1.ª Energía de ionización: 890.1 kJ/mol
2.ª Energía de ionización: 1980 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 19300 kg/m3
Punto de fusión: 1337.33 K (700 °C)
Punto de ebullición: 3129 K (1737 °C)
Entalpía de fusión: 12.55 kJ/mol
Presión de vapor: 0.000237
Varios
Estructura cristalina: Cúbica centrada en las caras
Calor Específico: 128 J/(K·kg)
Conductividad Térmica: 317 W/(K·m)
Isótopos más estables
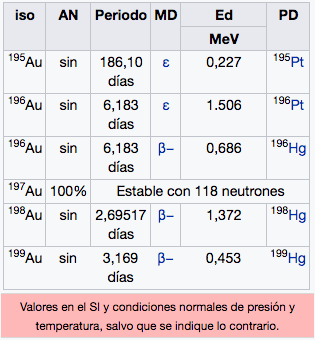
Mercurio
El mercurio es un elemento químico con el símbolo Hg y número atómico 80. En la literatura antigua era designado comúnmente como plata líquida y también como azogue o hidrargiro.
Características principales
El mercurio es un metal pesado plateado que a temperatura ambiente es un líquido inodoro. No es buen conductor del calor comparado con otros metales, aunque es buen conductor de la electricidad. Se alea fácilmente con muchos otros metales como el oro o la plata produciendo amalgamas, pero no con el hierro. Es insoluble en agua y soluble en ácido nítrico. Cuando aumenta su temperatura, produce vapores tóxicos y corrosivos, más pesados que el aire por lo que se evapora creando miles de partículas en el vapor que al enfriarse se depositan de nuevo. Es dañino por inhalación, ingestión y contacto: se trata de un producto muy irritante para la piel, ojos y vías respiratorias. Es incompatible con el ácido nítrico concentrado, el acetileno, el amoníaco, el cloro y los metales.
Aplicaciones
El mercurio se utiliza principalmente para la fabricación de productos químicos industriales o para aplicaciones eléctricas y se emplea en algunos termómetros, especialmente los que se usan para medir temperaturas elevadas. Una cantidad cada vez mayor se usa como mercurio gaseoso en lámparas fluorescentes, mientras que la mayoría de las otras aplicaciones se están eliminando lentamente debido a las regulaciones de salud y seguridad, siendo reemplazado en algunas aplicaciones por materiales menos tóxicos, pero considerablemente más caros, como la aleación Galinstano.
- Medicina
- Producción de cloro y sosa cáustica
- Uso en equipos de laboratorio
- Cosméticos
Obtención
El mercurio es un elemento extremadamente raro en la corteza terrestre, que tiene una abundancia media en peso de tan solo 0,08 partes por millón. Debido a la alta toxicidad del mercurio, tanto la extracción como el refinado del mercurio son causas peligrosas e históricas de envenenamiento.
Referencias
1. El mercurio sintetizado
2. Hand Book of Chemistry
3. El mercurio y el medio ambiente
Información general
Nombre: Mercurio
Símbolo: Hg
Número: 80
Serie Química: Metales de Transición
Grupo: 12
Período: 6
Bloque: d
Masa Atómica: 200.59 u
Configuración Electrónica: [Xe]4f145d106s2
Electrones por Nivel: 2, 8, 18, 32, 18, 2
Propiedades Atómicas
Electronegatividad: 2.00 (escala de Pauling)
Radio Atómico (calc): 171 pm (radio de Bohr)
Radio Covalente: 149 pm
Estado(s) de oxidación: 4, 2, 1
1.ª Energía de ionización: 1007.1 kJ/mol
2.ª Energía de ionización: 1810 kJ/mol
Propiedades Físicas
Estado Ordinario: Liquido
Densidad: 13534 kg/m3
Punto de fusión: 234.32 K (700 °C)
Punto de ebullición: 629.88 K (1737 °C)
Entalpía de fusión: 2.295 kJ/mol
Presión de vapor: 0.0002
Varios
Estructura cristalina: Romboédrica
Calor Específico: 140 J/(K·kg)
Conductividad Térmica: 8.34 W/(K·m)
Isótopos más estables
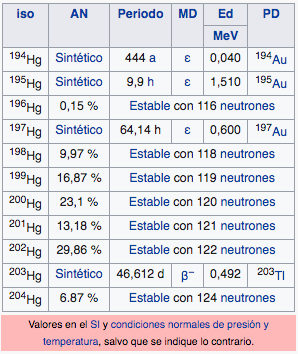
Meitnerio
El meitnerio (anteriormente llamado unnilenio con símbolo provisional Une o Wolschakio con símbolo Wl al no ser oficial) es un elemento químico de la tabla periódica cuyo símbolo es Mt y su número atómico es 109. Es un elemento sintético cuyo isótopo más estable es el 278Mt, cuya vida media es de 7,6 s.
Historia
El meitnerio fue encontrado por accidente en 1982 por Peter Armbruster y Gottfried Münzenberg en el Instituto de Investigación de iones Pesados (Gesellschaft für Schwerionenforschung) en Darmstadt.
El equipo lo consiguió bombardeando bismuto-209 con núcleos acelerados de hierro-58. La creación de este elemento demostró que las técnicas de fusión nuclear podían ser usadas para crear nuevos núcleos pesados.
El nombre de meitnerio fue sugerido en honor a la matemática y física, de origen austríaco y sueco, Lise Meitner, pero había una controversia acerca de los nombres de los elementos comprendidos entre 101 y 109; así pues, la IUPAC adoptó el nombre de unnilennio (símbolo Une) de manera temporal, como nombre sistemático del elemento. En 1997, decidieron la disputa y adoptaron el nombre actual.
Aplicaciones
Al igual que otros transfermios, su uso es meramente científico.
Referencias
1. Chemical Data. Meitnerium - Mt, Royal Chemical Society
2. «wolschakio – El Enciclopedista». Consultado el 13 de febrero de 2019.
Información general
Nombre: Meitnerio
Símbolo: Mt
Número: 109
Serie Química: Metales de transición
Grupo: 9
Período: 7
Bloque: d
Masa Atómica: 268 u
Configuración Electrónica: [Rn] 7s2 5f14 6d7
Electrones por nivel: 2, 8, 18, 32, 32, 15, 2 (predicción)
Propiedades Atómicas
Radio covalente: 129 (estimado) pm
Estado(s) de oxidación: 3, 4, 6 (suposición basada en el iridio)
Propiedades Físicas
Estado ordinario: Probablemente sólido
Varios
Estructura cristalina: Cúbica centrada en las caras
N.º CAS: 54038-01-6
Isótopos más estables
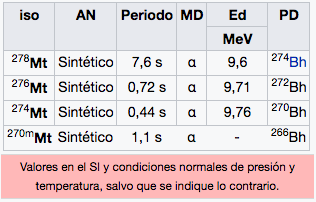
Darmstatio
El darmstatio (anteriormente llamado ununnilio, con símbolo provisional Uun; o madveded, madvedevio o medvedio, con símbolo Mv al no ser oficial) es un elemento químico de la tabla periódica cuyo símbolo es Ds y cuyo número atómico es 110, lo cual lo hace uno de los átomos superpesados. Es un elemento sintético que decae rápidamente; sus isótopos de números másicos entre 267 y 273 tienen periodos de semidesintegración del orden de los microsegundos. Sin embargo, isótopos más pesados, de números másicos 279 y 281, sintetizados recientemente, son más estables, con periodos de semidesintegración de 180 milisegundos y 11,1 segundos, respectivamente. Debido a su presencia en el grupo 10, se cree que este elemento puede ser un metal sólido brillante. Recibe su nombre en honor a la ciudad alemana de Darmstadt donde fue descubierto.
Historia
Fue sintetizado por primera vez el miércoles 9 de noviembre de 1994 en la Gesellschaft für Schwerionenforschung en Darmstadt, Alemania, por P. Armbruster, S. Hofmann, G. Münzenberg y otros. Nunca ha sido visto y solo unos pocos átomos del mismo han sido creados por el bombardeo de isótopos de plomo (208Pb) con iones acelerados de níquel (62Ni, 311 MeV), en un acelerador de iones pesados. El elemento fue nombrado en honor al lugar donde fue descubierto, Darmstadt, por la IUPAC en agosto de 2003.
Referencias
1. «UNUNNILIO». Etimologías de Chile - Diccionario que explica el origen de las palabras. Consultado el 13 de febrero de 2019.
2. Chemical Data. Darmstadtium - Ds, Royal Chemical Society
Información general
Nombre: Darmstatio
Símbolo: Ds
Número: 110
Serie Química: Metales de transición
Grupo: 10
Período: 7
Bloque: d
Masa Atómica: 281 u
Configuración Electrónica: [Rn] 7s2 5f14 6d8
Electrones por nivel: 2, 8, 18, 32, 32, 16, 2 (predicción)
Propiedades Atómicas
Radio covalente: 128 (estimado) pm
Estado(s) de oxidación: 6
Propiedades Físicas
Estado ordinario: Probablemente sólido
Varios
Estructura cristalina: Desconocida
Isótopos más estables
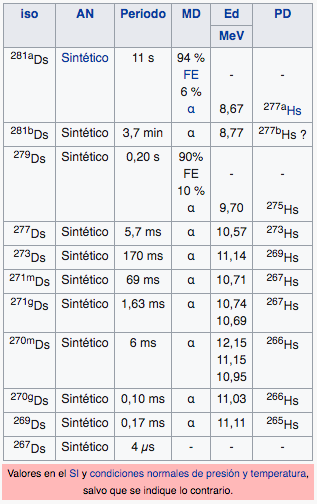
Roentgenio
El roentgenio (anteriormente llamado Unununio o Ununio, Uuu) es un elemento químico del grupo 11 de la tabla periódica cuyo símbolo es Rg y su número atómico es 111.5
Fue descubierto en 1994 por científicos alemanes en Darmstadt. En noviembre de 2004 recibió el nombre de roentgenio en honor a Wilhelm Conrad Roentgen (1845-1923), premio Nobel de Física, descubridor de los rayos X. El roentgenio se obtiene a través del bombardeo de hojas de bismuto (Bi) con iones de níquel (Ni), decayendo en 15 milisegundos.
Aplicaciones
Al igual que otros transfermios, su uso es meramente científico.
Referencias
1. Turler, A. (2004). «Gas Phase Chemistry of Superheavy Elements». Journal of Nuclear and Radiochemical Sciences 5 (2): R19-R25. Archivado desde el original el 11 de junio de 2011.
2. Chemical Data. Roentgenium - Rg, Royal Chemical Society
Información general
Nombre: Roentgenio
Símbolo: Rg
Número: 111
Serie Química: Metales de transición
Grupo: 11
Período: 9
Bloque: d
Masa Atómica: 281 u
Configuración Electrónica: [Rn] 5f14 6d10 7s1
Electrones por nivel: 2, 8, 18, 32, 32, 17, 2 (predicción)
Propiedades Atómicas
Radio covalente: 121 (estimado) pm
Estado(s) de oxidación: -1, +1, +3, +5
Propiedades Físicas
Estado ordinario: Desconocido
Varios
N.º CAS: 54386-24-2
Isótopos más estables
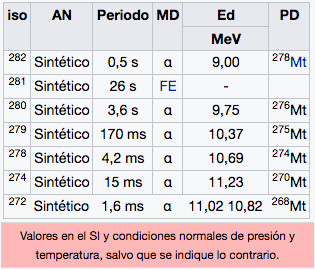
Copernicio
El copernicio (anteriormente llamado Ununbio, con el símbolo provisional Uub) es un elemento químico de la tabla periódica cuyo símbolo es Cn y su número atómico 112. Su apariencia física no se conoce aún, pero podría calcularse, sabiendo que por ahora el isótopo conocido, de 285 de masa atómica, tiene una vida media de 0,24 ms.
Nombre
A principios de 2009, la IUPAC (International Union of Pure and Applied Chemistry) confirmó oficialmente el descubrimiento por el laboratorio GSI Helmholtzzentrum für Schwerionenforschung (Centro de investigación de Iones Pesados) en Darmstadt. En julio de 2009 el grupo del profesor Sigurd Hofmann propuso el nombre Copernicio y el símbolo Cp en honor del científico y astrónomo Nicolás Copérnico (1473-1543). Tras la propuesta pasan seis meses hasta que la IUPAC hace oficial el nombre, con el fin de dejar ese tiempo para que la comunidad científica discuta el nombre sugerido, antes de otorgar el nombre oficial. No obstante, se cambió el posible símbolo Cp, por Cn, ya que el símbolo estaba antiguamente asociado al cassiopium (cuyo nombre oficial es lutecio [Lu]); y, además, en química orgánica ya existe el símbolo Cp, que indica el ciclopentadieno. Por tanto, el 19 de febrero de 2010 la IUPAC expuso oficialmente la denominación y el símbolo del elemento 112.
Historia
Científicos alemanes han conseguido que finalmente se incluya el elemento número 112 en la tabla periódica. Se trata de un elemento químico superpesado que, en ese entonces, a falta de un nombre (tienen el privilegio de elegirlo), se llamaba unumbio, que en latín significa «uno uno dos». Este elemento, que en realidad fue descubierto en 1996, ve así confirmada su existencia, aunque sólo han conseguido producir literalmente cuatro átomos de él.
Este elemento es 277 veces más pesado que el hidrógeno y tiene el récord de ser uno de los más pesados de la tabla periódica. Este mismo equipo lleva desde 1981 produciendo nuevos elementos, ya lo hizo con los numerados entre 107 y 111.
El último elemento natural de la tabla periódica fue descubierto en 1925; desde entonces todos los demás han sido, como el 112, creados en laboratorio.
Aplicaciones
Al igual que otros elementos, su uso es meramente científico. Pero al ser muy pesado, puede tener más aplicaciones no descubiertas todavía.
Referencias
1. Chart of Nuclides. Brookhaven National Laboratory
2. Chemical Data. Copernicium - Cn, Royal Chemical Society
Información general
Nombre: Copernicio
Símbolo: Cn
Número: 112
Serie Química: Metales de transición
Grupo: 12
Período: 7
Bloque: d
Masa Atómica: 285 u
Configuración Electrónica: [Rn] 5f14 6d10 7s2
Electrones por nivel: 2, 8, 18, 32, 32, 18, 2 (supuesto)
Propiedades Atómicas
Radio covalente: 122 (predicción) pm
Estado(s) de oxidación: 4, 2 un supuesto basado en el Mercurio
Propiedades Físicas
Densidad: Desconocido
Varios
N.º CAS: 54084-26-3
Isótopos más estables
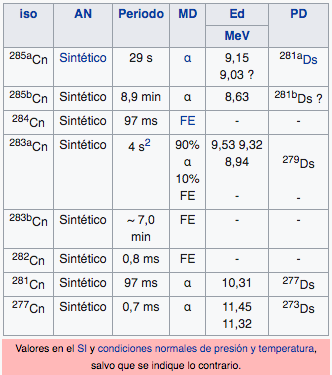
Nihonio
El nihonio o nihomio (anteriormente llamado ununtrio, con el símbolo provisional Uut hasta su aceptación oficial como nuevo elemento por la IUPAC en noviembre de 2016 o Tusfrano con símbolo Tf y erróneamente Trustano) es el nombre para el elemento sintético de la tabla periódica cuyo símbolo es Nh y su número atómico es 113.
Su descubrimiento ha sido adjudicado de forma oficial a los investigadores japoneses del laboratorio Riken, que lograron sintetizar y observar el elemento a finales de 2015, convirtiéndose así en el primer elemento sintético en ser producido en Japón, como resultado de la desintegración del elemento 115 (moscovio). Su nombre proviene de la palabra "Nihon", el término utilizado para designar a Japón. Es un elemento radiactivo cuyo isótopo más estable conocido, nihonio-286, tiene una vida media de 20 segundos.
En la tabla periódica, es un elemento transactínido del bloque p, y es miembro del séptimo período dentro del grupo del boro, aunque no se realizó ningún experimento químico que haya confirmado que este se comporte como el homólogo más pesado que el talio dentro de este grupo. Se cree que el nihonio tenga algunas propiedades similares a la de sus homólogos más livianos, es decir, boro, aluminio, galio, indio y talio, aunque también debería mostrar varias diferencias con estos. A diferencia de otros elementos del bloque p, se prevé que muestre algunas características de metales de transición.
Historia
Su descubrimiento fue reclamado conjuntamente por un equipo de científicos en el Laboratorio Nacional Lawrence Livermore en los Estados Unidos y un grupo de Dubna, Rusia, entre el 2003 y el 2004, así como por los investigadores japoneses en el laboratorio Riken, que lograron sintetizar y observar el elemento, convirtiéndose así en el primer elemento sintético en ser producido en Japón.
La Unión Internacional de Química Pura y Aplicada (IUPAC) denominó temporalmente al elemento como Ununtrium. Este nombre no es más que una identificación sistemática que se le da a los nuevos elementos, siguiendo un procedimiento utilizado por la IUPAC, que identifica los elementos sin nombre por su número atómico: (“ununtri”) significa (“un un tres”), con la terminación (“ium”), un sufijo estándar para los elementos químicos en inglés.
Los investigadores del Centro RIKEN Nishina —Center for Accelerator-based Science, (RNC)— lograron generar una cadena de seis desintegraciones alfa consecutivas, producidas en los experimentos realizados en la fábrica de radioisótopos RIKEN —Radioisotope Beam Factory (RIBF)—, identificado de manera concluyente el elemento 113 a través de las desintegraciones a nucleidos hijos bien conocidos. El resultado, publicado en la revista Journal of Physical Society de Japón, fue el primer paso para reclamar los derechos del nombre del elemento 113 para Japón.
El elemento 113 se sintetizó en Japón a finales de 2015.
El logro del descubrimiento del nihonio se ha atribuido oficialmente al RIKEN Nishina Center for Accelerator-Based Science de Japón.
Denominación
El elemento recibió oficialmente el nombre en inglés de nihonium (traducido al español como nihonio según una recomendación de la FUNDEU) mediante una comunicación de la IUPAC del 28 de noviembre de 2016.
El nombre "nihonium" proviene de la palabra japonesa para «Japón» (日本 Nihon?), en un claro homenaje al país donde ha sido descubierto.
De acuerdo a la nomenclatura de Mendeleyev para elementos innominados y aún no descubiertos, debería haberse denominado eka-talio o dvi-indio. Sin embargo, según las recomendaciones de la IUPAC publicadas en 1979, el elemento se denominó provisionalmente ununtrio (con el símbolo correspondiente Uut), un nombre sistemático del elemento con el que se pudo identificarlo, hasta que el descubrimiento del elemento fue confirmado, recibiendo su nombre oficial definitivo de nihonio. No obstante, estas recomendaciones fueron ignoradas en algunos medios científicos, donde se designaba como elemento 113, con el símbolo (113), o simplemente 113.
Aplicaciones
Por su vida media tan reducida de tan solo milisegundos a minutos y su inestabilidad son nulas las aplicaciones industriales o comerciales de este elemento superpesado, por lo que su aplicación se relega solo a la investigación científica.
Referencias
1. Seaborg (ca. 2006). «transuranium element (chemical element)». Encyclopædia Britannica. Consultado el 16 de marzo de 2010.
2. Chemical Data. Ununtrium - Uut, Royal Chemical Society
Información general
Nombre: Nihonio
Símbolo: Nh
Número: 113
Serie Química: Metales del bloque p
Grupo: 13
Período: 7
Bloque: p
Masa Atómica: 286 u
Configuración Electrónica: [Rn] 5f14 6d10 7p1 (predicción)
Electrones por nivel: 2, 8, 18, 32, 32, 18, 3 (predicción)
Propiedades Atómicas
Radio covalente: 136 (predicción) pm
Estado(s) de oxidación: 1, 3, 5 (predicción)
1.ª energía de ionización: 710 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido (predicción)
Densidad: 16 (predicción) kg/m3
Punto de fusión: 700 K (427 °C)
Punto de ebullición: 1400 K (1127 °C)
Entalpía de vaporización: 130 kJ/mol
Varios
N.º CAS: 54084-70-7
Isótopos más estables
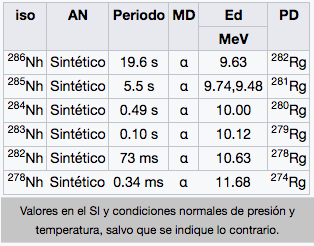
Flerovio
Flerovio (anteriormente llamado ununquadio, Uuq ó erristeneo, erristenio, Eo) es el nombre de un elemento químico radiactivo con el símbolo Fl y número atómico 114. Nombrado en honor a Gueorgui Fliórov.
Hasta la fecha se han observado alrededor de 80 desintegraciones de átomos de flerovio, 50 de ellas directamente y 30 de la desintegración de los elementos más pesados livermorio y oganesón. Todas las desintegraciones han sido asignadas a los cuatro isótopos vecinos con números de masa 286-289. El isótopo de más larga vida conocido actualmente es el 289Fl114 con una vida media de aproximadamente 2,6 s, aunque hay evidencias de un isómero, 289bFl114, con una vida media de aproximadamente 66 s, que sería uno de los núcleos más longevos en la región de los elementos superpesados.
Experimentos químicos muy recientes han indicado fuertemente que el elemento 114 no posee propiedades 'eka'-plomo y parece comportarse como el primer elemento superpesado, que presenta propiedades similares a los gases nobles debido a efectos relativistas.
Historia
Descubrimiento del elemento
En diciembre de 1998, científicos del Instituto Conjunto para la Investigación Nuclear de Dubná en Rusia, bombardearon un blanco de Pu-244 con iones de Ca-48. Se produjo un solo átomo del elemento 114, asignado al isótopo 289Uuq114, que se desintegró mediante emisión alfa de 9,67 MeV, con un tiempo de vida medio de 30 s. Esta observación fue posteriormente publicada en enero de 1999. Sin embargo, la cadena de desintegración observado no se ha repetido y la identidad exacta de esta actividad es desconocida, aunque es posible que sea debida a un isómero meta-estable, llamado, 289mFl114.
En marzo de 1999, el mismo equipo reemplazó el blanco de Pu-244 con uno de Pu-242 a fin de producir otros isótopos. En esta ocasión se produjeron dos átomos del elemento 114, que se desintegraron por emisión alfa de 10.29 MeV con una vida media de 5.5 s. Fueron asignados como 287Uuq114. Una vez más, esta actividad no se ha observado de nuevo y no está claro qué núcleo se produjo. Es posible que se tratara de un isómero meta-estable, llamado 287mUuq114.
El descubrimiento ahora confirmado del elemento 114 se realizó en junio de 1999, cuando el equipo de Dubná repitió la reacción del Pu-244. Esta vez se produjeron dos átomos del elemento 114 que se desintegraron por emisión de partículas alfa de 9,82 MeV, con una vida media de 2,6 s.
Esta actividad fue inicialmente asignada erróneamente al 288Uuq114, debido a la confusión en cuanto a las anteriores observaciones. Nuevos trabajos en diciembre de 2002, permitieron una reasignación positiva al 289Fl114,
244Pu94 + 48Ca20 → 292Fl 114* → 289Fl114 + 3 1n0
En mayo de 2009, el Joint Working Party (JWP) de la IUPAC publicó un informe sobre el descubrimiento del elemento 112 copernicio en el que se reconoció el descubrimiento del isótopo 283Cn112. Esto implica el descubrimiento de facto del elemento 114, del reconocimiento de los datos para la síntesis de 287Uuq114 y 291Uuh116 (ver abajo), relacionada con 283Cn112, aunque esto no puede determinarse como la primera síntesis del elemento. Un informe inminente de la JWP discutirá estos temas.
El descubrimiento del elemento 114, como 287Uuq114 y 286Uuq114, fue confirmado en enero de 2009 en Berkeley. Esto fue seguido de la confirmación del 288Uuq114 y 289Uuq114 en julio de 2009 en el GSI (ver sección 2.1.3).
Nombres
Ununquadio (Uuq) es un nombre de elemento sistemático IUPAC temporal. Los investigadores por lo general se refieren al elemento simplemente como elemento 114.
Según recomendaciones de la IUPAC, el descubridor de un nuevo elemento tiene derecho a sugerir un nombre. El 8 de diciembre de 2011 se le puso el nombre de Flerovio en honor a Gueorgui Fliórov.
Experimentos actuales
En abril de 2009, el Instituto de Paul Scherrer (PSI) en colaboración con el Laboratorio Fliórov de Reacciones Nucleares (FLNR) del Instituto Conjunto para la Investigación Nuclear realizaron otro estudio de la química del elemento 114. Los resultados no están aún disponibles.
Propiedades químicas
Estados de oxidación
Por su vida media tan reducida de tan solo milisegundos a minutos y su inestabilidad son nulas las aplicaciones industriales o comerciales de este elemento superpesado, por lo que su aplicación se relega solo a la investigación científica.
Química
Elemento 114 debería presentar las propiedades químicas del eka-plomo y, por tanto, podría formar un monóxido, UuqO, y dihaluros, UuqF2, UuqCl2, UuqBr2, y UuqI2. Si el estado +IV + es accesible, es probable que sólo sea posible en el óxido, UuqO2, y el fluoruro, UuqF4. También puede mostrar una mezcla de óxidos, Uuq3O4 análoga a Pb3O4.
Algunos estudios también sugieren que el comportamiento químico del elemento 114 pudiera, de hecho, estar más cercano al del gas noble radón, que al del plomo.
Referencias
1. Seaborg (ca. 2006). «transuranium element (chemical element)». Encyclopædia Britannica. Consultado el 16 de marzo de 2010.
2. Chemical Data. Ununquadium - Uuq, Royal Chemical Society
Información general
Nombre: Flerovio
Símbolo: Fl
Número: 114
Serie Química: Metales del bloque p
Grupo: 14
Período: 7
Bloque: p
Masa Atómica: 287 u
Configuración Electrónica: [Rn] 5f14 6d10 7s2 7p2 (predicción)
Electrones por nivel: 2, 8, 18, 32, 32, 18, 4 (predicción)
Propiedades Atómicas
Radio covalente: 143 (estimado) pm
Estado(s) de oxidación: 2, 4 (predicción)
1.ª energía de ionización: 820 kJ/mol
2.ª energía de ionización: 1620 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido (predicción)
Densidad: 14 (predicción) kg/m3
Punto de fusión: 340 K (67 °C)
Punto de ebullición: 420 K (147 °C)
Varios
Estructura cristalina: Desconocida
N.º CAS: 54085-16-4
Isótopos más estables
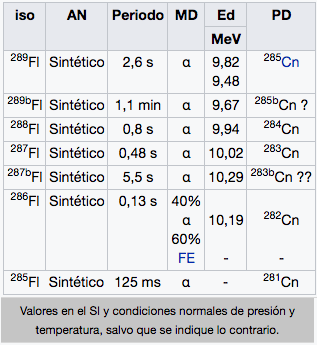
Moscovio
El moscovio (anteriormente llamado unumpentio, Uup, Ununpentio o Merchel [Mc]) es un elemento sintético de la tabla periódica cuyo símbolo es Mc y su número atómico es 115.
Actualmente se conocen cuatro isótopos desde 287Mc hasta 290Mc. Se prevé que el isótopo más estable del moscovio sea el 299Mc, que contiene el número mágico de 184 neutrones. El isótopo con mayor número de neutrones conocido hasta la fecha es el 290Mc, con 175 neutrones. Es muy inestable, con una vida media de milésimas de segundo. Su nombre hace referencia a la provincia de Moscú, región a la que pertenece la ciudad rusa donde se descubrió, Dubná.
Descubrimiento
El 2 de febrero de 2004 se informó en la revista Physical Review C que un equipo integrado por científicos rusos en el Instituto Central de Investigaciones Nucleares en Dubná,y los científicos estadounidenses en el Lawrence Livermore National Laboratory hicieron el descubrimiento del moscovio. El equipo informó que bombardearon americio 243 con calcio 48 para producir iones de cuatro átomos de moscovio. Estos átomos se desintegraron por emisión de partículas alfa en nihonio en aproximadamente 100 milisegundos. En agosto de 2013 otro experimento independiente confirmó el hallazgo del elemento.
Otros elementos químicos sintetizados con anterioridad, como los de números atómicos 111 (roentgenio) y 112 (copernicio), tienen una existencia muy breve, de apenas milésimas de segundo, antes de desintegrarse. Esta característica es muy común entre los elementos transuránicos (los que aparecen en la tabla periódica más allá del uranio, cuyo número atómico es 92). Pero, cuando en 1999 se sintetizó el elemento 114 (flerovio), se comprobó que es mucho más estable de lo que se pensaba: su vida media es de treinta segundos. A raíz de esto, muchos científicos pensaron que estaban a punto de encontrar la isla de estabilidad,es decir, átomos superpesados pero estables durante años. El premio Nobel Glenn Seaborg predijo esta posibilidad en 1991. Calculó que se podría conseguir con algún isótopo de los elementos 114 o 115.
La clave de la estabilidad radica en que el núcleo del átomo sea lo más esférico posible, algo que, según Seaborg, puede ocurrir si posee al menos 298 nucleones (la suma de los protones y los neutrones). En el caso del experimento realizado recientemente por investigadores suizos, dirigidos por el doctor Heinz Gäggeler, la vida del nuevo átomo fue muy breve: una décima de segundo. Pero eso sólo indica que con el proceso empleado (bombardear un disco de americio con un rayo de iones de calcio) se ha obtenido un isótopo del elemento 115 que no llega a alcanzar la tan esquiva estabilidad. En el centro de investigación nuclear de Dubná (Rusia), donde se ha sintetizado el moscovio, varios equipos internacionales llevan años tratando de obtener nuevos elementos químicos. Allí se descubrió también el elemento 114 y, es muy probable que sea en este centro donde se consiga un isótopo estable de este elemento, aunque expertos astrónomos creen podría conseguirse en estado natural en el universo al igual que otros elementos superpesados.
El moscovio en la tabla periódica de los elementos
El 5 de diciembre del 2016 la Unión Internacional de Química Pura y Aplicada (IUPAC) y la Unión Internacional de Física Pura y Aplicada (IUPAP) aprobaron su denominación junto a otros tres elementos como el nihonio, tenesino y oganesón. Además fue agregado a la tabla periódica de los elementos, al igual que los otros tres.
Referencias
1. «Consulta: elementos químicos». Fundéu BBVA. 24 de noviembre de 2016.
2. Chemical Data. Ununpentium - Uup, Royal Chemical Society
Información general
Nombre: Moscovio
Símbolo: Mc
Número: 115
Serie Química: Metales del bloque p
Grupo: 15
Período: 7
Bloque: p
Masa Atómica: 288 u
Configuración Electrónica: [Rn] 5f14 6d10 7s2 7p3 (predicción)
Electrones por nivel: 2, 8, 18, 32, 32, 18, 5 (predicción)
Propiedades Atómicas
Radio covalente: 162 (estimado) pm
Estado(s) de oxidación: 1, 3 (predicción)
Varios
N.º CAS: 54085-64-2
Isótopos más estables
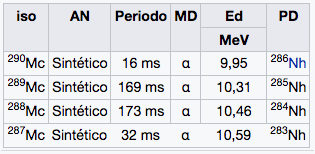
Livermorio
El livermorio (anteriormente llamado ununhexio, Uuh) es el nombre del elemento sintético de la tabla periódica cuyo símbolo es Lv y su número atómico es 116.
Su nombre viene dado en honor al Laboratorio Nacional Lawrence Livermore (Lawrence Livermore National Laboratory), en Livermore, California.
Historia
En 2000, investigadores del Laboratorio Nacional Lawrence Berkeley anunciaron la creación del elemento 116, en un artículo publicado en una revista de los EE. UU. llamada Physical Review Letters, explican que lo hicieron cuando se observó el decaimiento-α de un átomo de mayor número atómico. El año siguiente publicaron su retracción tras ver que no eran capaces de volver a hacer el experimento. En junio de 2002, el director del laboratorio anunció que los datos del experimento habían sido falsificados por su autor principal Victor Ninov.
En junio de 2000, el Instituto Conjunto para la Investigación Nuclear, en la ciudad de Dubna, realizó estudios por los cuales se describió el decaimiento-α del isótopo 292Uuh que se produjo en la reacción de fusión de un núcleo de 248 Cm al ser bombardeado con iones de 48 Ca acelerados por un ciclotrón, como producto secundario se obtuvieron 4 neutrones. Tiene una vida media de cerca de 6 milisegundos (0,006 segundos). Luego de esto tiene un decaimiento-α en 288Fl (Flerovio) seguido de dos más consecutivos en otros átomos de menor número atómico para más tarde tener una fisión espontánea.
Nuevos experimentos se hicieron entre finales de 2000 e inicios de 2001, pero estos fallaron en crear un nuevo átomo.
El 2 de mayo de 2001, el mismo instituto informó sobre la síntesis de un segundo átomo en su cuarta ronda de estudios, y que las propiedades confirmaron una región de la estabilidad "aumentada", aunque son acreditados de gran calidad y cuidadosos la confirmación de estos resultados está todavía pendiente por falta de estudios entre ellos un estudio con rayos X que pruebe la conexión entre las reacciones y descendientes.
En octubre de 2006 se anunció que, en tres ocasiones, bombardeando átomos de californio-249 con iones de calcio-48 producían ununoctio (elemento 118), que posteriormente decaía a ununhexio en tiempos de milisegundos. Confirmando esto, la síntesis del elemento 116 habrá sido demostrada definitivamente.
La reacción que crea el livermorio es:
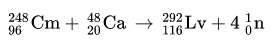
Decae en 47 milisegundos a un isótopo previamente identificado del elemento 114, Fl.
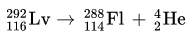
Aplicaciones
Por su inestabilidad, vida media tan reducida y dificultad de obtención, en la actualidad son nulas las aplicaciones industriales, comerciales o propagandísticas de este elemento muy pesado por lo que su aplicación se relega sólo a la investigación científica..
El nombre definitivo del Livermorio
Ununhexio es un nombre temporal IUPAC. Algunos científicos del Joint Institute for Nuclear Research propusieron para este elemento el nombre de "Flyorovium" (Fl) - en honor a G. N. Flyorov, director del grupo que sintetizó los elementos del 102 al 110. Pero no hay ninguna mención que confirme este nombre para el elemento aún.
El 8 de diciembre de 2011, la división de Química Inorgánica de la IUPAC confirmó el nombre y símbolo de este elemento a la vez que el nombre y símbolo del Ununquandio, ahora llamado Flerovio (Fl). El nombre definifivo decidido fue Livermorio (Lv), en honor al Laboratorio Nacional de la ciudad de Livermore, California.
Referencias
1. Oganessian, Yu. Ts.; et al. (2006). «Synthesis of the isotopes of elements 118 and 116 in the 249Cf and 245Cm+48Ca fusion reactions». Physical Review C 74: 044602. doi:10.1103/PhysRevC.74.044602.
2. Chemical Data. Ununhexium - Uuh, Royal Chemical Society
Información general
Nombre: Livermorio
Símbolo: Lv
Número: 116
Serie Química: Metales del bloque p
Grupo: 16
Período: 7
Bloque: p
Masa Atómica: 291 u
Configuración Electrónica: [Rn] 5f14 6d10 7s2 7p4 (predicción)
Electrones por nivel: 2, 8, 18, 32, 32, 18, 6 (predicción)
Propiedades Atómicas
Radio covalente: 175 (estimado) pm
Estado(s) de oxidación: 2, 4 (predicción)
Varios
N.º CAS: 54100-71-9
Isótopos más estables
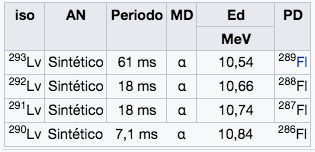
Teneso
El teneso (anteriormente llamado efelio, y símbolo Ef o ununseptio, con el símbolo provisional Uus hasta su aceptación oficial como nuevo elemento por la IUPAC en noviembre de 2016) es un elemento sintético muy pesado de la tabla periódica de los elementos cuyo símbolo es Ts y número atómico 117. También conocido como eka-astato o simplemente elemento 117, es el segundo elemento más pesado creado hasta ahora y el penúltimo del séptimo período en la tabla periódica.
Su descubrimiento se anunció en 2010 y fue fruto de una colaboración entre científicos rusos y estadounidenses en el Instituto Central de Investigaciones Nucleares de Dubná, Rusia. En un experimento en 2011, se creó directamente uno de sus productos de desintegración, confirmando parcialmente los resultados del experimento inicial; el experimento, además, fue repetido con éxito en 2012. En 2014, el Centro GSI Helmholtz para la Investigación de Iones Pesados de Alemania también afirmó haber reproducido el experimento original. El grupo formado por la IUPAC y la IUPAP —IUPAC/IUPAP Joint Working Party—, que se encarga de examinar las reivindicaciones de descubrimientos de elementos superpesados, confirmó el descubrimiento en diciembre de 2015. En junio de 2016, sus descubridores propusieron nombrarlo tennessine (según Tennessee, sede del Laboratorio Nacional Oak Ridge), traducido inicialmente como tenesino o téneso.Finalmente, el 28 de noviembre de 2016, la IUPAC aprobó el nombre propuesto (en inglés), habiendo divergencias en la traducción del nombre al español, hasta que finalmente la Real Academia de Ciencias, la Real Sociedad Española de Química, la RAE y la Fundéu acordaron promover la forma llana teneso.
En la tabla periódica, el teneso está ubicado en el grupo 17, cuyos miembros de número atómico menor son halógenos. Sin embargo, es probable que el teneso tenga propiedades significativamente diferentes de las del resto de elementos del grupo, aunque se prevé que el punto de fusión, el punto de ebullición y la primera energía de ionización sigan las tendencias periódicas. Los isótopos sintetizados hasta ahora son el teneso-293, con una vida media de aproximadamente 14 milisegundos, y teneso-294, con una vida media de alrededor de 78 milisegundos; esto parece confirmar la existencia de la isla de estabilidad. Asimismo, las predicciones teóricas prevén que los isótopos de teneso-309 y superiores sean aún más estables.
Historia
Antes del descubrimiento
En 2004, el equipo del Instituto Central de Investigaciones Nucleares en Dubná (en el óblast de Moscú, Rusia), propuso un experimento para sintetizar el elemento 117 —llamado así por los 117 protones en su núcleo atómico— mediante la fusión nuclear de un blanco de berkelio (elemento 97) con un haz de iones de calcio (elemento 20). El equipo del Laboratorio Nacional Oak Ridge de los Estados Unidos, el único productor de berkelio en el mundo en aquellos días, decidió iniciar la síntesis del material para el blanco en conjunción con la producción de californio para fines comerciales, tan pronto como esta fuera puesta en marcha. Mientras tanto, los planes para sintetizar el elemento 117 fueron dejados de lado temporalmente en favor de la síntesis del elemento 118, producido mediante el bombardeo de un blanco de californio con iones de calcio.
El equipo ruso deseaba usar el isótopo de calcio-48 debido a que tiene veinte protones y veintiocho neutrones; este es el núcleo más ligero con tal exceso de neutrones que es estable o casi estable. La inusual estabilidad de este isótopo de calcio radica en que es «doblemente mágico» debido a que cuenta con «números mágicos» tanto de neutrones como de protones, veintiocho y veinte respectivamente. El siguiente núcleo de semejantes características, zinc-68, es ya mucho más pesado. El haz de iones de calcio fue preparado en Rusia separando químicamente las pequeñas cantidades de calcio-48 presentes en el calcio natural de la tierra. Los núcleos resultantes de la fusión de isótopos ricos en neutrones son más pesados y se encuentran más cerca de la buscada isla de estabilidad.
Descubrimiento
En 2008, el equipo americano inició la producción del blanco de berkelio en el laboratorio de Oak Ridge para el experimento. Tras irradiar curio-244 con partículas alfa durante un total de 250 días, se obtuvieron 22 mg de berkelio, con etapas posteriores de enfriamiento y purificación que sumaron seis meses. El período de semidesintegración del isótopo de berkelio usado (berkelio-249) es de únicamente trescientos treinta días, transcurridos los cuales la mitad de este se transforma en otros elementos, por lo que el equipo determinó un plazo de seis meses a partir de la purificación del blanco para iniciar el experimento, pues más tarde podría no quedar la suficiente cantidad de elemento para llevar a cabo la síntesis del teneso. En el verano boreal de 2009, el berkelio se transportó en un vuelo comercial desde Nueva York a Moscú empaquetado dentro de cinco recipientes de plomo.
La llegada del berkelio a Dubna se retrasó varios días, debido a documentación faltante o incompleta, lo que condujo a que la aduana rusa no permitiera la entrada del material al país y lo devolviera a los Estados Unidos dos veces, hasta que finalmente pudo ingresar a Rusia. Una vez permitida la entrada del «blanco», este se transfirió a Dimitrovgrad, en el óblast de Ulyanovsk, para ser fijado en una película delgada de titanio y luego ser llevada a Dubná, donde fue instalado en el acelerador de partículas del Instituto Central de Investigaciones Nucleares —el más potente del mundo— para la síntesis de elementos superpesados.
El experimento comenzó en junio del 2009 y en enero del 2010 científicos del Laboratorio Flerov de Reacciones Nucleares anunciaron que habían detectado con éxito la desintegración de un nuevo elemento con número atómico 117 a través de dos cadenas de isótopos impar-impar mediante seis desintegraciones alfa antes de una fisión espontánea, y de otro par-impar, con tres desintegraciones alfa antes de la fisión. Según el informe oficial publicado el 9 de abril de 2010 en la revista Physical Review Letters, dichos isótopos eran el teneso-294 y el teneso-293 respectivamente, formados como sigue a continuación:
Antes de la síntesis del teneso, no se conocía ninguno de sus isótopos productos de desintegración; por lo tanto, no había una base para una reclamación del descubrimiento ante el comité de la IUPAC y mucho menos para su reconocimiento. El moscovio-289 —uno de los productos de desintegración del teneso— fue sintetizado de forma directa en 2011 —en lugar de haberse obtenido a partir de la desintegración del teneso—; a pesar de la distinta vía de obtención las propiedades de desintegración medidas en este experimento coincidieron con las del descubrimiento del teneso. Sin embargo, los descubridores no reivindicaron el descubrimiento del teneso cuando el comité encargado estaba revisando los reclamos de descubrimientos de elementos más allá del copernicio. El grupo de Dubna repitió exitosamente el experimento original en 2012, confirmando así la síntesis del teneso. Los científicos presentaron una solicitud para registrar de forma oficial el elemento, y los presidentes de IUPAC y IUPAP formaron un nuevo comité conjunto de trabajo para asignar el derecho de descubrimiento. El 2 de mayo de 2014, científicos del Centro GSI Helmholtz para la Investigación de Iones Pesados, en Darmstadt, aseguraron haber confirmado el descubrimiento del teneso y de un nuevo isótopo: lawrencio-266, obtenido de la desintegración alfa del dubnio-270; este modo de desintegración no fue observado en los experimentos de Dubna, donde el dubnio-270 experimentó una fisión espontánea.
Denominación
Utilizando la nomenclatura de Mendeléyev para los elementos no identificados y sin descubrir, el teneso debería ser conocido como «eka-astato» o «dvi-iodo». En 1979, la IUPAC publicó una serie de recomendaciones para la nomenclatura de elementos de número atómico mayor que 100, que resultaron en el nombre ununseptio y el correspondiente símbolo de Uus, de acuerdo a la denominación sistemática de elementos, como una manera de referirse al elemento de manera temporal, hasta la asignación de un nombre permanente. Conforme a este sistema, el nombre temporal literalmente significa 117 (uno-uno-siete). Las recomendaciones fueron mayoritariamente ignoradas entre los científicos, quienes lo llaman «elemento 117», con el símbolo de «(117)» o incluso simplemente «117».
También llegó a ser llamado o Efelio con cuyo símbolo es Ef.
El descubrimiento del elemento fue confirmado en diciembre de 2015, junto a los elementos 115 y 118, sintetizados por el mismo equipo ruso-estadounidense, y el elemento 113, descubierto por investigadores japoneses. En junio de 2016, sus descubridores propusieron nombrarlo tennessine, con símbolo Ts, que devino la denominación oficial en noviembre de 2016.
Referencias
1. Gramling, Carolyn (8 de junio de 2016). «Four new element names are on the table». Science.
2. «Tennessine - Element information, properties and uses». Periodic Table (en inglés). Royal Chemical Society.
Información general
Nombre: Teneso
Símbolo: Ts
Número: 117
Serie Química: Halógenos
Grupo: 17
Período: 7
Bloque: p
Masa Atómica: 294 u (isótopo más estable)
Configuración Electrónica: [Rn] 5f14 6d10 7s2 7p5 (predicción)
Electrones por nivel: 2, 8, 18, 32, 32, 18, 7 (predicción)
Propiedades Atómicas
Radio covalente: 165 (estimado) pm
Estado(s) de oxidación: −1, +1, +3, +5 (predicción)
1.ª energía de ionización: 742,9 kJ/mol (predicción)
Propiedades Físicas
Estado ordinario: Sólido (predicción)
Punto de fusión: 573 K (300 °C) a 773 K (500 °C) (predicción)
Punto de ebullición: 823 K (550 °C) (predicción)
Varios
N.º CAS: 54101-14-3
Isótopos más estables
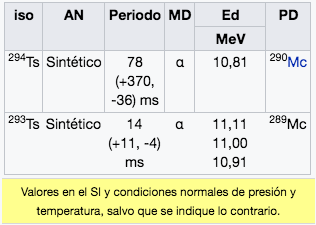
Oganesón
El oganesón (anteriormente llamado ununoctio) es el nombre para el elemento sintético de la tabla periódica cuyo símbolo es Og y su número atómico es 118. Es el elemento más pesado sintetizado hasta ahora y el último del séptimo período en la tabla periódica. En la tabla periódica es un elemento del bloque p y el último del periodo 7. El 3 es actualmente el único elemento sintético del grupo 18 y posee el número y masa atómica más altos de todos los elementos sintetizados.
El 30 de diciembre de 2015, la IUPAC anunció en su portal web la verificación del descubrimiento de cuatro elementos del período 7, entre ellos el oganesón. El nuevo elemento fue así llamado en español (con la terminación –ón tónica) siguiendo el criterio ortográfico de denominación de los gases nobles (neón, xenón…). Fue nombrado así en honor al físico ruso Yuri Oganesián.
El átomo de oganesón es radiactivo y altamente inestable, por lo que desde 2002 solo se han detectado tres o posiblemente cuatro átomos del isótopo 294Og. Si bien este hecho no posibilita un estudio experimental adecuado que pueda caracterizar sus propiedades y sus posibles compuestos, varios cálculos teóricos han permitido predecir muchas de sus cualidades, incluidas algunas inesperadas. Por ejemplo, a pesar de que el oganesón es formalmente un elemento del grupo 18, probablemente no sea un gas noble, como el resto de elementos del grupo. Si bien inicialmente se pensaba que era un gas, ahora se supone que es un sólido bajo condiciones normales de presión y temperatura.
El oganesón es el elemento químico más pesado observado en laboratorio y su síntesis, junto a la del livermorio, no estuvo exenta de polémica. El equipo estadounidense que anunció en primer lugar la síntesis en 1999 tuvo que publicar una retractación en 2002 reconociendo que habían amañado los datos experimentales. Este hecho provocó un escándalo científico de grandes proporciones y la revisión de las normas éticas de la investigación en varios centros del país. En 2006 un equipo ruso publicó su síntesis y este resultado no ha sido cuestionado por otros científicos. El descubrimiento de este elemento fue reafirmado por el español Miguel Antón en el año 2013 en el CERN en Ginebra.
Historia
Rutas de síntesis
A finales de 1998 el físico polaco Robert Smolańczuk publicó sus cálculos sobre la fusión nuclear de varios núcleos atómicos para sintetizar elementos transuránicos, incluido el elemento 118. Sus cálculos sugerían que era posible formar dicho elemento fusionando plomo y kriptón bajo condiciones cuidadosamente controladas.
Según las predicciones de Smolańczuk, en la siguiente tabla se muestran las posibilidades de combinaciones de átomos para la síntesis del oganesón que teóricamente proporcionan una sección eficaz (σmax) adecuada para la expulsión de un neutrón y un rendimiento químico apreciable.
Intentos infructuosos
En 1999 un grupo de investigación del Laboratorio Nacional Berkeley, en Estados Unidos, hizo uso de las predicciones de Smolańczuk y anunció el descubrimiento de los elementos 116 y 118 en un artículo publicado en Physical Review Letters, y poco después en Science, mediante la siguiente reacción, que también libera un neutrón:
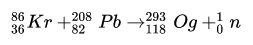
Según el artículo, se usó un ciclotrón de 88 pulgadas para acelerar el haz de 86Kr hasta una energía aproximada de 449 MeV y lanzarlo contra el blanco de 208Pb. Tras once días, el equipo separó e identificó tres átomos de oganesón, con un rendimiento aproximado de un impacto productivo por cada 1012 interacciones.
Sin embargo, al año siguiente tuvieron que publicar una retractación, después de que investigadores de otros laboratorios no lograran reproducir el experimento. En junio de 2002 el director del laboratorio anunció que la afirmación del descubrimiento de los elementos 116 y 118 se basaba en datos inventados por el principal autor del experimento, el búlgaro Victor Ninov.
Descubrimiento
El primer grupo de átomos de oganesón fue propiamente observado en el Instituto Central de Investigaciones Nucleares (JINR) de Dubná, Rusia, en 2002. El 9 de octubre de 2006 un equipo conjunto del JINR y del Laboratorio Nacional Lawrence Livermore estadounidense, trabajando en las instalaciones del JINR, anunciaron que habían detectado indirectamente un total de tres o quizás cuatro núcleos de oganesón-294, solo uno o dos en 2002 y dos más en 2005, mediante la colisión de iones de californio-249 y calcio-48:
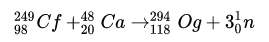
Debido a que la probabilidad de que ocurra una reacción de fusión es muy pequeña (la sección eficaz del núcleo es ~ 0,3-0,6 pb = (3-6)×10−41 m2) el experimento duró cuatro meses y precisó un haz de 4×1019 iones de calcio colisionados con el californio para producir la primera posible síntesis de oganesón. Sin embargo, los científicos están de acuerdo en que no se trata de un falso positivo, pues la posibilidad de que la detección fuera debida a un evento aleatorio se estimó en menos de una parte en 100000.
En estos experimentos se observó la desintegración alfa (αn en el gráfico) de los tres átomos de oganesón en la que el 294Og se desintegra a livermorio-290 liberando un átomo de helio-4. También se propuso una fisión espontánea directa. Se calculó un periodo de semidesintegración (o semivida) de 0,89 ms, pero como solo se observaron tres átomos, es un valor con poca exactitud, estimado como 0,89 (+1,07|-0,31)ms. La desintegración se produce de la siguiente forma:
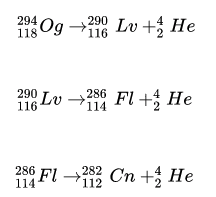
La identificación del núcleo de 294Og se verificó creando separadamente su producto de desintegración 290Lv mediante el bombardeo de Curio-245 con iones de 48Ca y comprobando que el 290Lv sigue la cadena de desintegración del núcleo de 294Og:
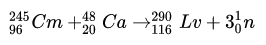
El producto de desintegración 290Lv es muy inestable, con un periodo de semidesintegración de 14 ms, tras el cual se desintegra a flerovio-286, que a su vez prosigue la desintegración, que puede ser espontánea o de tipo alfa, a copernicio-282, que también se desintegra espontáneamente.
En un modelo de túnel cuántico, una técnica predictiva de química computacional, se calculó el periodo de semidesintegración por desintegración alfa del 294Og en 0,66(+0,23,-0,18)ms, resultado publicado, junto a la energía cinética liberada en la desintegración, denominada valor Q, en 2004. Los cálculos del valor Q en el modelo macroscópico-microscópico de Muntian-Hofman-Patyk-Sobiczewski predicen unos resultados menores pero comparables.
Tras el éxito en la obtención del oganesón, el equipo de descubridores ha realizado experimentos similares con el objetivo de crear el unbinilio a partir de hierro-58 y plutonio-244. Los cálculos predictivos adelantan que los isótopos del elemento 120 tendrán un periodo de semidesintegración en desintegración alfa del orden de los microsegundos. En 2009 publicaron los resultados, hasta ahora infructuosos, de sus experimentos.
Nombre
Hasta los años 1960, de forma similar al resto de elementos predichos por Dmitri Mendeléyev el oganesón fue conocido por el nombre de eka-emanation, siendo eka la palabra sánscrita para «uno» y emanation el antiguo nombre del radón.
En 1979 la Unión Internacional de Química Pura y Aplicada (IUPAC) publicó una serie de recomendaciones de nomenclatura para los elementos con número atómico mayor de cien, de acuerdo al cual el elemento 118 debe ser llamado ununoctium o, en forma hispanizada, ununoctio. Este nombre sistemático sirve como marcador de la posición del elemento en la tabla periódica hasta que su descubrimiento sea confirmado y la IUPAC decida un nombre.
Antes de la retractación de 2002, los investigadores del laboratorio Berkeley propusieron el nombre ghiorsium (Gh), como homenaje a Albert Ghiorso, uno de los líderes del equipo.
Tras el descubrimiento de los científicos rusos, el director del Instituto Central de Investigaciones Nucleares (JINR) afirmó en 2007 que estaban considerando dos nombres para el nuevo elemento: Flyorium en honor de Gueorgui Fliórov, el fundador del instituto, y moskovium, en honor del óblast de Moscú donde está localizada Dubná. También defendió que, aunque el elemento fue descubierto gracias a una investigación conjunta con científicos de Estados Unidos, que proporcionaron el californio necesario, el elemento debe llevar un nombre ruso, puesto que el Laboratorio Fliórov de Reacciones Nucleares en el JINR era la única instalación en todo el mundo en la que se podía conseguir la síntesis.
El ununoctio fue renombrado como oganesón, en honor al Profesor Yuri Oganesián. Su símbolo químico es Og.
Referencias
1. «Consulta: elementos químicos». Fundéu BBVA. 24 de noviembre de 2016.
2. Clinton S. Nash (2005). «Atomic and Molecular Properties of Elements 112, 114, and 118». Journal of Physical Chemistry A 109 (15): 3493-3500. Consultado el 27 de septiembre de 2009.
Información general
Nombre: Oganesón
Símbolo: Og
Número: 118
Serie Química: Gases nobles
Grupo: 18
Período: 7
Bloque: p
Masa Atómica: 294 u
Configuración Electrónica: [Rn] 5f14 6d9 7s2 7p6
Electrones por nivel: 2, 8, 18, 32, 32, 18, 8 (predicción)
Propiedades Atómicas
Radio medio: 19e7x+3 pm
Radio atómico (calc): 1.8x10dec=1.9 =e7.3\4 (predicción) 152 pm (radio de Bohr)
Radio covalente: (extrapolación) 230 pm
Estado(s) de oxidación: 0, +2, +4
1.ª energía de ionización: (cálculo) 820–1130 kJ/mol
2.ª energía de ionización: (extrapolación) 1450 kJ/mol
Propiedades Físicas
Estado ordinario: Desconocido
Densidad: (predicción) 13,65 kg/m3
Punto de ebullición: (predicción) 320 K (47 °C) a 380 K (107 °C)
Entalpía de vaporización: (extrapolación) 19,4 kJ/mol
Entalpía de fusión: (extrapolación) 23,5 kJ/mol
Punto crítico: (extrapolación) 439(6,8 · 103) Pa
Varios
N.º CAS: 54144-19-3
Isótopos más estables

Ástato
El ástato o astato es un elemento químico de la tabla periódica cuyo símbolo es At y su número atómico es 85. Es radiactivo y el más pesado de los halógenos. Se produce a partir de la degradación de uranio y torio.
Características
El comportamiento químico de este elemento altamente radiactivo es muy similar al de otros halógenos, especialmente el yodo. Se piensa que el ástato es más metálico que el yodo. Investigadores del Laboratorio Nacional de Brookhaven han realizado experimentos en los que se han identificado y medido reacciones elementales que involucran al ástato.
El ástato, seguido del francio, es el elemento más raro de la naturaleza, con una cantidad total sobre la superficie terrestre menor de 25 gramos en el mismo instante de tiempo.
Todos los isótopos conocidos del ástato son de vida corta; el más estable de estos, es el ástato-210, cuya vida data de aproximadamente 8,1 horas. El ástato elemental nunca ha sido observado, ya que cualquier muestra macroscópica sería inmediatamente vaporizada, debido a su calentamiento radiactivo; aún no se ha determinado con exactitud si este obstáculo puede ser superado exponiendo al ástato a una refrigeración adecuada.
Las propiedades de volumen del ástato no son conocidas. Algunas pueden ser estimadas basándose en su ubicación en la tabla periódica, como un análogo más pesado del yodo. El ástato tiende a tener una apariencia oscura, lustrosa y brillante; puede ser un elemento semiconductor o posiblemente un metal. Probablemente posee un punto de fusión más elevado que el punto de fusión del yodo. Químicamente, muchas especies de ástato aniónico son conocidas, y la mayoría de estas variaciones se asemejan al yodo.
El primer grupo de átomos de oganesón fue propiamente observado en el Instituto Central de Investigaciones Nucleares (JINR) de Dubná, Rusia, en 2002. El 9 de octubre de 2006 un equipo conjunto del JINR y del Laboratorio Nacional Lawrence Livermore estadounidense, trabajando en las instalaciones del JINR, anunciaron que habían detectado indirectamente un total de tres o quizás cuatro núcleos de oganesón-294, solo uno o dos en 2002 y dos más en 2005, mediante la colisión de iones de californio-249 y calcio-48:
El ástato también manifiesta cierto comportamiento metálico, como su capacidad de formar cationes monoatómicos estables en soluciones acuosas; a diferencia de los halógenos más ligeros (flúor, bromo y yodo).
Historia
El ástato (del griego αστατος, astatos, que significa inestable) fue sintetizado por primera vez en 1940 por Dale R. Corson, K. R. MacKenzie y Emilio Segrè en la Universidad de Berkeley (California), bombardeando bismuto con partículas alfa. Un primer nombre para el elemento fue alabamio (Ab).
Obtención
El ástato se obtiene bombardeando bismuto con partículas alfa, obteniendo isótopos 209At y 210At, con un periodo de semidesintegración relativamente alto.
Isótopos
Existen 41 isótopos conocidos de ástato, todos radiactivos. El isótopo más longevo, el 210At, que tiene un periodo de semidesintegración de 8,1 horas, y el menos longevo es el isótopo 213At, con uno de 125 nanosegundos.
Referencias
1. «Ástato, el elemento químico más raro de la Tierra». Consultado el 13 de mayo de 2015.
Información general
Nombre: Ástato
Símbolo: At
Número: 85
Serie Química: Halógenos
Grupo: 17
Período: 6
Bloque: p
Masa Atómica: 210 u
Configuración Electrónica: [Xe] 4f14 5d10 6s2 6p5
Electrones por nivel: 2, 8, 18, 32, 18, 7
Propiedades Atómicas
Electronegatividad: 2, 2 (escala de Pauling)
Estado(s) de oxidación: ±1,3,5,7
1.ª energía de ionización: 920 kJ/mol
Propiedades Físicas
Estado ordinario: sólido
Punto de fusión: 575 K (302 °C)
Entalpía de fusión: 114 kJ/mol
Conductividad térmica: 2,7 W/(K·m)
Isótopos más estables

Radón
El radón es un elemento químico perteneciente al grupo de los gases nobles. En su forma gaseosa es incoloro, inodoro e insípido y en forma sólida su color es rojizo. En la tabla periódica tiene el número 86 y símbolo Rn. Su masa media es de 222, lo que implica que por término medio tiene 222-86 = 136 neutrones. Igualmente, en estado neutro le corresponde tener el mismo número de electrones que de protones, esto es, 86.
Es un elemento radiactivo y gaseoso, encuadrado dentro de los llamados gases nobles.
El radón es producto de la desintegración del radio (226Ra), elemento altamente radiactivo. El isótopo 219Rn es producto de la desintegración del actinio, llamado actinón y tiene una vida media de 4 segundos. Además de todos estos, el radón tiene 22 isótopos artificiales, producidos por reacciones nucleares por transmutación artificial en ciclotrones y aceleradores lineales. El isótopo más estable es el 222Rn, también el más abundante, con una vida media de 3,2 días y producto de la desintegración del 226Ra. Al emitir partículas alfa se convierte en 218Po.
Aplicaciones
La emanación del radón del suelo varía con el tipo de suelo y con el contenido de uranio superficial, así que las concentraciones al aire libre del radón se pueden utilizar para seguir masas de aire en un grado limitado. Este hecho ha sido puesto al uso por algunos científicos atmosféricos.
Aunque algunos médicos creyeron una vez que el radón se puede utilizar terapéuticamente, no hay evidencia para esta creencia y el radón no está actualmente en uso médico, por lo menos en el mundo desarrollado.
El sismólogo italiano Gianpaolo Giuliani había anticipado el terremoto que sacudió la zona central de Italia el 6 de abril de 2009 y basó sus pronósticos en las concentraciones de gas radón en zonas sísmicamente activas, fue denunciado a la policía por "extender la alarma" y se vio obligado a quitar sus conclusiones de Internet. Un mes antes del terremoto de una magnitud de entre 5,8 y 6,3 en la escala de Richter que habría dejado unas 50.000 personas sin techo, alrededor de 26 ciudades sufrieron daños graves y más de un centenar de muertos, unas furgonetas con altavoces comenzaron a circular por L'Aquila (Italia) pidiendo a sus habitantes que evacuaran sus casas, después de que el sismólogo anticipara que se produciría un gran terremoto. Cuando los medios de comunicación preguntaron sobre la supuesta falla de las autoridades a la hora de salvar a la población antes del terremoto, el director del Instituto Nacional de Geofísica, Enzo Boschi, quitó importancia a las predicciones de Giuliani.
"Cada vez que hay un sismo hay gente que dice que lo ha predicho", afirmó. "Por lo que yo sé, nadie predijo este sismo con precisión. No es posible predecir los terremotos".
No obstante, existen varios precedentes de predicción de terremotos donde han sido confirmadas las altas concentraciones de este gas antes de los sismos. Por citar algunos ejemplos: Galicia, España en 1997 y Haicheng en China, en los años setenta, cuya predicción a tiempo salvó miles de vidas. Estos terremotos no fueron predichos basándose únicamente en las concentración del gas, pero este fue uno de los factores influyentes.
Historia y etimología
El radón fue descubierto en 1900 por Friedrich Ernst Dorn, siendo el quinto elemento radiactivo conocido después del uranio, el torio, el radio y el polonio. En 1900 Dorn informó sobre algunos experimentos en los que notificó que los compuestos de radio emanan un gas radiactivo al que llamó Radium emanation (Ra Em). Anteriormente, en 1899, Pierre y Marie Curie habían observado que el gas emitido por el radio mantuvo su radiactividad durante un mes. Ese mismo año, Robert Bowie Owens y Ernest Rutherford, en la Universidad McGill de Montreal, observaron variaciones al tratar de medir la radiación del óxido de torio. Rutherford se dio cuenta de que los compuestos de torio emiten continuamente un gas radiactivo que conserva los poderes radiactivos durante varios minutos, y llamó primero a este gas emanación (del latín "Emanare"), y después emanación de torio (Th Em). En 1901, demostró que estas emanaciones son radiactivas, atribuyendo a los Curie el descubrimiento del elemento. En 1903 André-Louis Debierne observó similares emanaciones del actinio, este gas fue denominado emanación del actinio (Ac Em).
Varios nombres fueron sugeridos para estos tres gases: exradio, extorio, y exactinio en 1904; radón, torón, y actón en 1918; radeón, toreón, y actineón en 1919, y, finalmente radón, torón, y actinón en 1920. La semejanza de los espectros de estos tres gases con los del argón, criptón y xenón, además de su carácter inerte, llevó a Sir William Ramsay a sugerir en 1904 que las "emanaciones" podían contener un elemento nuevo de la familia de los gases nobles.
En 1910, Sir William Ramsay y Robert Whytlaw-Gray aislaron el radón, determinaron su densidad, y se determinó que era el gas conocido más pesado. Escribieron que "L'expression de l'émanation du radium est fort incommode", (La presencia de la emanación de radio es muy incómoda) y sugirieron el nuevo nombre de nitón (Nt) (de la palabra latina "nitens" que significa "brillante") para enfatizar la propiedad de radioluminiscencia que exhibe el gas, y en 1912 fue aceptado por la Comisión sobre Abundancia de Isótopos y Pesos Atómicos. En 1923, el Comité Internacional de los Elementos Químicos y la Unión Internacional de Química Pura y Aplicada (IUPAC) eligió entre los nombres de radón (Rn), torón (Tn), y actinón (An). Más tarde, cuando se numeraron los isótopos en lugar de ser nombrados, el elemento tomó el nombre del isótopo más estable, el radón, el torón Tn se renombró como 220Rn y el actinón An fue renombrado como 219Rn. En la década de 1960, el elemento todavía se designaba simplemente como emanación en algunos textos. El primer compuesto sintetizado de radón, el fluoruro de radón, se obtuvo en 1962.
El peligro de una alta exposición al radón en las minas, donde se pueden encontrar exposiciones que alcanzan los 1.000.000 Bq / m3, es conocido desde hace mucho tiempo. En 1530, Paracelso describió una enfermedad degenerativa de los mineros, la mala metallorum, y Georgius Agricola señaló la importancia de la ventilación en las minas para evitar este mal de las montañas (Bergsucht). Este hecho ya fue identificado en 1879 como causante de cáncer de pulmón en una investigación efectuada por Herting y Hesse sobre los mineros de Schneeberg, Alemania. Los primeros estudios importantes sobre el radón y la salud se efectuaron en el contexto de la minería del uranio en la región de Jáchymov en Bohemia. En los EE.UU., los estudios y la adopción de medidas de protección solo se llevaron a cabo tras décadas de efectos perniciosos sobre la salud de los mineros del uranio del sudoeste del país, a comienzos de la Guerra Fría; las primeras normas no se implementan hasta 1971.
La presencia de radón en el aire interior de los edificios fue documentada ya en 1950. A partir de la década de 1970 se inició la investigación para hacer frente a las fuentes de radón en el interior, los factores determinantes de la concentración, efectos sobre la salud, y medidas de protección. En los Estados Unidos, el problema del radón en el interior de las viviendas tuvo una gran repercusión pública, intensificándose la investigación después de un incidente ampliamente difundido en 1984. Durante una inspección rutinaria en una planta de energía nuclear de Pensilvania, se encontró un trabajador contaminado con radiactividad. Una alta contaminación de radón en su domicilio fue identificada posteriormente como la causa responsable de esta contaminación.
Efectos perjudiciales
Cuando se habla del peligro del radón no se debe olvidar la radiación emitida por todo el conjunto: radón y descendientes. El peligro está sobre todo en sus descendientes de vida corta: en concreto el 218Po y 214Po. Existe también una exposición externa causada por la radiación gamma directa, pero el verdadero riesgo está en las partículas alfa.
La radiación alfa es relativamente poco peligrosa fuera del cuerpo porque la epidermis nos protege de ella. El principal problema viene cuando se inhala: las partículas radioactivas se adhieren al tejido pulmonar, donde pueden emitir radiación alfa a las células broncopulmonares. La absorción de esta radiación provoca ionizaciones y excitaciones de las estructuras celulares provocando efectos lesivos: puede dañar directa e indirectamente el DNA y provocar mutaciones en el tejido pulmonar. Recordemos que el cáncer es una división incontrolada de células mutadas. En EE. UU. está considerada la segunda causa de muerte por cáncer de pulmón después del tabaco . Además, sus efectos son sinérgicos: fumar y vivir en una casa con alto contenido de radón aumenta el riesgo unas 46 veces más que de darse los dos fenómenos por separado.
Un estudio en Alemania nos dice que con una concentración de 40 Bq/m3 el 7% de todos los cánceres de pulmón en fumadores se puede atribuir al radón: en no fumadores se puede atribuir hasta un 22%. Esto es lógico porque en fumadores es difícil atribuir una sola causa. Otros estudios en no fumadores en Francia nos dicen que puede llegar a atribuirse hasta un 25%. En Holanda un 17% y en Suecia un 24%. En Galicia la combinación de Tabaco y radón se atribuye en un 25%. La recomendación de protección radiológica en Europa establece el nivel de referencia acción de remedio 400 Bq/m3. Y el nivel de diseño de nuevas viviendas en 200 Bq/m3. La agencia norteamericana de protección ambiental establece como el nivel de acción cuando se superan los 4 PCi/l (148 Bq/m3).
Referencias
1. Rutherford, E. (1900). «A radioactive substance emitted from thorium compounds». Phil. Mag. 40: 1-4.
2. Le radon, aspects historiques et perception du risque, Roland Masse.
Información general
Nombre: Radón
Símbolo: Rn
Número: 86
Serie Química: Gases nobles
Grupo: 18
Período: 6
Bloque: p
Masa Atómica: (222) u
Configuración Electrónica: [Xe] 4f14 5d10 6s2 6p6
Electrones por nivel: 2, 8, 18, 32, 18, 8
Propiedades Atómicas
Radio atómico (calc): 120 pm (radio de Bohr)
Radio covalente: 145 pm
Estado(s) de oxidación: 0 (desconocido)
1.ª energía de ionización: 1037 kJ/mol
Propiedades Físicas
Estado ordinario: Gas (no magnético)
Densidad: 9,73 kg/m3
Punto de fusión: 202 K (−71 °C)
Punto de ebullición: 211,3 K (−62 °C)
Entalpía de vaporización: 16,4 kJ/mol
Entalpía de fusión: 2,89 kJ/mol
Varios
Estructura cristalina: Cúbica centrada en las caras
Calor específico: 94 J/(K·kg)
Conductividad térmica: 0,00364 W/(K·m)
Isótopos más estables
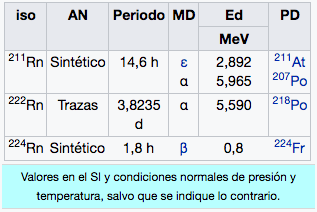
Talio
Es un metal del bloque p gris, blando y maleable es parecido al estaño, pero se decolora expuesto al aire. Es muy tóxico y se ha empleado como raticida e insecticida, pero este uso ha sido disminuido o eliminado en muchos países debido a sus posibles efectos cancerígenos. También se emplea en detectores infrarrojos.
Características principales
Este metal es muy blando y maleable; se puede cortar con un cuchillo. Al ser expuesto al aire pasa de presentar un brillo metálico a rápidamente empañarse con un tono gris azulado parecido al plomo.
Aplicaciones
El sulfato de talio, que es inodoro e insípido fue usado para exterminar ratas y hormigas. Desde 1972 su uso fue prohibido en Estados Unidos a causa de su toxicidad. Otros países siguieron el ejemplo en los años siguientes. Las sales de talio se usaron como tratamiento de dermatofitosis, otras infecciones de la piel y para reducir la sudoración nocturna de los pacientes con tuberculosis. Sin embargo, este uso fue muy limitado debido a su estrecho índice terapéutico, y el desarrollo de medicamentos más eficientes.
- Óptica
- Electrónica
- Imagenología médica
Obtención
Aunque el talio no es tan escaso como otros elementos (abundancia de 0.000085%), se encuentra asociado con potasio en arcillas, suelos, y granitos.
Referencias
1. The discovery of the elements. XIII. Supplementary note on the discovery of thallium
2. Spectroscopy and the Elements in the Late Nineteenth Century: The Work of Sir William Crookes
3. De l'existencè d'un nouveau métal, le thallium
Información general
Nombre: Talio
Símbolo: Tl
Número: 81
Serie Química: Metales del bloque p
Grupo: 13
Período: 6
Bloque: p
Masa Atómica: 204.3833 u
Configuración Electrónica: [Xe]4f145d106s26p1
Electrones por Nivel: 2, 8, 18, 32, 18, 3
Propiedades Atómicas
Electronegatividad: 1.62 (escala de Pauling)
Radio Atómico (calc): 170 pm (radio de Bohr)
Radio Covalente: 145 pm
Estado(s) de oxidación: 3, 1
1.ª Energía de ionización: 589.4 kJ/mol
2.ª Energía de ionización: 1971 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 11850 kg/m3
Punto de fusión: 577 K (700 °C)
Punto de ebullición: 1746 K (1737 °C)
Entalpía de fusión: 4.14 kJ/mol
Presión de vapor: 0.00000533
Varios
Estructura cristalina: Hexagonal
Calor Específico: 129 J/(K·kg)
Conductividad Térmica: 46.1 W/(K·m)
Isótopos más estables
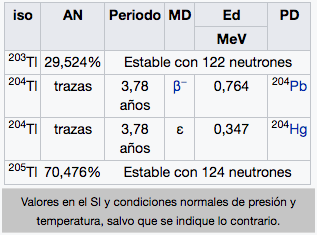
Plomo
El plomo es un elemento químico de la tabla periódica, cuyo símbolo es Pb (del latín plumbum) y su número atómico es 82 según la tabla actual, ya que no formaba parte en la tabla periódica de Mendeléyev . Este químico no lo reconocía como un elemento metálico común por su gran elasticidad molecular. Cabe destacar que la elasticidad de este elemento depende de la temperatura ambiente, la cual extiende sus átomos.
El plomo es un metal pesado de densidad relativa o gravedad específica 11,4 a 16 °C, de color plomo (gris oscuro), que se empaña para adquirir un color gris mate. Es flexible, inelástico y se funde con facilidad. Su fusión se produce a 327,4 °C y hierve a 1725 °C. Las valencias químicas normales son 2 y 4. Es relativamente resistente al ataque del ácido sulfúrico y del ácido clorhídrico, aunque se disuelve con lentitud en ácido nítrico y ante la presencia de bases nitrogenadas. El plomo es anfótero, ya que forma sales de plomo de los ácidos, así como sales metálicas del ácido plúmbico. Tiene la capacidad de formar muchas sales, óxidos y compuestos organometálicos.
Características principales
Los compuestos de plomo más utilizados en la industria son los óxidos de plomo, el tetraetilo de plomo y los silicatos de plomo. El plomo forma aleaciones con muchos metales, y, en general, se emplea en esta forma en la mayor parte de sus aplicaciones. Es un metal pesado y tóxico, y la intoxicación por plomo se denomina como saturnismo o plumbosis.
Efectos en el organismo
- Perturbación de la biosíntesis de hemoglobina y subsecuentemente anemia
- Incremento de la presión sanguínea
- Daño a los riñones
- Aborto espontáneo
- Perturbación del sistema nervioso
- Daño al cerebro
- Disminución de la fertilidad del hombre a través del daño en el esperma
- Disminución de las habilidades de aprendizaje de los niños
- Perturbación en el comportamiento de los niños, como es agresión, comportamiento impulsivo e hipersensibilidad
- Alteraciones graves en la propiocepción, equilibriocepción, nocicepción y electrocepción, magnetocepción, ecolocalización en ciertos animales
- La formación de depósitos plúmbicos en las encías que forman una línea de color gris claro azulado llamada «la línea del plomo» o «la línea de Burton»
Referencias
1. ATSDR en Español - Estudios de Caso en Medicina Ambiental: La toxicidad del plomo
2. ATSDR en Español - ToxFAQs™: Plomo (Pb)
3. Instituto Nacional de Seguridad e Higiene en el Trabajo de España
4. Lenntech Tabla periódica

Información general
Nombre: Plomo
Símbolo: Pb
Número: 82
Serie Química: Metales del bloque p
Grupo: 14
Período: 6
Bloque: p
Masa Atómica: 207.2 u
Configuración Electrónica: [Xe]6s24f145d106p2
Electrones por Nivel: 2, 8, 18, 32, 18, 4
Propiedades Atómicas
Electronegatividad: 2.33 (escala de Pauling)
Radio Atómico (calc): 154 pm (radio de Bohr)
Radio Covalente: 147 pm
Estado(s) de oxidación: 4, 2
1.ª Energía de ionización: 715.6 kJ/mol
2.ª Energía de ionización: 1450.5 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 11340 kg/m3
Punto de fusión: 600.61 K (700 °C)
Punto de ebullición: 2022 K (1737 °C)
Entalpía de fusión: 4.799 kJ/mol
Presión de vapor: 0.000000421
Varios
Estructura cristalina: Cúbica centrada en las caras
Calor Específico: 129 J/(K·kg)
Conductividad Térmica: 35.3 W/(K·m)
Isótopos más estables
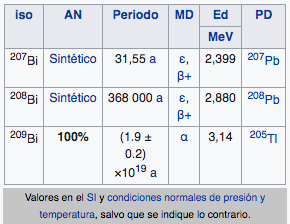
Bismuto
El bismuto es un elemento químico de la tabla periódica cuyo símbolo es Bi, su número atómico es 83 y se encuentra en el grupo 15 del sistema periódico.
Características principales
Cuando es sólido flota sobre su estado líquido, por tener menor densidad en el estado sólido. Esta característica es compartida con el agua, el galio, el ácido acético, el antimonio y el silicio.
El bismuto es uno de los dos peores conductores térmicos que existen entre todos los metales (junto al manganeso); es también el metal más diamagnético y sus aleaciones aprovechan ambas ventajas en situaciones donde se requiera. No existe de manera natural en el cuerpo humano ni en ninguna forma de vida en general. Se utiliza mucho en medicina, siendo parte de los astringentes recetados para problemas relacionados con el sistema digestivo, diarreas fuertes o irritaciones esofágicas, del colon, duodeno o intestinos.
Aplicaciones
- Puede ser usado como sustituto del plomo
- Cosméticos y pigmentos
Referencias
1. Chemistry of arsenic, antimony, and bismuth
2. Bismuto
3. Bismuto en environmentalchemistry.com.
Información general
Nombre: Bismuto
Símbolo: Bi
Número: 83
Serie Química: Metales del bloque p
Grupo: 15
Período: 6
Bloque: p
Masa Atómica: 208.98 u
Configuración Electrónica: [Xe]4f145d106s26p3
Electrones por Nivel: 2, 8, 18, 32, 18, 5
Propiedades Atómicas
Electronegatividad: 2.02 (escala de Pauling)
Radio Atómico (calc): 143 pm (radio de Bohr)
Radio Covalente: 146 pm
Estado(s) de oxidación: 3, 5
1.ª Energía de ionización: 703 kJ/mol
2.ª Energía de ionización: 1610 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 9780 kg/m3
Punto de fusión: 544.4 K (700 °C)
Punto de ebullición: 1837 K (1737 °C)
Entalpía de fusión: 11.3 kJ/mol
Presión de vapor: 0.000627
Varios
Estructura cristalina: Romboédrica
Calor Específico: 122 J/(K·kg)
Conductividad Térmica: 7.87 W/(K·m)
Isótopos más estables

Polonio
El polonio es un elemento químico en la tabla periódica de los elementos cuyo símbolo es Po y su número atómico es 84. Se trata de un raro metal altamente radiactivo, químicamente similar al telurio y al bismuto, presente en minerales de uranio.
Características principales
Estas sustancias se disuelven con mucha facilidad en ácidos, pero es solo ligeramente soluble en alcalinos. Está químicamente relacionado con el teluro y el bismuto. El polonio es un metal volátil, reducible al 50% tras 45 horas al aire a una temperatura de 54,8 °C (328 K). Ninguno de los 50 isotopos estimados del polonio es estable. Es extremadamente tóxico y altamente radiactivo. Se ha encontrado polonio en minerales de uranio, humo de tabaco y como contaminante. Todos los elementos a partir del polonio son significativamente radiactivos.
Aplicaciones
Mezclado o aleado con berilio, el polonio puede ser una fuente de neutrones, y fue utilizado como tal en la bomba atómica lanzada en Nagasaki, para producir en el breve lapso de la implosión (producida por el explosivo convencional TNT) un número suficiente de neutrones para desencadenar la reacción en cadena del plutonio, y la consiguiente explosión atómica. Se utiliza también en dispositivos destinados a la eliminación de carga estática, en cepillos especiales para eliminar el polvo acumulado en películas fotográficas y también en fuentes de calor para satélites artificiales o sondas espaciales.
Referencias
1. WebElements.com - Polonium
2. Información sobre el Polonio 210
3. Ficha técnica del Polonio-210
Información general
Nombre: Polonio
Símbolo: Po
Número: 84
Serie Química: Metaloides
Grupo: 16
Período: 6
Bloque: p
Masa Atómica: 209.98 u
Configuración Electrónica: [Xe]4f145d106s26p4
Electrones por Nivel: 2, 8, 18, 32, 18, 6
Propiedades Atómicas
Electronegatividad: 2.0 (escala de Pauling)
Radio Atómico (calc): 135 pm (radio de Bohr)
Radio Covalente: 146 pm
Estado(s) de oxidación: 6, 4, 2, -2
1.ª Energía de ionización: 812.1 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido (No Magnético)
Densidad: 9196 kg/m3
Punto de fusión: 527 K (700 °C)
Punto de ebullición: 1235 K (1737 °C)
Entalpía de fusión: 60.1 kJ/mol
Presión de vapor: 0.0176
Varios
Estructura cristalina: Cúbica simple
Conductividad Térmica: 20 W/(K·m)
Isótopos más estables
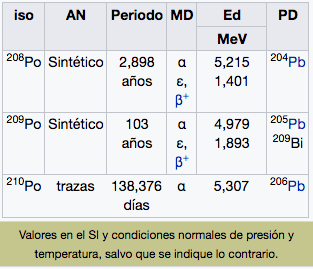
Cerio
El cerio es un elemento químico de símbolo Ce y número atómico 58. Es uno de los 14 elementos químicos que siguen al lantano en la tabla periódica, denominados por ello lantánidos. El cerio está situado entre el lantano y el praseodimio.
Es un metal blando, de color gris metálico similar al hierro, dúctil, que se oxida fácilmente al contacto con el aire y se torna pardo rojizo. El cerio es el más abundante de los elementos de las tierras raras, su abundancia representa solo el 0,0046% en peso de la corteza terrestre, donde aparece disperso en diversos minerales, como la cerita, bastnasita y monacita. Existen numerosas aplicaciones comerciales del cerio. Entre estos usos se incluyen catalizadores, aditivos para el combustible para reducir la contaminación ambiental y a los vidrios y esmaltes para cambiar sus colores. El óxido de cerio es un componente importante de los polvos utilizados para pulir vidrios y fósforos utilizados en pantallas y lámparas fluorescentes. Es utilizado también en la "piedra" o "yesca" de los encendedores (aleación ferrocerio).
Fue descubierto en 1803 por Martin Heinrich Klaproth y Jöns Jacob Berzelius y de manera independiente también por Wilhelm von Hisinger. El elemento fue nombrado en honor al planeta enano Ceres, descubierto dos años antes. El planeta lleva el nombre de la diosa romana Ceres (mitología).
Características principales
Es el lantánido más abundante y económico. El metal es duro y de color gris acerado, tornándose pardo rojizo. Es buen conductor del calor y la electricidad. Reacciona con los ácidos diluidos y con el agua (produciendo hidrógeno). Es inestable en el aire seco, cubriéndose de una capa de óxido en el aire húmedo.
En la Tierra el cerio es casi tan abundante como el cobre; especialmente en forma de óxido de cerio, que habitualmente se utiliza como polvos abrasivos para pulir vidrio. El metal cerio es pirofórico, lo que significa que se inflama fácilmente. El cerio no realiza ninguna función biológica conocida.
Aplicaciones
- Convertidores catalíticos para motores de combustión interna.
- Como catalizador del proceso de cracking en la industria del petróleo.
- En aleaciones utilizadas en encendedores.
- El óxido de cerio se usa para el pulido de lentes, instrumentos ópticos y semiconductores.
- En las aleaciones de los imanes permanentes.
Obtención
El radio es un producto de descomposición del uranio y por lo tanto se puede encontrar en todas las minas de uranio. Originalmente se obtenía de las minas de pechblenda de Joachimstal, Bohemia (con una concentración de unas siete partes por millón, siete gramos de radio por tonelada de pechblenda ). De las arenas de carnotita de Colorado se obtiene también este elemento, pero se han encontrado minas más ricas en la República Democrática del Congo (minas del Alto Katanga) y el área de los Grandes Lagos en Canadá, además de poder obtenerse de los residuos radiactivos de uranio. Hay grandes depósitos de uranio en Ontario, Nuevo México, Utah y Australia, entre otros lugares.
Referencias
1. Enciclopedia Ilustrada Cumbre,(1984), Tomo 3, Editorial Cumbre, S.A. ISBN 968-33-0066-9.

Información general
Nombre: Cerio
Símbolo: Ce
Número: 58
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: 140.116 u
Configuración Electrónica: [Xe]4f15d16s2
Dureza Mohs: 2.5
Electrones por Nivel: 2, 8, 18, 19, 9, 2
Propiedades Atómicas
Electronegatividad: 1.12 (escala de Pauling)
Radio Atómico (calc): 185 pm (radio de Bohr)
Estado(s) de oxidación: 3,4
1.ª Energía de ionización: 534.4 kJ/mol
2.ª Energía de ionización: 1050 kJ/mol
Propiedades Físicas
Estado Ordinario: sólido (no magnético)
Densidad: 6689 kg/m3
Punto de fusión: 1071 K (700 °C)
Punto de ebullición: 3699 K (1737 °C)
Entalpía de fusión: 5.46 kJ/mol
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-45-1
Calor Específico: 190 J/(K·kg)
Conductividad Térmica: 11.4 W/(K·m)
Isótopos más estables
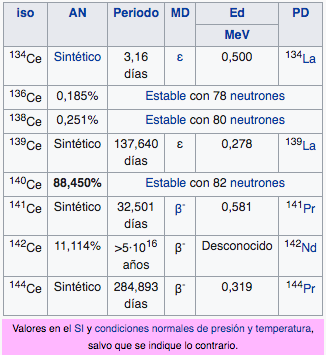
Praseodimio
El praseodimio es un elemento químico de la tabla periódica cuyo símbolo es Pr y su número atómico es 59. Es parte del grupo de tierras raras. Fue descubierto en 1885 por el químico austríaco Carl Auer von Welsbach.
Características principales
El praseodimio es un elemento metálico plateado suave, y pertenece al grupo de los lantánidos. Es algo más resistente a la corrosión en aire que el europio, el lantano, el cerio, o el neodimio, pero desarrolla una capa verde de óxido cuando se rompe o cuando está expuesto al aire, exponiendo más metal a la oxidación. Por esta razón, el praseodimio se debe guardar bajo un aceite mineral ligero o sellar en un cristal.
Aplicaciones
- Como un agente de aleación con el magnesio para crear los metales de alta resistencia que se utilizan en motores de avión.
- Los compuestos del praseodimio son usados para dar a los vidrios y esmaltes un color amarillo.
- El praseodimio se utiliza para colorear zirconia cúbica de un color verde-amarillo, para simular peridoto.
Historia
El nombre praseodimio proviene de las palabras griegas prasios didymos, que significan gemelo verde (πρασιος prasios= "verde") (διδυμος didymos= "gemelo"). El praseodimio y el neodimio se descubrieron juntos y por eso se les llamó gemelos, al ver que formaba una capa de óxido verde al contacto del aire, se le añadió a su nombre ese color. Praseodimio es frecuentemente mal pronunciado como praseodinio.
El praseodimio ha sido históricamente una tierra rara cuyo suministro ha excedido la demanda. No buscado como tal, mucho praseodimio se ha comerciado como una mezcla con lantano y cerio, o "LCP" por las primeras letras de cada uno de los componentes, para usar en reemplazo de las mezclas tradicionales de lantánido que fueron hechas económicamente de monacita o de bastnasita. El LCP es el que permanece de tales mezclas, después del neodimio deseable, y todos los más pesados, más raros y más valiosos lantánidos son quitados, por extracción solvente. Sin embargo, como la tecnología avanza, se ha encontrado posible incorporar el praseodimio en los imanes de neodimio-hierro-boro, de tal modo extendiendo mucho el suministro de la demanda de neodimio. De esta manera, el LC está comenzando a substituir al LCP consecuentemente.
Obtención
El praseodimio está disponible en pequeñas cantidades en la corteza terrestre (9,5 ppm). Se encuentra en los minerales de tierra rara monacita y bastnasita, comprendiendo típicamente cerca del 5% de los lantánidos contenidos en estos, y puede ser recuperado de la bastnasita o de la monazita por un proceso de intercambio de iones, o por extracción solvente de contracorriente.
Referencias
Información general
Nombre: Praseodimio
Símbolo: Pr
Número: 59
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: (140.90765) u
Configuración Electrónica: [Xe]6s24f3
Electrones por Nivel: 2, 8, 18, 21, 8, 2
Propiedades Atómicas
Electronegatividad: 1.13 (escala de Pauling)
Radio Atómico (calc): 247 pm (radio de Bohr)
Radio Covalente: 165 ± 2 pm
Estado(s) de oxidación: 3
1.ª Energía de ionización: 527 kJ/mol
2.ª Energía de ionización: 1020 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 6640 kg/m3
Punto de fusión: 1204 K (700 °C)
Punto de ebullición: 3793 K (1737 °C)
Entalpía de fusión: 6.89 kJ/mol
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-10-0
Calor Específico: 193 J/(K·kg)
Conductividad Térmica: 12.5 W/(K·m)
Isótopos más estables
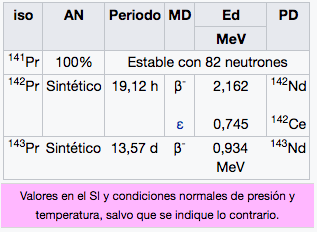
Neodimio
A la temperatura ambiente, se encuentra en estado sólido. Es parte del grupo de tierras raras. Fue descubierto en 1885 por el químico austríaco Carl Auer von Welsbach.
Características principales
Es una tierra rara que compone el metal de Misch aproximadamente en proporción del 18 %, siendo una de las tierras raras más reactivas. Posee un brillo metálico-plateado y brillante. Oscurece rápidamente al contacto con el aire formando un óxido. Pertenece a la familia de los elementos de transición interna y contiene en su forma estable 60 electrones y su isótopo más conocido es Nd-142.
Aplicaciones
Algunas aplicaciones del neodimio:
- Es un componente del didimio, usado para colorear cristales y la fabricación de gafas de protección para los soldadores, pues absorben la luz ámbar de la llama.
- Confiere delicados colores a los cristales que varían desde el violeta puro, hasta el gris claro. La luz transmitida a través de estos cristales presenta bandas de absorción inusualmente agudas. Estos cristales son usados por los astrónomos para calibrar unos dispositivos llamados espectrómetros y filtros de radiación infrarroja. El neodimio se utiliza también para eliminar el color verde causado por los contaminantes del hierro.
- Es muy buen sustituto de la pintura metalizada de los coches.
- Sales de neodimio son usadas como colorantes de esmaltes.
- Recientemente se han fabricado fonocaptores de guitarra con este material por su buen comportamiento electrónico
Historia
El neodimio fue descubierto por Carl Auer von Welsbach, un químico austríaco, en Viena en el año 1885. Separó el neodimio, así como el praseodimio, de un material denominado didimio por medio de análisis espectroscópicos. Sin embargo, este metal no fue aislado antes de 1925. El nombre neodimio proviene de las palabras griegas neos didymos, que significan nuevo gemelo (neos, nuevo) (didymos, gemelo). El praseodimio y el neodimio se descubrieron juntos y por eso se les llamó gemelos; a este se le llamó nuevo ya que al otro se le había dado el nombre de gemelo verde.
Obtención
El neodimio nunca se encuentra en la naturaleza como elemento libre. Se encuentra en minerales como la arena de monacita y bastnasita, que presentan en su composición pequeñas cantidades de todos los metales de las tierras raras. También se puede encontrar en el metal de Misch. Es difícil separarlo de otros elementos de las tierras raras.
Referencias
Información general
Nombre: Neodimio
Símbolo: Nd
Número: 60
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: (144.24) u
Configuración Electrónica: [Xe]4f46s2
Electrones por Nivel: 2, 8, 18, 22, 8, 2
Propiedades Atómicas
Electronegatividad: 1.14 (escala de Pauling)
Radio Atómico (calc): 206 pm (radio de Bohr)
Estado(s) de oxidación: 3
1.ª Energía de ionización: 533.1 kJ/mol
2.ª Energía de ionización: 1040 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 6800 kg/m3
Punto de fusión: 1297 K (700 °C)
Punto de ebullición: 3373 K (1737 °C)
Entalpía de fusión: 7.14 kJ/mol
Varios
Estructura cristalina: Cristalina
N° CAS: 7440-00-8
Calor Específico: 190 J/(K·kg)
Conductividad Térmica: 16.5 W/(K·m)
Isótopos más estables
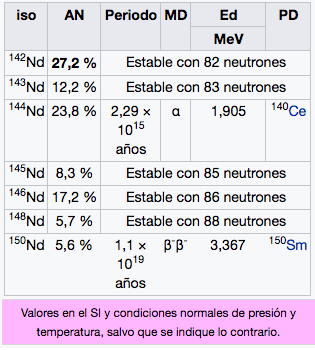
Prometio
El prometio es un elemento químico de la tabla periódica cuyo símbolo es Pm y su número atómico es 61. Algún tiempo se le denominó ilinio (por Illinois). Aunque, tras la observación de ciertas líneas espectrales, algunos científicos han reclamado haber descubierto este elemento en la naturaleza, nadie ha podido aislarlo de sustancias naturales.
En 1902, Branner predijo la existencia de este elemento. Diversos grupos adujeron haberlo obtenido, pero -debido a la dificultad para separar el prometio de otros elementos- no pudieron confirmar tales descubrimientos. Jacob A. Marinsky, Lawrence E. Glendenin y Charles D. Coryell, en 1944, probaron la existencia del prometio.
Demasiado ocupados con las investigaciones relacionadas con la defensa durante la segunda guerra mundial, no reivindicaron su descubrimiento hasta 1947. Lo obtuvieron analizando subproductos de la fisión del uranio generados en un reactor nuclear situado en los laboratorios Clinton, en Tennessee.
Aplicaciones
Su aplicación principal es en la industria de sustancias fosforescentes. También se usa en fabricación de calibradores de aberturas y en baterías nucleares empleadas en aplicaciones exoespaciales (espacio exterior).
El prometio se podría aprovechar para elaboración de una batería que funcione con energía nuclear, que usaría las partículas beta emitidas por la transmutación del prometio para propiciar que una substancia fosforescente emitiera luz, que a su vez mediante un dispositivo similar a un panel solar se convertiría luego en electricidad. Se estima que este tipo de batería podría suministrar energía durante cinco años.
Referencias
1. Los Alamos National Laboratory – Promethium
2. WebElements.com – Promethium
Información general
Nombre: Prometio
Símbolo: Pm
Número: 61
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: (145) u
Configuración Electrónica: [Xe]4f56s2
Electrones por Nivel: 2, 8, 18, 23, 8, 2
Propiedades Atómicas
Electronegatividad: 1.13 (escala de Pauling)
Radio Atómico (calc): 205 pm (radio de Bohr)
Estado(s) de oxidación: 3
1.ª Energía de ionización: 540 kJ/mol
2.ª Energía de ionización: 1050 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7264 kg/m3
Punto de fusión: 1373 K (700 °C)
Punto de ebullición: 3273 K (1737 °C)
Entalpía de fusión: 86.7 kJ/mol
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-12-2
Isótopos más estables
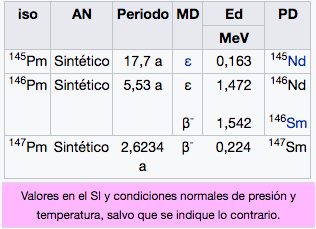
Samario
El samario fue descubierto en 1853 por el químico suizo Jean Charles Galissard de Marignac y aislado en 1879 por el químico Francés Paul Emile Lecoq de Boisbaudran a partir del mineral samarskita. El mineral se encontró inicialmente en los montes Urales y el nombre del mineral y el elemento fue colocado en honor a Samarski, un coronel ruso funcionario de minas.
Aplicaciones
- El óxido de samario se utiliza en óptica para absorber la luz infrarroja
- Como catalizador en la deshidratación y en la deshidrogenación de etanol.
- Se usa como parte de una aleación en los imanes de samario-cobalto.
- El Samario 153 se utiliza junto con el Estroncio 89 en radioterapia paliativa para la disminución del dolor en pacientes terminales.
Obtención
Actualmente el samario es obtenido principalmente a través de un proceso de intercambio iónico de la arena de monacita, un material rico en elementos de tierras raras que contiene hasta un 2,8 % de samario.
Referencias
1. Los Alamos National Laboratory - Samarium
2. WebElements.com - Samarium
Información general
Nombre: Samario
Símbolo: Sm
Número: 62
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: (150.35) u
Configuración Electrónica: [Xe]6s24f6
Electrones por Nivel: 2, 8, 18, 24, 8, 2
Propiedades Atómicas
Electronegatividad: 1.17 (escala de Pauling)
Radio Atómico (calc): 238 pm (radio de Bohr)
Estado(s) de oxidación: 2, 3
1.ª Energía de ionización: 544.5 kJ/mol
2.ª Energía de ionización: 1070 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7353 kg/m3
Punto de fusión: 1345 K (700 °C)
Punto de ebullición: 2076 K (1737 °C)
Entalpía de fusión: 8.63 kJ/mol
Presión de vapor: 563
Varios
Estructura cristalina: Romboédrica
N° CAS: 7440-19-9
Calor Específico: 200 J/(K·kg)
Conductividad Térmica: 13.3 W/(K·m)
Isótopos más estables
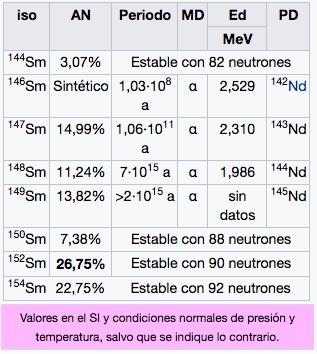
Europio
Fue descubierto en 1890 por Paul Emile Lecoq de Boisbaudran y aislado por primera vez por Eugène Demarçay, quien le dio su actual nombre, en 1901. Debe su nombre al continente europeo.
Características principales
El europio es el más reactivo de todos los elementos de tierras raras. Es peligroso en el ambiente de trabajo, debido al hecho de que los vapores y los gases pueden ser inhalados con el aire. Esto puede causar embolias pulmonares, especialmente por exposiciones a largo plazo. También puede ser una amenaza para el hígado cuando se acumula en el cuerpo humano.
Aplicaciones
No existen aplicaciones comerciales para el europio metálico, aunque ha sido usado para contaminar algunos tipos de plásticos para hacer láseres. Ya que es un buen absorbente de neutrones, el europio está siendo estudiado para ser usado en reactores nucleares.
Referencias
1. Los Alamos National Laboratory - Europium
2. WebElements.com - Europium

Información general
Nombre: Europio
Símbolo: Eu
Número: 63
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: (151.964) u
Configuración Electrónica: [Xe]6s24f7
Dureza Mohs: 1,25
Electrones por Nivel: 2, 8, 18, 25, 8, 2
Propiedades Atómicas
Electronegatividad: 1.2 (escala de Pauling)
Radio Atómico (calc): 231 pm (radio de Bohr)
Estado(s) de oxidación: 2, 3
1.ª Energía de ionización: 547,1 kJ/mol
2.ª Energía de ionización: 1085 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 5244 kg/m3
Punto de fusión: 1099 K (700 °C)
Punto de ebullición: 1800 K (1737 °C)
Entalpía de fusión: 143.5 kJ/mol
Presión de vapor: 144
Varios
Estructura cristalina: Cúbica centrada en el cuerpo
N° CAS: 7440-53-1
Calor Específico: 180 J/(K·kg)
Conductividad Térmica: 13.9 W/(K·m)
Isótopos más estables
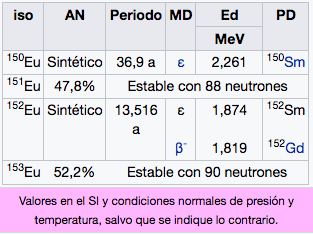
Gadolinio
Es un metal raro de color blanco plateado, es maleable y dúctil. Solo se encuentra en la naturaleza de forma combinada (sal).
Aplicaciones
Tiene usos médicos como contraste en la resonancia magnética nuclear. Se sabe que su uso es muy peligroso en personas con insuficiencia renal y es causante de una enfermedad muy grave conocida como fibrosis sistémica nefrogénica.
Historia
El gadolinio toma su nombre del mineral gadolinita, a su vez nombrado por el químico finlandés y geólogo Johan Gadolin.
En 1880, el químico suizo Jean Charles Galissard de Marignac observó las líneas espectroscópicas debidas al Gadolin en muestras de la gadolinita (que en realidad contiene relativamente poco gadolinio, pero suficiente para mostrarlo en un espectro), y en otro mineral separado, cerita. Este último mineral demostró tener mucho más del elemento que mostraba la nueva línea espectral, y Galissard de Marignac finalmente separó un óxido mineral de la cerita, que pensó que era el óxido de este nuevo elemento. Llamó al óxido "gadolinia." Dado que se dio cuenta de que la gadolinia era el óxido de un nuevo elemento, se le atribuye el descubrimiento del gadolinio. El químico francés Paul Émile Lecoq de Boisbaudran fue quien, en realidad, realizó la separación del gadolinio, metal de la gadolinia, en 1886.
Referencias
Información general
Nombre: Gadolinio
Símbolo: Gd
Número: 64
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: (157.25) u
Configuración Electrónica: [Xe]4f75d16s2
Dureza Mohs: 37
Electrones por Nivel: 2, 8, 18, 265, 9, 2
Propiedades Atómicas
Electronegatividad: 1.20 (escala de Pauling)
Radio Atómico (calc): 233 pm (radio de Bohr)
Estado(s) de oxidación: 3 (base fuerte)
1.ª Energía de ionización: 593.4 kJ/mol
2.ª Energía de ionización: 1170 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 7901 kg/m3
Punto de fusión: 1585 K (700 °C)
Punto de ebullición: 3523 K (1737 °C)
Entalpía de fusión: 10.05 kJ/mol
Presión de vapor: 24400
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-54-2
Calor Específico: 230 J/(K·kg)
Conductividad Térmica: 10.6 W/(K·m)
Isótopos más estables
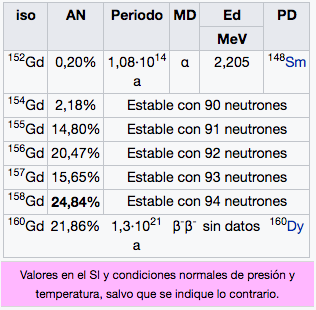
Terbio
Es un metal de transición interna de la familia de los lantánidos del Sistema Periódico. Se encuentra habitualmente como óxido en las tierras raras. Forma sales trivalentes de color blanco cuyas soluciones son incoloras. Su concentración en la corteza terrestre es de 0,09 ppm.
Características principales
El terbio es de color blanco-plateado, razonablemente estable al aire, maleable, dúctil y lo suficientemente blando como para ser cortado por un cuchillo. Existen dos variedades alotrópicas, con una temperatura de transformación de 1289 °C
Aplicaciones
Este elemento se utiliza en el dopaje de materiales usados en dispositivos de estado sólido, tales como el fluoruro de calcio, el tungstato de calcio y el molibdato de estroncio. El oxosulfato de gadolinio dopado con terbio es uno de los mejores colorantes en rayos X.
También se emplea como cristal estabilizador en células de combustible que operan a elevadas temperaturas, junto al óxido de circonio, en aleaciones y en la producción de componentes electrónicos. Su óxido se utiliza en los fósforos verdes de lámparas fluorescentes y tubos de imagen. El borato de terbio y sodio se aplica también en electrónica.
Historia
El terbio fue descubierto en 1843 por el químico sueco Carl Gustaf Mosander, que lo detectó como impureza en óxido de itrio. Su nombre se debe a la localidad sueca Ytterby. No fue aislado en estado puro hasta 1905 cuando se hicieron habituales las nuevas técnicas de intercambio de iones. Su aislamiento fue hecho por primera vez por Georges Urbain.
Este elemento se clasifica como tierra rara. El término "rara" puede conducir a equívoco, pues el terbio es más común que metales como la plata o el mercurio. Esta terminología poseía otro significado para los químicos de antaño. Se utilizaba porque los elementos clasificados como tales eran muy difíciles de separar unos de otros. No eran raros en la Tierra, sino que eran raramente usados para algo.
Obtención
El terbio no se encuentra nunca en estado libre en la naturaleza, sino contenido en diversos minerales como la cerita, la gadolinita, la monazita, la xenotima y la euxenita, algunos de ellos con un contenido inferior al 1% de terbio.
Referencias
1. «Descubiertos en el fondo del Pacífico grandes depósitos de raros minerales». Consultado el 4 de julio de 2011.
2. Jesús Peñas Cano. Desarrollo de materiales educativos para la enseñanza de las ciencias. copyright 2004.
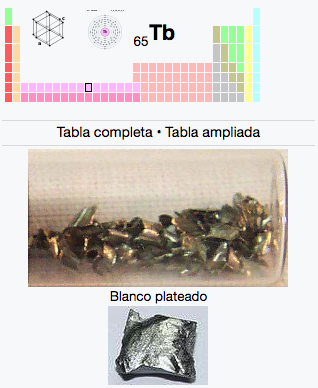
Información general
Nombre: Terbio
Símbolo: Tb
Número: 65
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: 158.95234 u
Configuración Electrónica: [Xe]6s24f9
Electrones por Nivel: 2, 8, 18, 27, 8, 2
Propiedades Atómicas
Electronegatividad: 1.20 (escala de Pauling)
Radio Atómico (calc): 225 pm (radio de Bohr)
Estado(s) de oxidación: 4
1.ª Energía de ionización: 565.8 kJ/mol
2.ª Energía de ionización: 1110 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8219 kg/m3
Punto de fusión: 1629 K (700 °C)
Punto de ebullición: 3503 K (1737 °C)
Entalpía de fusión: 10.8 kJ/mol
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-27-9
Calor Específico: 180 J/(K·kg)
Conductividad Térmica: 11.1 W/(K·m)
Isótopos más estables
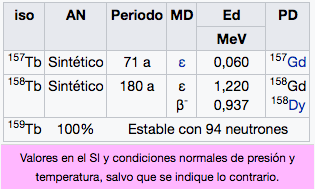
Disprosio
El disprosio es un elemento químico cuyo símbolo es Dy y su número atómico es 66. Es un metal de transición de color blanco plata, incluido en el grupo de los lantánidos o tierras raras. Fue identificado por primera vez en 1886 por Paul Émile Lecoq de Boisbaudran, pero no fue posible obtener una muestra pura hasta la década de 1950, con el método de intercambio iónico. En la naturaleza el disprosio se encuentra formado por 7 isótopos, y no existe en la corteza terrestre en forma aislada sino en compuestos junto con otros lantánidos.
Características principales
El disprosio es una tierra rara que presenta brillo metálico plateado. Es tan blando que puede ser cortado con una navaja, y puede ser procesado por máquinas sin emitir chispas, si se evita el sobrecalentamiento. Sus propiedades pueden verse muy afectadas por cantidades muy pequeñas de impurezas
Aplicaciones
El disprosio se usa, en conjunción con vanadio y otros elementos, como componente de materiales para láseres; su alta sección eficaz de absorción de neutrones térmicos y su alto punto de fusión también sugieren su utilidad para barras de control nuclear. Un óxido mixto de disprosio y níquel forma materiales que absorben los neutrones y no se contraen ni dilatan bajo bombardeo de neutrones prolongado, y que se usan para barras de control en reactores nucleares. Algunos calcogenuros de disprosio y cadmio son fuentes de radiación infrarroja para el estudio de reacciones químicas. El disprosio también se usa en la fabricación de discos compactos.
Historia
En 1878, se descubrieron minerales de erbio que contenían óxidos de holmio y tulio. En París en 1886 el químico francés Paul Émile Lecoq de Boisbaudran, mientras trabajaba con el óxido de holmio, consiguió separar óxido de disprosio a partir de este.11 Su procedimiento para separar el disprosio se basaba en disolver el óxido de disprosio en ácido, y luego añadir amoníaco para precipitar el hidróxido. Sin embargo sólo lo obtuvo a partir de su óxido después de 30 intentos. Por ello denominó disprosio al nuevo elemento, del griego dysprositos (δυσπρόσιτος), que significa "difícil de obtener". Aun así, el elemento no fue separado en una forma pura hasta después del desarrollo de las técnicas de intercambio de iones desarrolladas por Frank Spedding en la Universidad Estatal de Iowa a comienzos de la década de 1950
Referencias
1. Emsley, John (2001). Nature's Building Blocks. Oxford: Oxford University Press. pp. 129-132. ISBN 0-19-850341-5.
2. «Chemical reactions of Dysprosium». Webelements. Consultado el 16 de agosto de 2012.
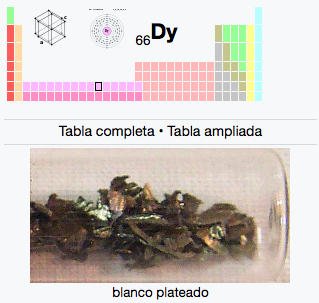
Información general
Nombre: Disprosio
Símbolo: Dy
Número: 66
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: 162.500 u
Configuración Electrónica: [Xe]6s24f10
Dureza Mohs: 1,25
Electrones por Nivel: 2, 8, 18, 28, 8, 2
Propiedades Atómicas
Electronegatividad: 1.22 (escala de Pauling)
Radio Atómico (calc): 228 pm (radio de Bohr)
Estado(s) de oxidación: 3
1.ª Energía de ionización: 573.0 kJ/mol
2.ª Energía de ionización: 1130 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8551 kg/m3
Punto de fusión: 1680 K (700 °C)
Punto de ebullición: 2840 K (1737 °C)
Entalpía de fusión: 11.06 kJ/mol
Varios
Estructura cristalina: Hexagonal
Calor Específico: 170 J/(K·kg)
Conductividad Térmica: 10.7 W/(K·m)
Isótopos más estables
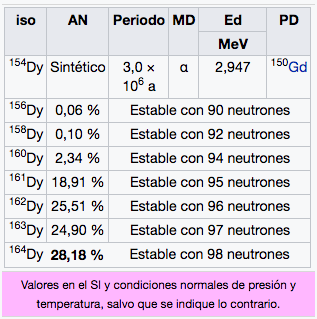
Holmio
El holmio es un elemento químico cuyo nombre deriva del nombre en Latín de la ciudad de Estocolmo, Holmia. Fue descubierto por Marc Delafontaine y Jacques-Louis Soret, quienes en 1878 observaron las inusuales bandas de absorción espectrográficas de un elemento entonces desconocido.
Características principales
El metal es paramagnético, pero a medida que la temperatura disminuye se convierte en antiferromagnético y luego al sistema ferromagnético.
Aplicaciones
El holmio tiene pocas aplicaciones prácticas, aunque se ha usado como catalizador en reacciones químicas industriales y también para la fabricación de algunos dispositivos electrónicos. En medicina se utiliza el láser de holmio.
Referencias
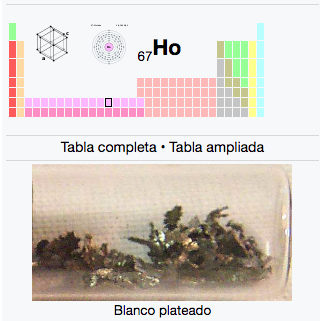
Información general
Nombre: Holmio
Símbolo: Ho
Número: 67
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: 164.9304 u
Configuración Electrónica: [Xe]6s24f11
Dureza Mohs: 1,25
Electrones por Nivel: 2, 8, 18, 29, 8, 2
Propiedades Atómicas
Electronegatividad: 1.23 (escala de Pauling)
Radio Atómico (calc): 158 pm (radio de Bohr)
Estado(s) de oxidación: 3, 2, 1
1.ª Energía de ionización: 581 kJ/mol
2.ª Energía de ionización: 1140 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8800 kg/m3
Punto de fusión: 1734 K (700 °C)
Punto de ebullición: 2873 K (1737 °C)
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-60-0
Calor Específico: 160 J/(K·kg)
Conductividad Térmica: 16.2 W/(K·m)
Isótopos más estables

Erbio
El erbio es un elemento un tanto raro de color plateado perteneciente a los lantánidos y que aparece asociado a otros lantánidos en el mineral gadolinita procedente de Ytterby (Suecia).
Características principales
El erbio es un elemento trivalente, maleable, relativamente estable en el aire y no se oxida tan rápidamente como otros metales de las tierras raras. Sus sales son rosadas y el elemento origina un característico espectro de absorción en el espectro visible, ultravioleta y cerca del infrarrojo. Su óxido es la erbia. Las propiedades del erbio están muy influenciadas por la cantidad y tipo de impurezas presentes. El erbio no tiene papel biológico conocido alguno aunque algunos creen que es capaz de estimular el metabolismo. Los cristales o vidrios dopados con erbio pueden ser utilizados en amplificación óptica, en la que los iones de erbio son bombeados ópticamente alrededor de las longitudes de ondas de 980 nm o 1480 nm e irradian luz en longitudes de onda de 1550 nm. Este proceso puede ser utilizado para crear láseres y amplificadores ópticos. La longitud de onda de 1550 nm es especialmente importante para las comunicaciones ópticas porque las fibras ópticas normalizadas tienen pérdidas mínimas en esta longitud de onda.
Aplicaciones
Las aplicaciones del erbio son variadas; es utilizado habitualmente como filtro fotográfico y debido a su resistencia es útil como aditivo metalúrgico.
Otros usos son:
- Se utiliza en tecnología nuclear como amortiguador de neutrones.
- Utilizado como dopante en amplificadores de fibra óptica.
- Cuando se adiciona al vanadio como elemento de aleación el erbio rebaja la dureza y mejora el mecanizado.
- El óxido de erbio tiene un color rosa y se utiliza a veces como colorante para vidrios y esmaltes para porcelanas. Ese mismo vidrio se utiliza a menudo en gafas de sol y joyería barata.
Historia
El erbio (de Ytterby, una ciudad sueca) fue descubierto por Carl Gustaf Mosander en 1843. Mosander separó la "itria" del mineral gadolinita en tres fracciones que denominó itria, erbia, y terbia. Nombró al nuevo elemento en honor a la ciudad de Ytterby, donde se encontraron grandes concentraciones de itria y erbio. La erbia y la terbia, sin embargo, se confundían por aquellos tiempos. Después de 1860, la terbia fue renombrada como erbia y en 1877 lo que era conocido como erbia se llamó terbia. Óxido de erbio (Er2O3) bastante puro fue aislado de forma independiente por Georges Urbain y Charles James en 1905. Hasta 1934 no se consiguió obtener erbio lo suficientemente puro hasta cuando se consiguió reducir el cloruro anhidro con vapor de potasio.
Obtención
Como otras tierras raras, el erbio nunca se encuentra como elemento libre en la naturaleza pero sí en minerales como la monazita. Históricamente siempre ha sido difícil y caro separar las tierras raras unas de otras a partir de sus menas pero las técnicas de producción basadas en el intercambio iónico desarrolladas a finales del siglo XX ha abaratado apreciablemente el coste de todas las tierras raras y sus compuestos químicos. Las principales fuentes comerciales de erbio son los minerales xenotimo y euxenita y recientemente las arcillas de adsorción iónica de China meridional. En las muestras ricas de itrio de este tipo de mena, el itrio representa alrededor de los 2/3 de la masa total; y la erbia (óxido de erbio) representa entre el 4 y 5%. Esta cantidad de erbio es suficiente para conferir un color rosa característico a la disolución cuando la muestra rica en erbio se disuelve en medio ácido. Este comportamiento cromático es extraordinariamente similar al que Mosander y los demás científicos que trabajaron con las tierras raras podrían haber visto en sus muestras de gadolinita procedente de Ytterby.
Referencias
1. Los Alamos National Laboratory - Erbium
2. WebElements.com - Erbium.
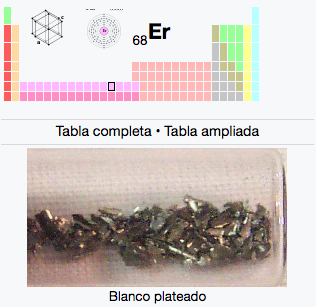
Información general
Nombre: Erbio
Símbolo: Er
Número: 68
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: 167.259 u
Configuración Electrónica: [Xe]6s24f12
Electrones por Nivel: 2, 8, 18, 30, 8, 2
Propiedades Atómicas
Electronegatividad: 1.24 (escala de Pauling)
Radio Atómico (calc): 226 pm (radio de Bohr)
Estado(s) de oxidación: 3
1.ª Energía de ionización: 589,3 kJ/mol
2.ª Energía de ionización: 1150 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 9066 kg/m3
Punto de fusión: 1795 K (700 °C)
Punto de ebullición: 3146 K (1737 °C)
Entalpía de fusión: 17.2 kJ/mol
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-52-0
Calor Específico: 170 J/(K·kg)
Conductividad Térmica: 14.3 W/(K·m)
Isótopos más estables
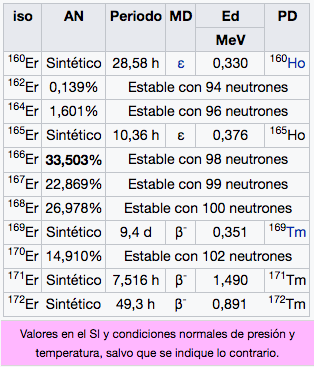
Tulio
Fue descubierto por Per Teodor Cleve en Suecia en el año 1879. Su nombre procede del antiguo nombre de Escandinavia en latín, Thule, ya que fue descubierto en esa región.
Características principales
El metal de Tulio puro posee un lustre plateado. Es medianamente estable al ser expuesto al aire, pero debe ser protegido de la humedad. El metal es blando, maleable y dúctil.
Obtención
El Tulio es el menos abundante de los lantánidos (el prometio es menos abundante que el Tulio, pero no se lo encuentra naturalmente en la Tierra). Es un metal blando, con un lustre gris plateado brillante. A pesar de su alto precio y escasez, el tulio es utilizado como fuente de radiación en los equipos de rayos X portátiles y láseres de estado sólido.
Referencias
1. C. R. Hammond (2000). The Elements, in Handbook of Chemestry and Physics 81st edition. CRC press. ISBN 0849304814.
2. Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. p. 934. ISBN 0070494398. Consultado el 6 de junio de 2009.
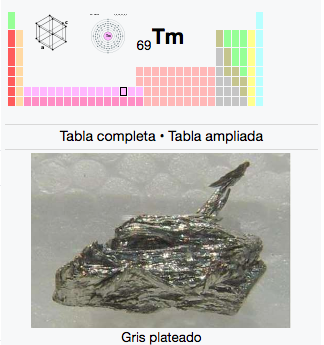
Información general
Nombre: Tulio
Símbolo: Tm
Número: 69
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: 168.934 u
Configuración Electrónica: [Xe]6s24f13
Electrones por Nivel: 2, 8, 18, 31, 8, 2
Propiedades Atómicas
Electronegatividad: 1.25 (escala de Pauling)
Radio Atómico (calc): 222 pm (radio de Bohr)
Estado(s) de oxidación: 3
1.ª Energía de ionización: 596.7 kJ/mol
2.ª Energía de ionización: 1160 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 9321 kg/m3
Punto de fusión: 1818 K (700 °C)
Punto de ebullición: 2220 K (1737 °C)
Entalpía de fusión: 16.84 kJ/mol
Varios
Estructura cristalina: Hexagonal
N° CAS: 7440-30-4
Calor Específico: 160 J/(K·kg)
Conductividad Térmica: 16.8 W/(K·m)
Isótopos más estables
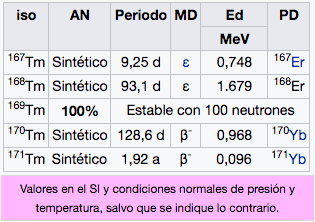
Iterbio
El iterbio o yterbio es un elemento químico de la tabla periódica que tiene el símbolo Yb y el número atómico 70. El iterbio es un elemento metálico plateado blando, una tierra rara de la serie de los lantánidos que se halla en la gadolinita, la monazita y el xenotimo. El iterbio se asocia a veces con el itrio u otros elementos relacionados y se usa en algunos aceros. El iterbio natural es una mezcla de siete isótopos estables.
Características principales
El iterbio es un elemento blando, maleable y bastante dúctil que exhibe un lustre plateado brillante. Es una tierra rara, fácilmente atacable y disoluble con ácidos minerales, reacciona lentamente con el agua, y se oxida al aire.
Aplicaciones
Un isótopo del iterbio se ha usado como fuente de radiación alternativa para una máquina de rayos X portátil cuando no se disponía de electricidad. Su metal también puede usarse para mejorar el refinamiento del grano, la resistencia y otras propiedades mecánicas del acero inoxidable. Algunas aleaciones de iterbio se usan en odontología. Hay pocos usos más de este elemento.
Historia
El iterbio (de Ytterby, una ciudad de Suecia) fue descubierto por el químico suizo Jean Charles Galissard de Marignac en 1878. Marignac encontró un nuevo componente en la tierra entonces llamada erbia, y lo llamó iterbia (por Ytterby, la ciudad sueca en la que encontró dicho componente). Él sospechaba que la iterbia era un compuesto de un nuevo elemento que bautizó iterbio (que era de hecho la primera tierra rara en ser descubierta).
Obtención
El iterbio se encuentra con otras tierras raras en varios minerales raros. Se obtiene comercialmente con mayor frecuencia a partir de la arena monazita.
Información general
Nombre: Iterbio
Símbolo: Yb
Número: 70
Serie Química: Lantánidos
Grupo: -
Período: 6
Bloque: f
Masa Atómica: 173.04 u
Configuración Electrónica: [Xe]4f146s2
Electrones por Nivel: 2, 8, 18, 32, 8, 2
Propiedades Atómicas
Electronegatividad: 1.1 (escala de Pauling)
Radio Atómico (calc): 222 pm (radio de Bohr)
Estado(s) de oxidación: 3
1.ª Energía de ionización: 603.4 kJ/mol
2.ª Energía de ionización: 1174.8 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 6965 kg/m3
Punto de fusión: 1097 K (700 °C)
Punto de ebullición: 1467 K (1737 °C)
Entalpía de fusión: 7.66 kJ/mol
Varios
Estructura cristalina: Cúbica centrada en las caras
N° CAS: 7440-64-4
Calor Específico: 150 J/(K·kg)
Conductividad Térmica: 34.9 W/(K·m)
Isótopos más estables
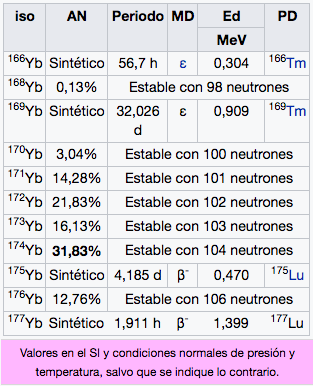
Lutecio
El lutecio es un elemento químico, de número atómico 71, cuyo símbolo químico es Lu. A pesar de ser uno de los elementos del bloque d, con frecuencia aparece incluido entre los lantánidos (tierras raras), ya que con estos comparte muchas propiedades. De todos ellos es el elemento más difícil de aislar, lo cual justifica su carestía y los relativamente pocos usos que se le han encontrado.
Características principales
El lutecio es un metal trivalente, de color blanco plateado, resistente a la corrosión y, en presencia de aire, relativamente estable. De todas las tierras raras es el elemento más pesado y duro.
Aplicaciones
Este metal se emplea como catalizador en el craqueo del petróleo en las refinerías, y en diversos procesos químicos, como alquilación, hidrogenación y polimerización. También se están investigando radioisótopos de lutecio para ser aplicados en medicina nuclear en tratamientos terapéuticos.
Obtención
En la naturaleza se encuentra con la mayoría del resto de tierras raras, pero nunca en solitario, nativo. De todos los elementos presentes en la naturaleza es el menos abundante. La principal mena de lutecio comercialmente explotable es la monacita, que contiene 0,003% de Lu.
Referencias

Información general
Nombre: Lutecio
Símbolo: Lu
Número: 71
Serie Química: Lantánidos
Grupo: 3
Período: 6
Bloque: d
Masa Atómica: 174.967 u
Configuración Electrónica: [Xe]4f145d16s2
Electrones por Nivel: 2, 8, 18, 32, 9, 2
Propiedades Atómicas
Electronegatividad: 1.27 (escala de Pauling)
Radio Atómico (calc): 217 pm (radio de Bohr)
Radio Covalente: 160 pm
Estado(s) de oxidación: 3
1.ª Energía de ionización: 523.5 kJ/mol
2.ª Energía de ionización: 1340 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 9841 kg/m3
Punto de fusión: 1925 K (700 °C)
Punto de ebullición: 3675 K (1737 °C)
Entalpía de fusión: 18.6 kJ/mol
Presión de vapor: 2460
Varios
Estructura cristalina: Hexagonal
N° CAS: 7439-94-3
Calor Específico: 150 J/(K·kg)
Conductividad Térmica: 16.4 W/(K·m)
Isótopos más estables
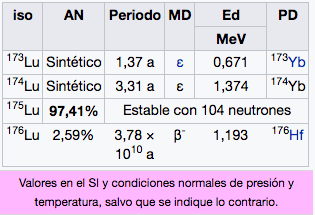
Torio
El torio es un elemento químico, de símbolo Th y número atómico 90, de la serie de los actínidos. Se encuentra en estado natural en los minerales monacita, torita y torianita. En estado puro es un metal blando de color blanco-plata que se oxida lentamente. Si se tritura finamente y se calienta, arde y emite luz blanca.
El torio pertenece a la familia de las sustancias radiactivas, si bien su periodo de semidesintegración es extremadamente largo. Su potencial como combustible nuclear, como material fértil, se debe a que presenta una alta sección eficaz frente a neutrones lentos (térmicos), derivando en protactinio-233, que rápidamente se desintegra en uranio-233, el cual es un isótopo fisible que puede sostener una reacción nuclear en cadena. Esta aplicación todavía está en fase de desarrollo.
Historia
El torio se llamó así en honor de Thor, el dios nórdico del relámpago y la tormenta. Jöns Jakob Berzelius lo aisló por primera vez en 1828. En el último decenio del siglo XIX, los investigadores Pierre Curie y Marie Curie descubrieron que este elemento emitía radiactividad.

Aplicaciones del torio
Aparte de su incipiente uso como combustible nuclear, el torio metálico o alguno de sus óxidos se utilizan en las áreas siguientes:
- Incorporación al wolframio metálico para fabricar filamentos de lámparas eléctricas.
- Aplicaciones en material cerámico de alta temperatura.
- Como:
- 1. Agente de aleación en estructuras metálicas.
- 2. Componente básico de la tecnología del magnesio.
- 3. Catalizador en química orgánica.
- Fabricación de:
- 1. Lámparas electrónicas.
- 2. Lentes de alta calidad para instrumentos de precisión. (El óxido de torio añadido al vidrio mejora sus propiedades difractivas).
- 3. Electrodos especiales para soldadura TIG (Tungsten Inert Gas), también conocida como soldadura GTAW (Gas Tungsten Arc Welding). La aleación con wolframio favorece mayor emisividad de electrones del electrodo. Esto facilita el encendido y permite que el electrodo de wolframio funcione a menor temperatura y aporte el mismo rendimiento en la pieza que se trabaje.
Existe el problema de que la temperatura de trabajo del electrodo de wolframio puro era aproximadamente la temperatura de fusión del wolframio: 3 400 °C. Al fundirse, esto dañaba el perfil del electrodo. Este inconveniente también se evita con electrodos que incorporan otros dopantes, como cerio, lantano o circonio. - Detector de oxígeno en la industria electrónica.
Últimamente (2018) se aplica como isótopo radiactivo en la deteccion de fósiles superior al carbono 14.
Desintegración nuclear del torio
Cuando un átomo de torio 232 (232Th) se desintegra emite una partícula alfa, constituida por dos protones y dos neutrones. La emisión de la partícula alfa reduce el número atómico del 232Th en dos unidades, y el número másico en cuatro, por lo cual se convierte en el isótopo 228 de otro elemento: el radio 228. Posteriores desintegraciones complementan la serie del torio. Este proceso continúa hasta que finalmente se genera un elemento no radiactivo, y por tanto estable: el plomo-208, o torio C.
El periodo de semidesintegración del 232Th es muy elevado (véase en la tabla), por lo que durante miles de millones de años libera radiactividad. A su vez, esto implica que la cantidad de radiactividad que emite en un periodo pequeño (p. ej. un día) sea muy pequeña.
El torio puede aprovecharse como fuente de energía en un Reactor reproductor termal (la reacción comienza a partir de una carga inicial con uranio enriquecido o plutonio y se sostenerse mediante U 233, que se genera del torio por captación de neutrones lentos hasta el total aprovechamiento del mismo, al mismo tiempo que se obtiene energía con la fisión del U 233).
Referencias
1. Educaplus.org. «Elementos químicos: Torio». Consultado el 24 de marzo de 2011.
2. Historia del torio
3. Aplicaciones del torio
Información general
Nombre: Torio
Símbolo: Th
Número: 90
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 232,0381 u
Configuración Electrónica: [Rn] 7s2 5f2
Dureza Mohs: 3,0
Electrones por nivel: 2, 8, 18, 32, 18, 10, 2
Propiedades Atómicas
Radio medio: 180 pm
Electronegatividad: 1,3 (escala de Pauling)
Radio atómico (calc): 179 pm (radio de Bohr)
Radio covalente: 206±6 pm
Estado(s) de oxidación: 4, 3, 2 (base débil)
1.ª energía de ionización: 587 kJ/mol
2.ª energía de ionización: 1110 kJ/mol
3.ª energía de ionización: 193 kJ/mol
4.ª energía de ionización: 2780 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 11724 kg/m3
Punto de fusión: 2028 K (1755 °C)
Punto de ebullición: 5061 K (4788 °C)
Entalpía de vaporización: 514,4 kJ/mol
Entalpía de fusión: 16,1 kJ/mol
Varios
Estructura cristalina: Cúbica centrada en las caras
N.º CAS: 7440-29-1
Calor específico: 120 J/(K·kg)
Conductividad térmica: 54 W/(K·m)
Módulo elástico: 79 GPa
Coeficiente de Poisson: 0,27
Velocidad del sonido: 2 490 m/s a 293,15 K (20 °C)
Isótopos más estables
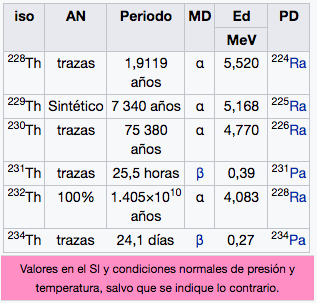
Protactinio
El protactinio es un elemento químico de la tabla periódica cuyo símbolo es Pa y su número atómico es 91.
Características notables
El protactinio es un elemento metálico plateado que pertenece al grupo de los actínidos, que presenta un brillo metálico intenso.
Es superconductor por debajo de 1.4 K.
Aplicaciones
Debido a su escasez, alta radioactividad y toxicidad, actualmente no existen usos para el protactinio fuera de la investigación científica básica.
El Protactinio-231 (que se forma por la desintegración alfa del Uranio-235 seguido de una desintegración beta del Torio-231) podría quizás mantener una reacción nuclear en cadena y, en principio, podría ser usado para construir una bomba nuclear. La masa crítica, según Walter Seifritz, es 750±180 kg. Otros autores concluyen que no es posible una reacción en cadena usando 231Pa.
Historia
Dimitri Ivánovic Mendeléiev predijo en 1871 que debería existir un elemento con número atómico igual a 91 y que aparecería en la tabla periódica entre el torio y el uranio. En 1900 William Crookes aisló el protactinio como un material radiactivo formado a partir del uranio, pero que no consiguió identificarlo.
El protactinio fue identificado por primera vez en 1913 cuando Kasimir Fajans y O.H. Göhring encontraron el isótopo de corta vida 234mPa, con una vida media de, en torno, 1,17 minutos, durante sus estudios de la cadena de decaimiento del 238U. Dieron al nuevo elemento el nombre de Brevium (latín: brevis, es decir, breve). El nombre se cambió a Protoactinium (progenitor del actinio) en 1918 cuando dos grupos de científicos (Otto Hahn y Lise Meitner de Alemania, y Frederick Soddy y John Cranston del Reino Unido) descubrieron de manera independiente el 231Pa, y acortaron el nombre a protactinium (en español, protoactinio) en 1949.
Aristid V. Grosse preparó 2 mg de Pa2O5 en 1927, y más tarde consiguió aislar protactinio por primera vez en 1934 de 0,1 mg de Pa2O5, convirtiendo primero el óxido en un ioduro y después rompiéndolo a alto vacío usando un filamento calentado mediante una corriente eléctrica produciendo la reacción 2PaI5 → 2Pa + 5I2 (proceso Van Arkel-De Boer).
En 1961, la Autoridad de la energía atómica del Reino Unido fue capaz de producir 125 g de protactinio puro al 99,9% procesando 60 toneladas de material de desecho en un proceso de 12 etapas con un gasto de 500.000 $. Esta fue la única fuente de este elemento durante muchos años y se dice que fue vendido a los laboratorios a un coste de 2800 $/g en los años sucesivos.
Abundancia y obtención
El protactinio natural se produce por la desintegración radiactiva del uranio y el torio, por tanto se encuentra en todos sus minerales, siendo su concentración proporcional al porcentaje de dichos elementos. En la pechblenda se halla en una cantidad de aproximadamente una parte de 231Pa en 10 millones de mena (es decir, 0,1 ppm). Algunas minas de la República Democrática del Congo llegan a tener en torno a 3 ppm.
Compuestos
Compuestos conocidos del protactinio:
- Fluoruros
- PaF4
- PaF5
- Cloruros
- PaCl4
- PaCl5
- Bromuros
- PaBr4
- PaBr5
- Ioduros
- PaI3
- PaI4
- PaI5
- Óxidos
- PaO
- PaO2
- Pa2O5
Isótopos
Se han caracterizado 29 radioisótopos del protactinio siendo los más estables el 231Pa, con una vida media de 32.760 años; el 233Pa, con una vida media de 26,967 días; y el 230Pa con una vida media de 17,4 días. El resto de isótopos radiactivos tienen vidas medias inferiores a 1,6 días y la mayoría tienen vidas medias menores de 1,8 segundos. Este elemento también tiene dos metaestados, 217mPa (vida media de 1,15 milisegundos) y 234mPa (vida media de 1,17 minutos).
El modo de desintegración primario del isótopo más estable 231Pa y de aquellos más ligeros es la desintegración alfa mientras que para los isótopos más pesados es la desintegración beta. Los productos primarios de la desintegración de los isótopos más ligeros (231Pa o más ligeros) son isótopos del actinio (Ac) mientras que los isótopos más pesados producen isótopos del uranio (U).
Precauciones
El protactinio es tóxico y altamente radiactivo. Por este motivo, requiere precauciones similares a las usadas cuando se maneja plutonio.
Referencias
1. Fowler, R. D. et al. (1965). «Superconductivity of Protactinium». Phys. Rev. Lett. 15 (22): 860. Bibcode:1965PhRvL..15..860F. doi:10.1103/PhysRevLett.15.860.
2. Emsley, John (2001). Nature's Building Blocks ((Hardcover, First Edition) edición). Oxford University Press. pp. page 347. ISBN 0-19-850340-7.
Información general
Nombre: Protactinio
Símbolo: Pa
Número: 91
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 231.03588 u
Configuración Electrónica: [Rn] 7s2 5f2 6d1
Electrones por nivel: 2, 8, 18, 32, 20, 9, 2
Propiedades Atómicas
Radio medio: 180 pm
Electronegatividad: 1,5 (escala de Pauling)
Radio atómico (calc): 163 pm (radio de Bohr)
Radio covalente: 200 pm
Estado(s) de oxidación: 2, 3, 4, 5 (base débil)
1.ª energía de ionización: 568 kJ/mol
Propiedades Físicas
Densidad: 15370 kg/m3
Punto de fusión: 2113 K (1840 °C)
Punto de ebullición: 4300 K (4027 °C)
Entalpía de vaporización: 470 kJ/mol
Entalpía de fusión: 15 kJ/mol
Presión de vapor: 5,1 × 10-5 Pa a 2200 K
Varios
Estructura cristalina: Tetragonal
N.º CAS: 7440-13-3
Calor específico: 120 J/(K·kg)
Conductividad eléctrica: 5,29 × 106 m-1 S/m
Conductividad térmica: 47 W/(K·m)
Isótopos más estables
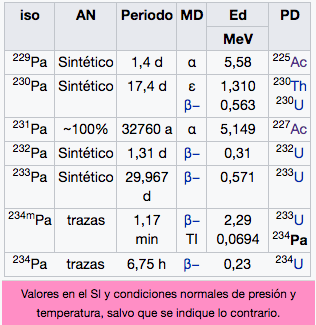
Uranio
El uranio es un elemento químico metálico de color plateado-grisáceo de la serie de los actínidos, su símbolo químico es U y su número atómico es 92. Por ello posee 92 protones y 92 electrones, con una valencia de 6. Su núcleo puede contener entre 142 y 146 neutrones, sus isótopos más abundantes son el 238U que posee 146 neutrones y el 235U con 143 neutrones. El uranio tiene el mayor peso atómico de entre todos los elementos que se encuentran en la naturaleza. El uranio es aproximadamente un 70 % más denso que el plomo, aunque menos denso que el oro o el wolframio. Es levemente radiactivo. Fue descubierto como óxido en 1789 por M. H. Klaproth que lo llamó así en el honor del planeta Urano que acababa de ser descubierto en 1781.
Características
En la naturaleza se presenta en muy bajas concentraciones (unas pocas partes por millón o ppm) en rocas, tierras, agua y los seres vivos. Para su uso el uranio debe ser extraído y concentrado a partir de minerales que lo contienen, como por ejemplo la uranitita (ver minería del uranio). Las rocas son tratadas químicamente para separar el uranio, convirtiéndolo en compuestos químicos de uranio. El residuo se denomina estéril. Esos estériles contienen las mismas sustancias radioactivas que poseía el mineral original y que no fueron separadas, como el radio, el torio o el potasio.
El uranio natural está formado por tres tipos de isótopos: uranio-238 (238U), uranio-235 (235U) y uranio-234 (234U). De cada gramo de uranio natural el 99,284 % de la masa es uranio-238, el 0,711 % uranio-235, y el 0,0085 % uranio-234. La relación uranio-238/uranio-235 es constante en la corteza terrestre, salvo ciertas excepciones, como ocurre en los yacimientos de Oklo donde hay evidencias de que hace unos 2000 millones de años se produjeron reactores nucleares naturales.
El uranio decae muy lentamente emitiendo una partícula alfa. El periodo de semidesintegración del uranio-238 es aproximadamente 4470 millones de años y el del uranio-235 es 704 millones de años, lo que los convierte en útiles para estimar la edad de la Tierra (véase fechado mediante uranio-torio, fechado mediante uranio-plomo y fechado mediante uranio-uranio). Muchos usos contemporáneos del uranio hacen uso de estas propiedades nucleares únicas. El uranio-235 se distingue por ser el único elemento que se encuentra en la naturaleza que es un isótopo fisionable. El uranio-238 es fisionable por neutrones rápidos, y también es un material fértil (que puede transmutarse en un reactor nuclear en plutonio-239 que es fisionable). Es posible producir el isótopo fisionable artificial, uranio-233, a partir de torio natural, lo que desempeña un rol importante en la tecnología nuclear. Mientras que el uranio-238 posee una pequeña probabilidad de fisión espontánea o al ser bombardeado por neutrones rápidos, el uranio-235 posee una mayor probabilidad de fisionarse al ser bombardeado por neutrones térmicos, por lo que es la principal reacción responsable de la generación de calor en un reactor nuclear, y es la principal fuente de material fisible para las armas nucleares. Ambos usos son posibles por la capacidad del uranio de sostener una reacción nuclear en cadena.
El uranio, fundamentalmente el U-238 desempeña un papel fundamental en conservar el campo magnético terrestre.
El uranio empobrecido (uranio-238) es utilizado en penetradores de energía cinética y protecciones para vehículos blindados.
El 235U se utiliza como combustible en centrales nucleares y en algunos diseños de armamento nuclear. Para producir combustible, el uranio natural es separado en dos porciones. La porción combustible tiene más 235U que lo normal, denominándose uranio enriquecido, mientras que la porción sobrante, con menos U235 que lo normal, se llama uranio empobrecido. El uranio natural, enriquecido o empobrecido es químicamente idéntico. El uranio empobrecido es el menos radiactivo y el enriquecido el más radiactivo.
En el año 2009, la sonda japonesa SELENE descubrió por primera vez indicios de uranio en la Luna.
Origen
Junto con todos los elementos con pesos atómicos superiores al del hierro, el uranio se origina de forma natural durante las explosiones de las supernovas. El proceso físico determinante en el colapso de una supernova es la gravedad. Los valores tan elevados de gravedad que se dan en las supernovas son los que generan las capturas neutrónicas que dan lugar a átomos más pesados, entre ellos el uranio y el protactinio.
Reservas de uranio
La producción mundial de uranio fue en 2009 de 50 572 toneladas, de las que el 27,3 % se extrajo en minas de Kazajistán, el 20,1 % en Canadá, el 15,7 % en Australia, el 9,1 % en Namibia, el 7 % en Rusia, y el 6,4 % en Níger.
La OCDE y el OIEA publican periódicamente un informe llamado Uranium: Resources, Production and Demand, conocido como "Red Book", donde se hace una estimación de las reservas mundiales de uranio por países. Los grandes productores son Canadá, Australia, Kazajistán, Rusia, Níger, República Democrática del Congo, Namibia y Brasil. También hay prospecciones y yacimientos de uranio en distintos países como Colombia (en la serranía del Perijá, en la frontera compartida con Venezuela.), Perú (en la provincia de Carabaya en la región Puno) y España, entre otras zonas.
Según este informe, los recursos mundiales de uranio son suficientes para satisfacer las necesidades actuales hasta un máximo de ochenta y cinco años. Se estima que la cantidad total de existencias de uranio convencional, que puede ser explotado por menos de 130 USD por kg, es de unos 4,7 millones de toneladas, que permitirían abastecer la demanda de uranio para generación nuclear de electricidad durante 85 años. Sin embargo, los recursos mundiales de uranio en total se consideran mucho más altos. Basándose en la evidencia geológica y el conocimiento de los fosfatos de uranio, el estudio considera más de 35 millones de toneladas disponibles para su explotación. A largo plazo, los supuestos avances en la tecnología nuclear permitirían una utilización mucho mejor de los recursos de uranio. Los reactores que se están diseñando supuestamente podrían extraer unas 30 veces más energía del uranio que los reactores de hoy, lo que aumentaría la duración de las reservas a 2550 años.
En 2025, la capacidad mundial de la energía nuclear se supone que crezca a entre 450 GWe (+22 %) y 530 GWe (+44 %) de la capacidad de generación actual de cerca de 370 GWe. Esto aumentará las necesidades de uranio anuales de entre 80 000 toneladas y 100 000 toneladas lo que consecuentemente reducirá las expectativas de la duración de las reservas naturales de uranio.
Aplicación
El principal uso del uranio en la actualidad es como combustible para los reactores nucleares que producen el 3 % de la energía generada por el ser humano en el mundo.[cita requerida] Para ello el uranio es enriquecido aumentando la proporción del isótopo U235 desde el 0,71 % que presenta en la naturaleza hasta valores en el rango 3-5 %.
El uranio empobrecido (con una proporción de U-235 inferior a la natural), producido como producto de desecho tras la utilización del uranio en centrales nucleares, es usado en la producción de municiones perforadoras y blindajes de alta resistencia; debido principalmente a su elevada densidad (unos 19 g/cm³), su fragmentación en trozos afilados y sobre todo a que es pirofórico (entra en combustión de forma espontánea al entrar en contacto con el aire a 600 ºC aproximadamente). Su uso además conlleva la dispersión de contaminación radiactiva, como ocurrió durante la Primera Guerra del Golfo.
Otros usos incluyen:
- Por su alta densidad, se utiliza el uranio en la construcción de estabilizadores para aviones, satélites artificiales y veleros (balastos/quillas).
- Se ha utilizado uranio como agregado para la creación de cristales de tonos fluorescentes verdes o amarillos.
- El largo periodo de semi-desintegración del isotopo 238U se utiliza para estimar la edad de la Tierra.
- El 238U se convierte en plutonio en los reactores reproductores. El plutonio puede ser usado en reactores o en armas nucleares.
- Algunos accesorios luminosos utilizan uranio, del mismo modo que lo hacen algunos químicos fotográficos (nitrato de uranio).
- Su alto peso atómico hace que el 238U pueda ser utilizado como un eficaz blindaje contra las radiaciones de alta penetración.
- El uranio en estado metálico es usado para los blancos de rayos X, para hacer rayos X de alta energía.
- El uranio empobrecido se usa como blindaje en los carros de combate modernos, también los misiles llevan uranio empobrecido en su espolón.
- Fertilizantes de fosfato a menudo contienen altos contenidos de uranio natural, debido a que el mineral del cual son hechos es típicamente alto en uranio.
La exposición humana
Una persona puede estar expuesta al uranio (o a sus descendientes radiactivos como el radón) por la inhalación de polvo en el aire o por la ingestión de agua y alimentos contaminados. La cantidad de uranio en el aire es muy pequeña, sin embargo, las personas que trabajan en las fábricas de procesado de fosfatos o fertilizantes, viven cerca de instalaciones donde se hicieron pruebas de armas nucleares, viven o trabajan cerca de un campo de batalla moderno donde se ha utilizado uranio empobrecido, o que viven o trabajan cerca de la exposición de una central térmica de carbón, las instalaciones de las minas de mineral de uranio, o instalaciones de enriquecimiento de uranio para combustible, pueden haber aumentado su exposición al uranio. Casas o estructuras que están sobre los depósitos de uranio (naturales o depósitos artificiales de escoria) pueden tener un aumento de la incidencia de la exposición al gas radón.
La mayoría del uranio ingerido se excreta naturalmente. Sólo el 0,5 % es absorbido cuando se ingieren formas insolubles de uranio, como el óxido, mientras que la absorción de los más solubles iones uranilo puede ser de hasta un 5 %. Sin embargo, los compuestos solubles de uranio tienden a pasar rápidamente a través de todo el cuerpo mientras que los compuestos de uranio insolubles, en especial cuando se inhala polvo en los pulmones, representan un riesgo de exposición más grave. Después de entrar en el torrente sanguíneo, el uranio absorbido tiende a la bioacumulación y la estancia durante muchos años en los tejidos óseos debido a la afinidad de uranio para los fosfatos. El uranio no se absorbe a través de la piel, y las partículas alfa liberadas por el uranio no pueden penetrar la piel.
Genotóxicos mutágenos procedentes de la exposición al uranio pueden ser tratado con terapia de quelación o por otros medios poco después de la exposición. El uranio asimilado se convierte en iones uranilo, que se acumulan en los huesos, el hígado, los riñones y los tejidos reproductivos. El uranio puede ser descontaminado de las superficies de acero y acuíferos.
Referencias
1. Morss, L.R.; Edelstein, N.M. and Fuger, J., ed. (2006). The Chemistry of the Actinide and Transactinide Elements (3rd edición). Netherlands: Springer. ISBN 9048131464.
2. «Health Concerns about Military Use of Depleted Uranium» (PDF). Archivado desde el original el 19 de abril de 2011.
Información general
Nombre: Uranio
Símbolo: U
Número: 190537363727
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 238,02891 u
Configuración Electrónica: [Rn] 5f3 6d1 7s2
Electrones por nivel: 2, 8, 18, 32, 21, 9, 2
Propiedades Atómicas
Radio medio: 175 pm
Electronegatividad: 1.38 (escala de Pauling)
Radio atómico (calc): 156 pm (radio de Bohr)
Radio covalente: 196±7 pm
Radio de van der Waals: 186 pm
Estado(s) de oxidación: 6, 5, 4, 3 (base débil)
1.ª energía de ionización: 597,6 kJ/mol
2.ª energía de ionización: 1420 kJ/mol
3.ª energía de ionización: 234 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 19,050 kg/m3
Punto de fusión: 1900 K (1627 °C)
Punto de ebullición: 2334 K (2061 °C)
Entalpía de vaporización: 789 kJ/mol
Entalpía de fusión: 15,48 kJ/mol
Varios
Estructura cristalina: ortorrómbica
Calor específico: 120 J/(K·kg)
Conductividad eléctrica: 3,8 × 106 S/m
Conductividad térmica: 27,6 W/(K·m)
Velocidad del sonido: 3155 m/s a 293,15 K (20 °C)
Isótopos más estables
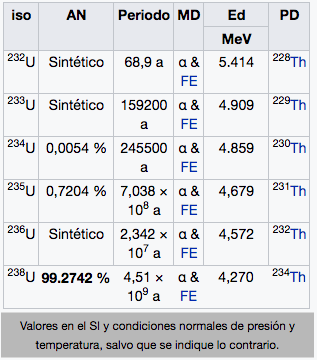
Neptunio
El neptunio es un elemento transuránico de la tabla periódica cuyo símbolo es Np y su número atómico es 93. Cuarto de la familia de los actínidos o segundo período de transición interna del sistema periódico de los elementos. Su nombre proviene del planeta Neptuno.
Historia y obtención
Fue obtenido por primera vez en 1940 por Edwin Mattison McMillan y Philip Hauge Abelson bombardeando uranio con deuterones de gran velocidad. El isótopo 237 ha sido encontrado, en cantidades muy pequeñas, en minas de uranio. Se obtiene más abundantemente como subproducto en la fabricación de plutonio 239. El neptunio metálico se obtiene del trifluoruro de neptunio por reducción con vapor de bario a 1.20 °C.
Propiedades físicas y químicas
Se obtiene artificialmente. Es un metal blanco plateado, similar químicamente al uranio. Existen diversas variedades cristalinas. El neptunio es un elemento reactivo que es mezclable a la mayoría de los elementos. Se presenta en diversos grados de oxidación: +3, +4, +5, +6, y +7, siendo +5 el que posee mayor estabilidad.

Referencias
1. «Criticality test» (en inglés). LANL. Consultado el 24 de noviembre de 2015.
Información general
Nombre: Neptunio
Símbolo: Np
Número: 93
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 237 u
Configuración Electrónica: [Rn] 5f4 6d1 7s2
Electrones por nivel: 2, 8, 18, 32, 22, 9, 2
Propiedades Atómicas
Radio medio: 175 pm
Electronegatividad: 1.36 (escala de Pauling)
Estado(s) de oxidación: 6, 5, 4, 3 (anfótero)
1.ª energía de ionización: 604,5 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 20250 kg/m3
Punto de fusión: 910 K (637 °C)
Punto de ebullición: 4273 K (4000 °C)
Entalpía de fusión: 5,19 kJ/mol
Varios
Estructura cristalina: Ortorrómbico, tetragonal, cúbico
Conductividad eléctrica: 0,822 × 106 m-1·Ω-1 S/m
Conductividad térmica: 6,3 W/(K·m)
Isótopos más estables
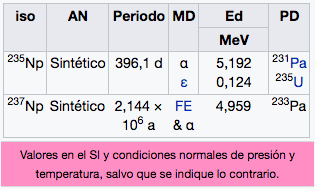
Plutonio
El plutonio es un elemento transuránico radiactivo con el símbolo químico Pu y el número atómico 94. Es un metal actínido con apariencia gris plateada que se oscurece cuando es expuesto al aire, formando una capa opaca cuando se oxida. El elemento normalmente exhibe seis estados alotrópicos y cuatro de oxidación. Reacciona con el carbono, los halógenos, nitrógeno y silicio. Cuando se expone al aire húmedo forma óxidos e hidruros que expanden hasta un 70% su volumen, que a su vez, se desprende en forma de polvo que puede inflamarse de forma espontánea. También es un elemento radiactivo y se puede acumular en los huesos. Estas propiedades hacen que manipular plutonio sea peligroso.
El plutonio es el elemento primordial más pesado en virtud a su isótopo más estable, el plutonio-244, con una semivida aproximada de 80 millones de años es tiempo suficiente para que el elemento se encuentre en pequeñas cantidades en la naturaleza. El plutonio es principalmente un subproducto de la fisión nuclear en los reactores, donde algunos de los neutrones liberados por el proceso de fisión convierten núcleos de uranio-238 en plutonio.
Uno de los isótopos del plutonio utilizados es el plutonio-239, que tiene una semivida de 24.100 años. El plutonio-239, junto con el plutonio-241 son elementos fisibles, esto quiere decir que el núcleo de sus átomos se puede dividir cuando es bombardeado con neutrones térmicos, liberando energía, radiación gamma y más neutrones. Esos neutrones pueden mantener una reacción nuclear en cadena, dando lugar a aplicaciones en armas y reactores nucleares.
El plutonio-238 tiene una semivida de 88 años y emite partículas alfa. Es una fuente de calor en los generadores termoeléctricos de radioisótopos, que son utilizados para proporcionar energía a algunas sondas espaciales. El plutonio-240 tiene una tasa elevada de fisión espontánea, aumentando el flujo de neutrones de cualquier muestra en la que se encuentre. La presencia de plutonio-240 limita el uso de muestras para armas o combustible nuclear y determina su grado. Los isótopos del plutonio son caros y difíciles de separar, por esto suelen fabricarse en reactores especializados.
El plutonio fue sintetizado por primera vez en 1940 por un equipo dirigido por Glenn T. Seaborg y Edwin McMillan en el laboratorio de la Universidad de California, Berkeley bombardeando uranio-238 con deuterio. Posteriormente se encontraron trazas de plutonio en la naturaleza. La producción de plutonio en cantidades útiles por primera vez fue una parte importante del Proyecto Manhattan durante la Segunda Guerra Mundial, que desarrolló las primeras bombas atómicas. La primera prueba nuclear ("Trinity", en julio de 1945), y la segunda bomba atómica usada para destruir una ciudad ("Fat Man" en Nagasaki, Japón en agosto de 1945) tenían núcleos de plutonio-239. Durante y después de la guerra, se realizaron experimentos con humanos sin consentimiento informado que estudiaban la radiación del plutonio y tuvieron lugar varios accidentes críticos, algunos de ellos letales. La eliminación de los residuos de plutonio de las centrales nucleares y el desmantelamiento de las armas nucleares construidas durante la Guerra Fría son preocupaciones sobre la proliferación nuclear y el medio ambiente. Otras fuentes de plutonio en el medio ambiente son consecuencia de las numerosas pruebas nucleares en la superficie (ahora prohibidas).
Historia
Enrico Fermi y un equipo de científicos de la Universidad de Roma informaron que habían descubierto el elemento 94 en 1934. Fermi llamo al nuevo elemento hesperio y lo mencionó en su discurso del Nobel en 1938. La muestra era en realidad una mezcla de bario, kriptón y otros elementos, pero esto no se conocía en ese momento porque la fisión nuclear todavía no se había descubierto.
El plutonio (específicamente, plutonio-238) fue producido y aislado por primera vez el 14 de diciembre de 1940 y fue identificado químicamente el 23 de febrero de 1941 por el Dr. Glenn T. Seaborg, Edwin M. McMillan, J. W. Kennedy y A. C. Wahl bombardeando uranio con deuterio en el ciclotrón de 150 cm de diámetro de la Universidad de California, Berkeley. En el experimento de 1940, se produjo neptunio-238 en el bombardeo pero se desintegró por emisión beta con una semivida corta de unos dos días, que indicaba la formación del elemento 94.
Un documento científico del descubrimiento fue preparado por el equipo y enviado a la revista Physical Review en marzo de 1941. El documento fue retirado antes de la publicación debido a que descubrieron que un isótopo de este nuevo elemento (plutonio-239) podría experimentar la fisión nuclear de forma que podría ser útil para la bomba atómica. La publicación fue retrasada hasta un año después del fin de la Segunda Guerra Mundial debido a las preocupaciones sobre la seguridad.
Edwin McMillan había nombrado recientemente el primer elemento transuránico debido al planeta Neptuno y sugirió que el elemento 94, siendo el siguiente elemento de la serie, fuera nombrado como el que en ese momento era el siguiente planeta, Plutón. Seaborg originalmente consideró el nombre "plutio", pero después pensó que no sonaba tan bien como "plutonio". Él eligió las letras "Pu" como una broma, que fue aprobada sin previo aviso en la tabla periódica. Otros nombres alternativos considerados por Seaborg y otros fueron "ultimio" o "extremio" debido a la creencia errónea de que habían encontrado el último elemento posible en la tabla periódica.
Características
El plutonio, como la mayoría de los metales, tiene una apariencia plateada brillante al principio, muy parecida a la del níquel, pero se oxida rápidamente a un gris opaco, aunque también se reportan amarillo y verde oliva. A temperatura ambiente, el plutonio esta en su forma α (alfa). Esta, la forma estructural más común del elemento (alótropo), es casi tan dura y quebradiza como el hierro fundido gris a menos que se alee con otros metales para hacerlo blando y dúctil. A diferencia de la mayoría de los metales, no es un buen conductor de calor o electricidad. Tiene un punto de fusión bajo. (640 °C) y un inusualmente alto punto de ebullición (3,228 °C).
La desintegración alfa, la liberación de un núcleo de helio de alta energía, es la forma más común de desintegración radioactiva para el plutonio. Una masa de 5 kg de 239Pu contiene alrededor de 12.5 × 1024 átomos. Con una vida media de 24.100 años, aproximadamente 11.5 × 1012 de sus átomos se descomponen cada segundo emitiendo una partícula alfa de 5.157 MeV. Esto equivale a 9,68 vatios de potencia. El calor producido por la deceleración de estas partículas alfa las hace calientes al tacto.
La resistividad es una medida de la fuerza con la que un material se opone al flujo de corriente eléctrica. La resistividad del plutonio a temperatura ambiente es muy alta para un metal, y se hace aún más alta con temperaturas más bajas, lo que es inusual para los metales. Esta tendencia continúa hasta 100 K, por debajo de la cual la resistividad disminuye rápidamente para las muestras frescas. La resistividad comienza a aumentar con el tiempo alrededor de los 20 K debido al daño por radiación, con la tasa dictada por la composición isotópica de la muestra.
Debido a la autoirradiación, una muestra de plutonio se fatiga en toda su estructura cristalina, lo que significa que la disposición ordenada de sus átomos se ve interrumpida por la radiación con el tiempo.. La autoirradiación también puede conducir a recocido que contrarresta algunos de los efectos de la fatiga a medida que la temperatura aumenta por encima de los 100 K.
A diferencia de la mayoría de los materiales, el plutonio aumenta en densidad cuando se funde, en un 2,5%, pero el metal líquido exhibe una disminución lineal en densidad con la temperatura. Cerca del punto de fusión, el plutonio líquido tiene una viscosidad y tensión superficial muy alta en comparación con otros metales.
Aplicaciones
Explosivos
El isótopo plutonio-239 es un componente clave en las armas nucleares debido a su fácil fisión y su disponibilidad. Encapsulando el pozo de plutonio de la bomba en un pisón (una capa opcional de material denso) disminuye la cantidad de plutonio necesaria para alcanzar la masa crítica que refleja los neutrones que escapan de nuevo en el núcleo de plutonio. Esto reduce la cantidad de plutonio necesaria para alcanzar la criticidad de 16 kg a 10 kg, que es una esfera con un diámetro de unos 10 cm (4 in). Esta masa crítica es aproximadamente un tercio de la del uranio-235.
La bombas de plutonio tipo "Fat Man" producidas durante el Proyecto Manhattan usaban explosivos para comprimir el plutonio y obtener densidades significativamente más altas de lo normal, combinado con una fuente central de neutrones para iniciar la reacción y aumentar su eficiencia. De esta forma solo se necesitaban 6,2 kg de plutonio para un rendimiento equivalente a una explosión de 20 kilotones de TNT (Véase también diseño de armas nucleares) Hipotéticamente, tan solo son necesarios 4 kg de plutonio, tal vez menos, para hacer una bomba atómica usando diseños de ensamblado muy sofisticados.
Precauciones
Toxicidad
Los isótopos y compuestos del plutonio son radiactivos y se acumulan en la médula ósea. La contaminación por óxido de plutonio se ha producido tras incidentes radiactivos y desastres nucleares, incluyendo accidentes nucleares militares donde armas nucleares han ardido. Estudios de los efectos de estas pequeñas fugas, así como el extensivo envenenamiento por radiación y posteriores muertes después de los bombardeos atómicos sobre Hiroshima y Nagasaki, han aportado información considerable con respecto a los peligros, síntomas y pronósticos del envenenamiento por radiación, que en el caso de los japoneses sobrevivientes (Hibakusha), se demostró que no estaban relacionados en gran medida con la exposición directa al plutonio.
Durante el decaimiento del plutonio, son liberados tres tipos de radiación, alfa, beta y gamma. La radiación alfa solo puede recorrer cortas distancias y no puede viajar a través de la capa exterior muerta de la piel humana. La radiación beta puede penetrar la piel humana pero no puede atravesar el cuerpo. La radiación gamma puede ir a través de todo el cuerpo. Los tres tipos de radiación son ionizantes. Una exposición aguda o de larga duración conlleva serios problemas de salud, incluyendo síndrome de irradiación aguda, daño genético, cáncer y hasta la muerte. El daño aumenta con la cantidad de exposición.
Potencial crítico
Es necesario evitar que el plutonio se acumule en cantidades cercanas a su masa crítica, debido a que la masa crítica del plutonio es de un tercio de la del uranio-235. La masa crítica del plutonio emite cantidades letales de neutrones y rayos gamma. El plutonio en estado líquido presenta una mayor probabilidad de formar una masa crítica que en estado sólido debido a la moderación que produce el hidrógeno en el agua.
Inflamabilidad
El plutonio metálico se inflama fácilmente, especialmente si el material está dividido en partes finas. En un ambiente húmedo, el plutonio forma hidruros piroforicos en su superficie que pueden incendiarse a temperatura ambiente. El plutonio expande hasta un 70% su volumen cuando se oxida y puede romper el contenedor. La radiactividad del material en combustión es un peligro adicional. La arena de óxido de magnesio es probablemente el material más efectivo para extinguir un fuego de plutonio. Esta enfría el material combustible, actuando como un disipador, y también bloquea el oxígeno. Para manipular o almacenar el plutonio en cualquier forma es necesario tomar precauciones especiales; generalmente se requiere una atmósfera seca de gas inerte.
Referencias
1. Bhadeshia, H. «Plutonium crystallography».
2. Sutcliffe, W.G.; et al. (1995). «A Perspective on the Dangers of Plutonium». Lawrence Livermore National Laboratory. Archivado desde el original el 29 de septiembre de 2006.
Información general
Nombre: Plutonio
Símbolo: Pu
Número: 94
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 244 u
Configuración Electrónica: [Rn] 5f6 7s2
Electrones por nivel: 2, 8, 18, 32, 24, 8, 2
Propiedades Atómicas
Radio medio: 135 pm
Electronegatividad: 1.28 (escala de Pauling)
Radio atómico (calc): 159 pm (radio de Bohr)
Radio covalente: 187±1 pm
Estado(s) de oxidación: 6, 5, 4, 3 (óxido anfotérico)
1.ª energía de ionización: 584,7 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 19816 kg/m3
Punto de fusión: 912,5 K (639 °C)
Punto de ebullición: 3505 K (3232 °C)
Entalpía de vaporización: 333,5 kJ/mol
Entalpía de fusión: 2,82 kJ/mol
Presión de vapor: 10,00 Pa a 2.926 K
Varios
Estructura cristalina: Monoclínica
N.º CAS: 7440-07-5
Calor específico: 35,5 J/(K·kg)
Conductividad térmica: 6,74 W/(K·m)
Módulo elástico: 96 GPa
Módulo de cizalladura: 43 GPa
Coeficiente de Poisson: 0,21
Velocidad del sonido: 2,260 m/s a 293,15 K (20 °C)
Isótopos más estables
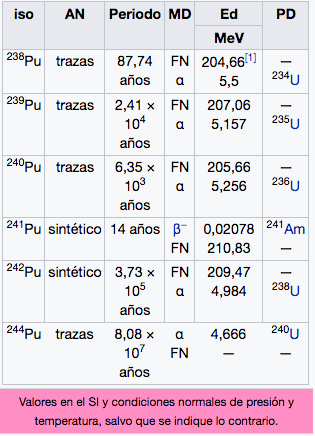
Americio
El americio es un elemento químico artificial de número atómico 95 situado dentro del grupo de los actínidos en la tabla periódica de los elementos. Su símbolo es Am. Todos sus isótopos son radiactivos y no existen en la naturaleza. Su nombre proviene de América, de forma análoga al europio.
Historia
El americio fue aislado por primera vez por Glenn T. Seaborg, Leon O. Morgan, Ralph A. James, y Albert Ghiorso en 1944 en el Laboratorio de Metalurgia de la Universidad de Chicago. El equipo creó el isótopo 241Am a partir de 239Pu, bombardeándolo con neutrones en un reactor nuclear. Esto se transformó en 240Pu y después en 241Pu, cambiando así a 241Am por desintegración beta. Seaborg obtuvo la patente US 3156523 para "Element 95 and Method of Producing Said Element" (Elemento 95 y el método para producir dicho elemento).

Características notables
El americio puro tiene un lustre plateado y blanco. Es más plateado que el plutonio y el neptunio, y aparentemente más maleable que éste o el uranio. La desintegración alfa de 241Am es aproximadamente tres veces la del radio. Unos cuantos gramos de 241Am emiten una alta cantidad de rayos gamma, lo cual crearía serios problemas de salud a cualquiera que se expusiese al elemento. También presenta la característica de que es fisible.
Isótopos
Han sido descritos 19 radioisótopos del americio, siendo los más estables el 243Am con una vida media de 7370 años y el 241Am con vida media de 472,7 años. El resto de los isótopos radiactivos tienen vidas medias menores que 51 horas, casi en su mayoría mayores a 100 minutos. El elemento también tiene ocho isómeros nucleares, siendo el de mayor estabilidad 242mAm (vida media de 141 años). Los pesos atómicos de los isótopos de americio oscilan entre 231,046 u.m.a (del 231Am) hasta 249,078 u.m.a. (correspondientes al 249Am).
Aplicaciones
Este elemento puede ser producido en cantidades de varios kilogramos y tiene algunos usos (en especial el 241Am, en virtud de que es relativamente más sencillo producir muestras de este radioisótopo). Este mismo radioisótopo fue utilizado como una fuente portátil de rayos gamma para su uso en radiografías. El isótopo 242Am es un emisor de neutrones y además es citado para uso en un avanzado cohete de propulsión nuclear; sin embargo, es demasiado caro como para producirse en cantidades suficientemente grandes.
Usos en el hogar
El americio tiene cierta utilidad en el hogar y en la industria: algunos detectores de humo contienen una pequeña muestra, normalmente unos 0,9 microcurios (cerca de 0,2 miligramos) de 241Am, como fuente de radiación ionizante. El funcionamiento de estos detectores se basa en la disminución de la conductividad del aire. Una cámara del detector permite el contacto entre el americio y el ambiente. Dicho aire es ionizado por la presencia de partículas alfa provenientes de la desintegración de los núcleos de 241Am y se vuelve, por tanto, conductor, cerrando así un circuito. La presencia de otras partículas no ionizadas reduce la conductividad dentro de la cámara, interrumpe el circuito, y permite que suene la alarma. Cabe destacar que la cantidad de americio presente en estos detectores no pone en peligro la salud de los inquilinos. A pesar de que se prohíba su comercialización el hecho de tener uno instalado no significa incurrir en un delito. Estas alarmas fueron retiradas del mercado debido a que su gestión como residuos era especial y más cara de lo normal.

Química
El número de oxidación más común del americio es +3. Es mucho más complicado oxidar Am(III) a Am(IV) que hacerlo de Pu(III) a Pu(IV) en solución acuosa.
Los científicos trabajan para reducir la radiotoxicidad o bien encontrar el modo de hacerla útil para ser usada como combustible nuclear.
El americio, a diferencia del uranio, no forma fácilmente dióxido de americio (AmO2). Esto se debe a su dificultad para oxidarse por arriba de +3 cuando se encuentra en solución acuosa. En el medio ambiente puede hacerse un compuesto complejo agregándose el carbono y oxígeno.
AmO2(OH)+1
AmO2(OH)2+2
AmO2CO3+1
AmO2(CO3)2-1
AmO2(CO3)3-3
Referencias
1. Patent Nr. 3156523; Google Patents..
2. G. T. Seaborg, R. A. James, L. O. Morgan: "The New Element Americium (Atomic Number 95)", NNES PPR (National Nuclear Energy Series, Plutonium Project Record), Vol. 14 B The Transuranium Elements: Research Papers, Paper No. 22.1, McGraw-Hill Book Co., Inc., New York, 1949; Abstract; Maschinoskript (Januar 1948).
Información general
Nombre: Americio
Símbolo: Am
Número: 95
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 243 u
Configuración Electrónica: [Rn] 5f7 7s2
Electrones por nivel: 2, 8, 18, 32, 25, 8, 2
Propiedades Atómicas
Radio medio: 175 pm
Electronegatividad: 1,3 (escala de Pauling)
Radio atómico (calc): 173 pm (radio de Bohr)
Radio covalente: 180±6 pm
Estado(s) de oxidación: 7, 6,5,4,3, 2 (óxido anfotérico)
1.ª energía de ionización: 578 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 13,670 kg/m3
Punto de fusión: 1449 K (1176 °C)
Punto de ebullición: 2880 K (2607 °C)
Entalpía de fusión: 14,39 kJ/mol
Varios
Estructura cristalina: Hexagonal
Conductividad eléctrica: 2,2 × 106 m-1 S/m
Conductividad térmica: 10 W/(K·m)
Isótopos más estables
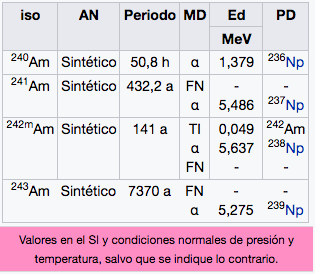
Curio
El curio es un elemento sintético de la tabla periódica cuyo símbolo es Cm y su número atómico es 96. Se produce bombardeando plutonio con partículas alfa (iones de helio). Es un actínido. El curio no existe en el ambiente terrestre, pero puede producirse en forma artificial. Sus propiedades químicas se parecen tanto a las de las tierras raras típicas que, si no fuera por su radiactividad, podría confundirse fácilmente con uno de estos elementos. Entre los isótopos conocidos del curio figuran los de número de masa 238 a 250. El isótopo 244Cm es de particular interés a causa de su uso potencial como una fuente compacta de fuerza termoeléctrica, al utilizarse el calor generado por decaimiento nuclear para generar fuerza eléctrica.
El curio metálico puede producirse por reducción del trifluoruro de curio, con vapor de bario. El metal tiene un lustre plateado, el cual se pierde al contacto con el aire, y una densidad relativa de 13.5. El punto de fusión es de 1340 (+/-) 40 °C (2444 +/- 72 °F). El metal se disuelve con facilidad en ácidos minerales comunes, con formación de ion tripositivo.
Se han preparado varios compuestos sólidos del curio y sus estructuras se han determinado por difracción de rayos X. Estos incluyen CmF4, CmF3, CmCl3, CmBr3, CmI3, Cm2O3, CmO2. En los lantánidos hay análogos isoestructurales de los compuestos de curio.
Historia
El curio fue sintetizado por primera vez en la Universidad de California, Berkeley, también por Glenn T. Seaborg, Ralph A. James y Albert Ghiorso en 1944. Se eligió el nombre curio en honor a Marie Curie y su marido Pierre, famosos por descubrir el radio y por otros importantes trabajos sobre radiactividad.

Referencias
1. Hall, Nina (2000). The New Chemistry: A Showcase for Modern Chemistry and Its Applications. Cambridge University Press. pp. 8–9. ISBN 978-0-521-45224-3.
2. Noe, M.; Fuger, J. (1971). "Self-radiation effects on the lattice parameter of 244CmO2". Inorganic and Nuclear Chemistry Letters. 7 (5): 421. doi:10.1016/0020-1650(71)80177-0.
Información general
Nombre: Curio
Símbolo: Cm
Número: 96
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 247 u
Configuración Electrónica: [Rn] 5f7 6d1 7s2
Electrones por nivel: 2, 8, 18, 32, 25, 9, 2
Propiedades Atómicas
Electronegatividad: 1,3 (escala de Pauling)
Estado(s) de oxidación: 3
1.ª energía de ionización: 581 kJ/mol
Propiedades Físicas
Estado ordinario: Sólido
Densidad: 13,510 kg/m3
Punto de fusión: 1613 K (1340 °C)
Punto de ebullición: 3383 K (3110 °C)
Entalpía de fusión: 15 kJ/mol
Varios
Estructura cristalina: Hexagonal compacta
Isótopos más estables
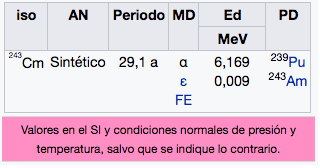
Lawrencio
El lawrencio o laurencio también es un elemento sintético radiactivo de la tabla periódica de los elementos cuyo símbolo es Lr (anteriormente Lw) y su número atómico es 103. En la tabla periódica de los elementos, se trata de un elemento del bloque d en el período 7 y es el último elemento de la serie de los actínidos. Experimentos químicos confirmaron que el lawrencio se comporta homólogamente al lutecio y es químicamente similar a otros actínidos.
El lawrencio fue sintetizado por primera vez por el equipo de física nuclear del Lawrence Berkeley National Laboratory de la Universidad de California, dirigido por Albert Ghiorso. Los primeros átomos de lawrencio fueron producidos al bombardear un blanco de tres miligramos, compuesto de tres isótopos de californio con núcleos de boro-10 y boro-11 del Acelerador lineal de iones pesados. El equipo sugirió para el elemento el nombre lawrencio, en honor al físico estadounidense Ernest O. Lawrence, y el símbolo «Lw», pero la IUPAC cambió el símbolo a «Lr» en 1963. Este fue el elemento más pesado que se sintetizó en la serie de los actínidos.
Todos los isótopos del lawrencio son radiactivos; su isótopo más estable conocido es 266Lr, con un período de semidesintegración de aproximadamente 11 horas. Todos los demás isótopos, excepto 260Lr, 261Lr, 262Lr y 266Lr, se desintegran con una vida menor a un minuto.
Historia
Descubrimiento
El lawrencio fue sintetizado por primera vez por el equipo de física nuclear integrado por Albert Ghiorso, Torbjørn Sikkeland, Almon Larsh, Robert M. Latimer, y sus colaboradores el 14 de febrero de 1961, en el Lawrence Radiation Laboratory —ahora llamado Lawrence Berkeley National Laboratory— de la Universidad de California. Los primeros átomos de lawrencio se produjeron mediante el bombardeo de un blanco de tres miligramos, compuesto por tres isótopos de californio, 10B y 11B desde el Acelerador lineal de iones pesados —HILAC por sus siglas en inglés—. El equipo de Berkeley informó que el isótopo 257Lr fue detectado de esta manera, y que se desintegró emitiendo una partícula alfa 8,6 MeV con un período de semidesintegración de unos ocho segundos. Esta identificación posteriormente se corrigió a 258Lr.
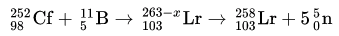
En 1967, investigadores en física nuclear en Dubna, Rusia, informaron que no pudieron confirmar la asignación de un emisor alfa con un período de semidesintegración de ocho segundos al isótopo 257Lr. Este isótopo posteriormente se dedujo que se trataba de 258Lr. En su lugar, el equipo de Dubna reportó un isótopo con un período de semidesintegración de 45 segundos como 256Lr.
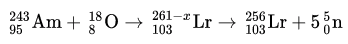
Otros experimentos demostraron la química actínida del nuevo elemento, por lo que en 1970 fue conocido como el último actínido. En 1971, el equipo de física nuclear de la Universidad de California en Berkeley realizaron con éxito toda una serie de experimentos dirigidos a la medición de las propiedades de desintegración nuclear de los isótopos de lawrencio con masa de 255 a 260.
En 1992, el grupo trans-fermio de la IUPAC —TWG por sus siglas en inglés— reconoció oficialmente a los equipos de física nuclear en Dubna y Berkeley como los co-descubridores del lawrencio.
Denominación
El origen del nombre, ratificado por la American Chemical Society, es una referencia al físico nuclear Ernest O. Lawrence de la Universidad de California, que inventó el acelerador de partículas de ciclotrón. Óriginalmente fue utilizado como símbolo Lw, pero finalmente le fue asignado el símbolo Lr. En agosto de 1997, la Unión Internacional de Química Pura y Aplicada ratificó el nombre lawrencio y el símbolo Lr durante una reunión en Ginebra.
Características principales
Es el primer miembro del bloque 6d; de acuerdo con la regla de Madelung. Una correlación estricta entre los bloques de la tabla periódica y las configuraciones de las capas orbitales para átomos neutros clasificaría al lawrencio como un metal de transición, ya que podría ser clasificado como un elemento del bloque d. Sin embargo, el lawrencio se clasifica como un elemento actínido, de acuerdo con las recomendaciones de la IUPAC
Aplicaciones
Se puede usar para reactores nucleares debido a su isómero y sus propiedades.
Referencias
1. Lawrencio
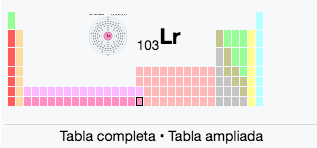
Información general
Nombre: Lawrencio
Símbolo: Lr
Número: 103
Serie Química: Actínidos
Grupo: 3
Período: 7
Bloque: d
Masa Atómica: 262 u
Configuración Electrónica: [Rn]5f147s27p1
Electrones por Nivel: 2, 8, 18, 32, 32, 8, 3
Propiedades Atómicas
Electronegatividad: 1.3 (escala de Pauling)
Estado(s) de oxidación: 3
1.ª Energía de ionización: 443.8 kJ/mol
2.ª Energía de ionización: 1428 kJ/mol
Propiedades Físicas
Estado Ordinario: Presuntamente Sólido
Nobelio
El nobelio (anteriormente llamado unnilbio (Unb)) es un elemento sintético de la tabla periódica cuyo símbolo es No y su número atómico es 102, llamado así en honor del inventor Alfred Nobel. Es el 11º elemento sintético de la tabla periódica. Su decaimiento se realiza por emisión de partículas alfa, es decir, un ion de helio doblemente cargado. Hasta la fecha solo se han producido cantidades atómicas del elemento. El nobelio es el décimo elemento más pesado que el uranio producido sintéticamente y el 14.º miembro de los actínidos.
Fue identificado por primera vez en forma correcta en 1966 por científicos del Laboratorio Fliórov de Reacciones Nucleares en Dubná, Rusia. Se sabe muy poco sobre este elemento, pero los escasos experimentos químicos que se han llevado a cabo han permitido establecer que el mismo forma un ion bivalente estable en solución como también el ion trivalente predicho asociado con su pertenencia al grupo de los actínidos.
Aplicaciones
Solo se usa, al igual que otros Lantánidos, en estudios científicos atómicos, pero éste se podría implantar en la dinamita, si se llegase a hacer compatible con el Nitrógeno (Nitroglicerina).
Características principales
Fue identificado por primera vez en forma correcta en 1966 por científicos del Laboratorio Fliórov de Reacciones Nucleares en Dubná, Rusia. Se sabe muy poco sobre este elemento, pero los escasos experimentos químicos que se han llevado a cabo han permitido establecer que el mismo forma un ion bivalente estable en solución como también el ion trivalente predicho asociado con su pertenencia al grupo de los actínidos.
Referencias
1. Nobelio
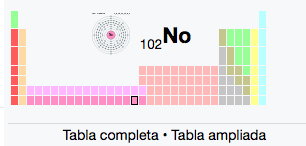
Información general
Nombre: Nobelio
Símbolo: No
Número: 102
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 259 u
Configuración Electrónica: [Rn]5f147s2
Electrones por Nivel: 2, 8, 18, 32, 32, 8, 2
Propiedades Atómicas
Estado(s) de oxidación: 2, 3
1.ª Energía de ionización: 641.6 kJ/mol
2.ª Energía de ionización: 1254.3 kJ/mol
Isótopos más estables
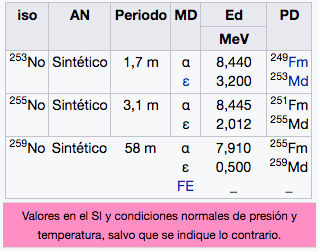
Mendelevio
El mendelevio (anteriormente llamado unnilunio) es un elemento de la tabla periódica cuyo símbolo es Md (anteriormente Mv) y su número atómico es 101. El nombre de este elemento proviene del creador de la Tabla periódica de los Elementos: Dmitri Mendeleyev (1834-1907), padre de la tabla periódica.
Descubrimiento
El mendelevio es el noveno elemento transuránido descubierto de la serie de los actínidos. Lo identificaron Albert Ghiorso, Bernard G. Harvey, Gregory R. Choppin, Stanley G. Thompson y Glenn T. Seaborg el 19 de febrero de 1955 mediante el bombardeo del isótopo einstenio-253 con iones helio en el ciclotrón de 60 pulgadas de la Universidad de California en Berkeley. El isótopo producido fue el 256-Md (vida media de 76 minutos).
El isótopo 258-Md (55 días) se ha obtenido por bombardeo de un isótopo del einstenio con iones helio. Este isótopo es el que se utiliza para estudiar las propiedades químicas y físicas. En solución acuosa parece adoptar los números de oxidación (III) (característico de los actínidos).
Aplicaciones
Sólo se usa para estudio científico y para nuevos isótopos y relaciones atómicas, además, dada la rareza del elemento, tiene usos meramente reservados.
Referencias
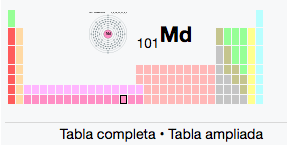
Información general
Nombre: Mendelevio
Símbolo: Md
Número: 101
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 258.1 u
Configuración Electrónica: [Rn]5f137s2
Electrones por Nivel: 2, 8, 18, 32, 31, 8, 2
Propiedades Atómicas
Electronegatividad: 1.3 (escala de Pauling)
Estado(s) de oxidación: 2, 3
1.ª Energía de ionización: 635 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Isótopos más estables
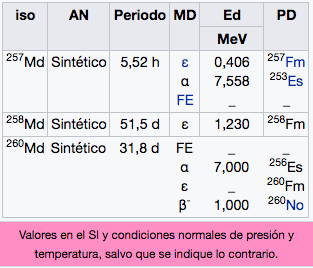
Fermio
El fermio es un elemento químico radiactivo creado artificialmente cuyo número atómico es 100 y de peso atómico 254, de símbolo Fm. Existen 16 isótopos conocidos siendo el 257Fm el más estable con un periodo de semidesintegración de 100,5 días. El fermio es uno de los elementos transuránicos del grupo de los actínidos del sistema periódico. El elemento fue aislado en 1952, a partir de los restos de una explosión de bomba de hidrógeno, por el químico estadounidense Albert Ghiorso y sus colegas. Más tarde el fermio fue preparado sintéticamente en un reactor nuclear bombardeando plutonio con neutrones, y en un ciclotrón bombardeando uranio 238 con iones de nitrógeno. Se han obtenido isótopos con números másicos desde 242 a 259; el fermio 257, que es el que tiene una vida más larga, tiene una vida media de 80 días. Al elemento se le dio el nombre de fermio en 1955, en honor al físico nuclear estadounidense de origen italiano Enrico Fermi. El fermio no tiene aplicaciones industriales.
Características principales
El fermio no se encuentra en la naturaleza; su descubrimiento y producción se alcanza por transmutación artificial de elementos más ligeros. Se han descubierto los isótopos radiactivos de número de masa 244-259. La masa total del fermio que ha sido sintetizado es mucho menor de una millonésima de gramo.
La fisión espontánea es el modo principal de decaimiento para 244Fm, 256Fm y 258Fm. El isótopo con vida más larga es 257Fm, el cual tiene una vida media de unos 100 días. El fermio -258 decae por fisión espontánea y tiene una vida media de 0.38 milisegundos. Esto sugiere la existencia de una anormalidad en este punto en la tabla periódica.
Aplicaciones
Sólo se usa en estudios atómicos, por lo cual se produce solamente en millonésimas de gramo.
Información general
Nombre: Fermio
Símbolo: Fm
Número: 100
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 257 u
Configuración Electrónica: [Rn]5f127s2
Electrones por Nivel: 2, 8, 18, 32, 30, 8, 2
Propiedades Físicas
Estado Ordinario: Sólido
Isótopos más estables

Einstenio
El einstenio (antiguamente también llamado atenio) es un elemento sintético de la tabla periódica cuyo símbolo es Es y su número atómico es 99. Fue llamado así en honor de Albert Einstein, aunque se descubrió en diciembre de 1952 en los restos de la primera explosión termonuclear en el Pacífico, realizada un mes antes, por el equipo de investigadores formado por G. R. Choppin, A. Ghiorso, B. G. Harvey y S. G. Thompson
Como muchos elementos de este mismo grupo, no se encuentra en la naturaleza, sino que se obtiene artificialmente, además de que su tiempo de vida es menor.
El proceso de obtención es a través de una transmutación nuclear de elementos más ligeros. La transmutación consiste en convertir núcleos estables en otros núcleos al ser bombardeados por partículas a alta velocidad. El primer experimento de ese tipo fue realizado por Ernest Rutherford (físico y químico neozelandés). Consistió en mandar partículas alfa sobre una fina lámina de oro y observar cómo esta afectaba a la trayectoria de los rayos.
El 254Es puede sintetizarse por bombardeo de Am, Pu o Cm con neutrones.
Aplicaciones
El isótopo 253Es se emplea para producir el elemento mendelevio. Actualmente, no hay aplicaciones prácticas que no sean las de la investigación científica básica, debido a las pequeñas cantidades de einstenio que se producen y la corta vida media de su isótopo. En particular, el einstenio fue utilizado para sintetizar, por primera vez, 17 átomos del nuevo elemento mendelevio en 1955.
Método de obtención
Su método de obtención consiste en irradiar aproximadamente 1 kg de Pu-239 en un reactor para generar Pu-242. Este Pu-242 se introduce en bolas de óxido de plutonio y aluminio en polvo. Posteriormente estas bolas se introducen en varillas y se irradian. Finalmente, se introducen las varillas en un reactor isotópico de alto flujo. Tras todo esto se separa el einstenio del californio.
Referencias
1. Einstenio
Información general
Nombre: Einstenio
Símbolo: Es
Número: 99
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 252 u
Configuración Electrónica: [Rn]5f117s2
Electrones por Nivel: 2, 8, 18, 32, 29, 8, 2
Propiedades Atómicas
Electronegatividad: 1.3 (escala de Pauling)
Estado(s) de oxidación: 2, 3, 4
1.ª Energía de ionización: 619 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 8.84 kg/m3
Punto de fusión: 1133 K (700 °C)
Isótopos más estables
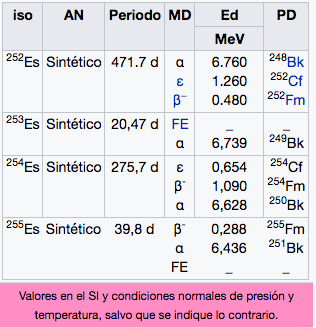
Californio
El californio es un elemento químico radiactivo con símbolo Cf y número atómico 98. Este elemento fue obtenido por primera vez en la Universidad de California en Berkeley en 1950 bombardeando curio con partículas alfa —iones de helio-4—. Es un elemento actínido, el sexto de los elementos transuránicos en ser sintetizado, y tiene la segunda mayor masa atómica de todos los elementos que han sido producidos en cantidades suficientemente grandes para ser visto a simple vista, después del einstenio. El nombre del elemento se debe a California y la Universidad de California. Es el elemento más pesado que se produce en la Tierra de forma natural; los elementos de mayor masa atómica solo pueden ser producidos mediante síntesis.
Existen dos estructuras cristalinas para el californio a presión normal: una por encima y otra por debajo de los 900 °C. A altas presiones aparece una tercera forma. El californio pierde su brillo lentamente en contacto con el aire a temperatura ambiente. Los compuestos del californio tienen en su mayoría una forma química del elemento, denominada californio (III), la cual puede participar en tres enlaces químicos. De los veinte isótopos conocidos del californio, el más estable es el californio-251, que tiene una vida media de 898 años. Esta vida media tan corta implica que no se encuentren cantidades significativas de este elemento en la corteza terrestre. El californio-252, con una vida media de 2,64 años, es el isótopo usado más común y es producido en el Laboratorio Nacional Oak Ridge en los Estados Unidos y en el Instituto de Investigación de Reactores Atómicos en Rusia.
El californio es uno de los pocos elementos transuránicos que tiene aplicaciones prácticas. La mayor parte de estas usan las propiedades de ciertos isótopos del californio para emitir neutrones. Por ejemplo, se puede usar para ayudar a encender reactores nucleares y como fuente de neutrones en el estudio de materiales mediante la difracción de neutrones y espectroscopía de neutrones. También se puede usar en la síntesis nuclear de elementos de mayor masa; el ununoctio —elemento 118— fue sintetizado bombardeando átomos de californio-249 con iones de calcio-48. Cuando se trabaja con californio hay que tener en cuenta consideraciones radiológicas así como la capacidad de este elemento para interrumpir la producción de glóbulos rojos por bioacumulación en el tejido óseo.
Características
Propiedades físicas
El californio es un metal actínido de color blanco plateado con un punto de fusión de 900 ± 30 °C y un punto de ebullición estimado de 1745 °C. El metal puro es maleable y puede ser cortado fácilmente con una cuchilla de afeitar. El californio metálico empieza a evaporarse por encima de los 300 °C en el vacío. Por debajo de 51 K (−220 °C) es ferromagnético o ferrimagnético —actúa como un imán—, entre 48 y 66 K es antiferromagnético —un estado intermedio— y por encima de los 160 K (−110 °C) es paramagnético, por lo que puede convertirse en magnético gracias a campos magnéticos externos. Forma aleaciones con metales lantánidos, aunque se tienen pocos conocimientos sobre ello.
El elemento posee dos formas cristalinas a presión atmosférica: una forma doble-hexagonal compacta llamada alfa (α) y una forma cúbica centrada en las caras llamada beta (β). La forma α tiene lugar por debajo de los 900 °C con una densidad de 15,10 g/cm3 y la β se da por encima de los 900 °C con una densidad de 8,74 g/cm3. A 48 GPa de presión, la forma β cambia a un sistema cristalino ortorrómbico debido a la deslocalización de los electrones 5f de los átomos, que rompe los enlaces.
El módulo de compresibilidad del californio es de 50 ± 5 GPa, que es similar al de los metales lantánidos trivalentes pero menor que el de la mayoría de los metales comunes, como el del aluminio (70 GPa).
Propiedades químicas y compuestos
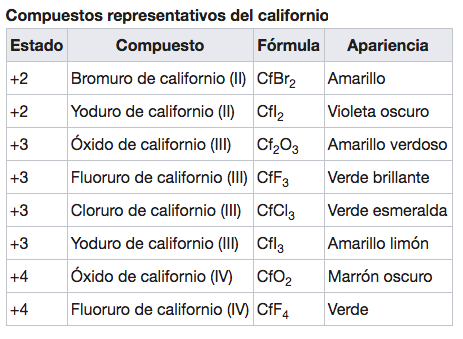
El californio puede tener valencia 2, 3 o 4. Se cree que sus propiedades químicas son similares a las de otros elementos actínidos de valencia 3+ y a las del disprosio, que es el lantánido situado encima del californio en la tabla periódica. El elemento pierde brillo lentamente en contacto con el aire a temperatura ambiente, tanto más rápido cuanto más se incrementa la humedad. El californio reacciona cuando se calienta en una mezcla con hidrógeno, nitrógeno o un calcógeno —elemento de la familia del oxígeno—. Las reacciones con hidrógeno seco y con ácidos minerales acuosos son rápidas.
El californio solo es soluble en agua en su forma de catión californio (III). Los intentos de reducción-oxidación del ion +3 en solución han fracasado. El elemento forma una solución soluble en agua en forma de cloruro, nitrato, perclorato y sulfato y se precipita en forma de fluoruro, oxalato o hidróxido.
Isótopos
Se caracterizaron 20 radioisótopos del californio. Los más estables son: el californio-251, con una vida media de 898 años; el californio-249, con una vida media de 351 años; el californio-250, con una vida media de 13,08 años; y el californio-252, que tiene una vida media de 2,645 años. El resto de los isótopos tienen vidas medias menores a un año, no llegando la mayoría de ellas a 20 minutos. El número másico de los isótopos del californio se encuentra en un rango entre 237 y 256.
El californio-249 se forma a partir de la desintegración beta del berkelio-249 mientras que otros isótopos del californio son formados sometiendo al berkelio a radiaciones de neutrones intensas en un reactor nuclear. A pesar de que el californio-251 es el isótopo con la mayor vida media, su rendimiento de producción es de solo un 10% debido a su tendencia a recoger neutrones —alta captura neutrónica— y su tendencia a interactuar con otras partículas —elevada sección transversal de neutrones—.
El californio-252 es un fuerte emisor de neutrones, lo que lo convierte en extremadamente radiactivo y peligroso. El 96,9% de las veces, el californio-252 se ve sometido a desintegración alfa —que supone la pérdida de dos protones y dos neutrones— para formar curio-248, mientras que el 3,1% restante de las desintegraciones son fisiones espontáneas. Un microgramo (µg) de californio-252 emite 2,3 millones de neutrones por segundo, un promedio de 3,7 neutrones por cada fisión espontánea. La mayor parte de los restantes isótopos se desintegran en curio —con número atómico 96— mediante desintegración alfa.
Aplicaciones
El californio-252 tiene aplicaciones especializadas como un fuerte emisor de neutrones y cada microgramo de californio puro produce 139 millones de neutrones por minuto. Esta propiedad hace que el californio sea útil como fuente inicial de neutrones para algunos reactores nucleares y como fuente de neutrones portátil —no basada en reactor— en el análisis por activación neutrónica para detectar pequeñas cantidades de elementos en muestras. Los neutrones del californio son empleados para tratar ciertos tipos de cáncer cervical y tumores cerebrales cuando otras técnicas de radioterapia no resultan efectivas. Ha sido usado en aplicaciones educacionales desde 1969 cuando el Instituto de Tecnología de Georgia recibió un préstamo de 119 µg de californio-252 de la Savannah River Plant. También se utiliza en analizadores de carbón y analizadores de materiales a granel en la industria del carbón y el cemento.
La penetración de los neutrones en los materiales hace que el californio sea útil en instrumentos de detección como los escáneres de barras de combustible nuclear; radiografía neutrónica de aeronaves y componentes de armas para detectar la corrosión, malas soldaduras, grietas y humedad acumulada; y en detectores de metales portátiles. Los medidores de humedad de neutrones usan californio-252 para encontrar agua y capas de petróleo en los pozos de petróleo, como fuente portátil de neutrones en las prospecciones de oro y plata para el análisis in situ y para detectar el movimiento de agua subterránea. Los principales usos del californio-252 en 1982 eran, en orden de uso: puesta en marcha de reactores (48,3%), escáneres de barras de combustible nuclear (25,3%) y análisis por activación (19,4%). En 1994 la mayoría del californio-252 era usado en radiografía neutrónica (77,4%); los escáneres de barras de combustible nuclear (12,1%) y la puesta en marcha de reactores (6,9%) tenían importancia pero ocupaban usos secundarios.
El californio-251 tiene una masa crítica muy pequeña —unos 5 kg—, es muy letal y en un corto periodo de tiempo vuelve tóxico el medio ambiente. Esto ha dado lugar a algunas afirmaciones exageradas sobre los posibles usos del elemento.
El californio también ha sido usado para producir otros elementos transuránicos; por ejemplo, el lawrencio fue sintetizado por primera vez en 1961 bombardeando californio con núcleos de boro. En octubre de 2006, investigadores del Instituto Central de Investigaciones Nucleares en Dubná, Rusia anunciaron que habían identificado tres átomos de ununoctio —elemento 118 (oganesón)— como resultado de bombardear californio-249 con calcio-48, produciendo el elemento más pesado que se ha conseguido sintetizar. El experimento contenía unos 10 mg de californio-249 depositados en un papel de titanio de 32 cm2 de área.
Precauciones
El californio se bioacumula en el tejido óseo y libera radiación que interrumpe la capacidad del cuerpo para producir glóbulos rojos. El elemento no tiene un rol biológico en ningún organismo debido a su radiactividad intensa y la baja concentración en el medio ambiente.
Puede entrar en el cuerpo por la ingestión de comidas o bebidas contaminadas o por respirar aire con partículas suspendidas de este elemento. Una vez en el cuerpo, solo el 0,05% del californio alcanzará el torrente sanguíneo. Aproximadamente el 65% de este californio será depositado en el esqueleto, el 25% en el hígado y el resto en otros órganos o excretado, principalmente en la orina. La mitad del californio depositado en el esqueleto y en el hígado desaparece en 50 y 20 años respectivamente. El californio en el esqueleto se adhiere a la superficie del hueso antes de migrar lentamente a todo el hueso.
El elemento es más peligroso si se encuentra dentro del cuerpo. Además, el californio-249 y el californio-251 pueden causar daños en los tejidos externos por la emisión de rayos gamma. La radiación ionizante emitida por el californio acumulado en los huesos y el hígado puede provocar cáncer.
Referencias

Información general
Nombre: Californio
Símbolo: Cf
Número: 98
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 251 u
Configuración Electrónica: [Rn]5f107s2
Electrones por Nivel: 2, 8, 18, 32, 28, 8, 2
Propiedades Atómicas
Electronegatividad: 1.3 (escala de Pauling)
Estado(s) de oxidación: 2, 3, 4
1.ª Energía de ionización:608 kJ/mol
Propiedades Físicas
Estado Ordinario: Sólido
Densidad: 15100 kg/m3
Punto de fusión: 1173 K (700 °C)
Punto de ebullición: 1743 (1737 °C)
Varios
Estructura cristalina: Hexagonal
Isótopos más estables
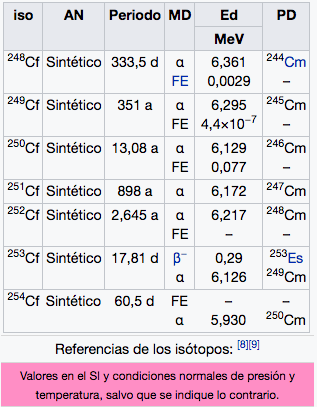
Berkelio
El berkelio es un elemento sintético de la tabla periódica cuyo símbolo es el Bk y su número atómico es 97. Pertenece a la serie de los actínidos y elementos transuránicos. Su nombre es un homenaje a la ciudad de Berkeley, California, donde se encuentra el Laboratorio de Radiación de la Universidad de California, Lo descubrieron en 1949 S. G. Thompson, A. Ghiorso y G. T. Seaborg en la Universidad de California en Berkeley. El berkelio fue el quinto elemento descubierto luego del neptunio, plutonio, curio y americio.
El isótopo principal del berkelio es el berkelio-249, el cual se sintetiza en cantidades ínfimas en un reactor nuclear de alto flujo, especialmente en el Oak Ridge National Laboratory de Tennessee, Estados Unidos, y en el Research Institute of Atomic Reactors de Dimitrovgrad, Rusia. Para producir el isótopo berkelio-247, se irradia el isótopo sintético curio-244, que es muy escaso, con partículas alfa de alta energía.
Desde 1967, la producción total de berkelio en los Estados Unidos apenas supera la cantidad de un gramo. No existe, pues, una aplicación práctica del berkelio, aparte de la investigación científica, que se centra principalmente en la síntesis de elementos transuránicos más pesados y transactínidos. En el año 2009, en Oak Ridge, se preparó una cantidad de 22 miligramos de berkelio-249 mediante la irrradiación durante 250 días, seguida de un proceso de purificación de 90 días. Esta muestra fue utilizada para sintetizar, en 2009 y por primera vez, el elemento ununseptio en el Joint Institute for Nuclear Research, Rusia, tras ser bombardeado con iones de calcio-48 durante 150 días. Este experimento fue la culminación de la colaboración entre Rusia y los Estados Unidos para la síntesis de los elementos 113 al 118.
Características principales
El berkelio es un metal radiactivo, blando y de color plateado blanquecino. El isótopo berkelio-249 emite electrones de baja energía y por lo tanto es relativamente segura su manipulación. Sin embargo, su vida media es de 330 días y, al desintegrarse, da como resultado californio-249, un emisor de partículas alfa muy potente y peligroso. Esta transformación gradual resulta especialmente problemática cuando se estudian las propiedades del berkelio elemental y sus compuestos químicos, dado que la formación del californio no solo produce contaminación química, sino también daño por radiación autoinfligido, además de ser termógeno debido a las partículas alfa que emite.
Referencias
1. Berkelio
Información general
Nombre: Berkelio
Símbolo: Bk
Número: 97
Serie Química: Actínidos
Grupo: -
Período: 7
Bloque: f
Masa Atómica: 247 u
Configuración Electrónica: [Rn]5f97s2
Electrones por Nivel: 2, 8, 18, 32, 27, 8, 2
Propiedades Físicas
Estado Ordinario: Sólido
Varios
Estructura cristalina: Hexagonal Compacta
Isótopos más estables
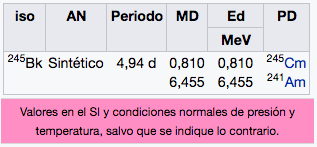
Elementos del Grupo 1
 Los metales alcalinos o simplemente alcalinos (del árabe, alqali) son los seis elementos situados en el grupo I (1) de la tabla periódica1 (excepto el hidrógeno, que es un gas).
Los metales alcalinos o simplemente alcalinos (del árabe, alqali) son los seis elementos situados en el grupo I (1) de la tabla periódica1 (excepto el hidrógeno, que es un gas).
El grupo de los metales alcalinos están formados por los elementos que se sitúan en la primera columna (grupo) de la tabla periódica o sistema periódico, lo componen los elementos químicos litio (Li), sodio (Na), potasio (K), rubidio (Rb), cesio (Cs), francio (Fr). Pertenecen a la serie de elementos s, esto significa que los metales alcalinos tienen su electrón más externo en un orbital s, cada uno tiene solo un electrón en su nivel energético más externo (s), con buena tendencia a perderlo (esto es debido a que tienen poca afinidad electrónica, y baja energía de ionización), con lo que forman un catión monovalente, M+. Esta configuración electrónica compartida da como resultado que tengan propiedades características muy similares. De hecho, los metales alcalinos proporcionan el mejor ejemplo de tendencias de grupo en propiedades en la tabla periódica, con elementos que exhiben un comportamiento homólogo bien caracterizado.
Presentan densidades muy bajas y son buenos conductores de calor y de electricidad; reaccionan de inmediato con el agua, oxígeno y otras sustancias químicas, y nunca se les encuentra como elementos libres (no combinados) en la naturaleza.
Los metales alcalinos son todos brillantes, blandos y muy reactivos a temperatura y presión normal. Son maleables y se pueden cortar fácilmente debido a su escasa dureza, exponiendo una superficie brillante que se empaña rápidamente en el aire debido a la oxidación por la humedad atmosférica y el oxígeno (y en el caso de litio, por la presencia de nitrógeno también). Debido a su alta reactividad, deben ser almacenados en aceite para evitar la reacción con el aire, naturalmente se encuentran sólo como sales, nunca como los elementos libres. El cesio, quinto metal alcalino, es el más reactivo de todos los metales. En la nomenclatura moderna IUPAC, los metales alcalinos comprenden los elementos del grupo 1, salvo el hidrógeno (H), que nominalmente es un elemento del grupo 1, pero no se considera un metal alcalino, pero como el hidrógeno no tiene un lugar asignado entre los grupos del sistema periódico se le suele asignar el grupo 1. Todos los metales alcalinos reaccionan con el agua, los metales alcalinos más pesados más vigorosamente que los más ligeros.
Los compuestos típicos de los metales alcalinos son solubles en agua y están presentes en el agua de mar y en depósitos salinos. Como estos metales reaccionan rápidamente con el oxígeno, se venden en recipientes al vacío, pero por lo general se almacenan bajo aceite mineral queroseno. La configuración electrónica del grupo 1 o los metales alcalinos es ns¹. Por ello se dice que se encuentran en la zona "s" de la tabla periódica.
Todos los metales alcalinos descubiertos se encuentran en la naturaleza: en orden de abundancia, el sodio es el más abundante, seguido por el potasio, litio, rubidio, cesio y finalmente el francio, que es muy raro debido a su alta radioactividad y corta vida media; en la naturaleza el francio se encuentra como subproducto en la descomposición natural del actinio.
Se han realizado experimentos para intentar la síntesis del ununennio (119-Uue), que probablemente sea el próximo miembro del grupo, pero todos han sido infructuosos. Sin embargo, el 119 (ununennio) es posible que no se le pueda incluir en el grupo, lo que sí es cierto es que se prevé que tendrá una gran influencia en las propiedades químicas de los elementos superpesados; Incluso si se acepta como metal alcalino, se prevé que tenga diferencias en las propiedades físicas y químicas de sus homólogos más ligeros.
Referencias
1. Alcalino (https://books.google.com.sv/books?id=EdsLZGYbK-gC&pg=PA105), p. 105, en Google Libros
Obtenido de «https://es.wikipedia.org/wiki/Alcalino»
Alcalinos
 Los metales alcalinos o simplemente alcalinos (del árabe, alqali) son los seis elementos situados en el grupo I (1) de la tabla periódica1 (excepto el hidrógeno, que es un gas).
Los metales alcalinos o simplemente alcalinos (del árabe, alqali) son los seis elementos situados en el grupo I (1) de la tabla periódica1 (excepto el hidrógeno, que es un gas).
El grupo de los metales alcalinos están formados por los elementos que se sitúan en la primera columna (grupo) de la tabla periódica o sistema periódico, lo componen los elementos químicos litio (Li), sodio (Na), potasio (K), rubidio (Rb), cesio (Cs), francio (Fr). Pertenecen a la serie de elementos s, esto significa que los metales alcalinos tienen su electrón más externo en un orbital s, cada uno tiene solo un electrón en su nivel energético más externo (s), con buena tendencia a perderlo (esto es debido a que tienen poca afinidad electrónica, y baja energía de ionización), con lo que forman un catión monovalente, M+. Esta configuración electrónica compartida da como resultado que tengan propiedades características muy similares. De hecho, los metales alcalinos proporcionan el mejor ejemplo de tendencias de grupo en propiedades en la tabla periódica, con elementos que exhiben un comportamiento homólogo bien caracterizado.
Presentan densidades muy bajas y son buenos conductores de calor y de electricidad; reaccionan de inmediato con el agua, oxígeno y otras sustancias químicas, y nunca se les encuentra como elementos libres (no combinados) en la naturaleza.
Los metales alcalinos son todos brillantes, blandos y muy reactivos a temperatura y presión normal. Son maleables y se pueden cortar fácilmente debido a su escasa dureza, exponiendo una superficie brillante que se empaña rápidamente en el aire debido a la oxidación por la humedad atmosférica y el oxígeno (y en el caso de litio, por la presencia de nitrógeno también). Debido a su alta reactividad, deben ser almacenados en aceite para evitar la reacción con el aire, naturalmente se encuentran sólo como sales, nunca como los elementos libres. El cesio, quinto metal alcalino, es el más reactivo de todos los metales. En la nomenclatura moderna IUPAC, los metales alcalinos comprenden los elementos del grupo 1, salvo el hidrógeno (H), que nominalmente es un elemento del grupo 1, pero no se considera un metal alcalino, pero como el hidrógeno no tiene un lugar asignado entre los grupos del sistema periódico se le suele asignar el grupo 1. Todos los metales alcalinos reaccionan con el agua, los metales alcalinos más pesados más vigorosamente que los más ligeros.
Los compuestos típicos de los metales alcalinos son solubles en agua y están presentes en el agua de mar y en depósitos salinos. Como estos metales reaccionan rápidamente con el oxígeno, se venden en recipientes al vacío, pero por lo general se almacenan bajo aceite mineral queroseno. La configuración electrónica del grupo 1 o los metales alcalinos es ns¹. Por ello se dice que se encuentran en la zona "s" de la tabla periódica.
Todos los metales alcalinos descubiertos se encuentran en la naturaleza: en orden de abundancia, el sodio es el más abundante, seguido por el potasio, litio, rubidio, cesio y finalmente el francio, que es muy raro debido a su alta radioactividad y corta vida media; en la naturaleza el francio se encuentra como subproducto en la descomposición natural del actinio.
Se han realizado experimentos para intentar la síntesis del ununennio (119-Uue), que probablemente sea el próximo miembro del grupo, pero todos han sido infructuosos. Sin embargo, el 119 (ununennio) es posible que no se le pueda incluir en el grupo, lo que sí es cierto es que se prevé que tendrá una gran influencia en las propiedades químicas de los elementos superpesados; Incluso si se acepta como metal alcalino, se prevé que tenga diferencias en las propiedades físicas y químicas de sus homólogos más ligeros.
Referencias
1. Alcalino (https://books.google.com.sv/books?id=EdsLZGYbK-gC&pg=PA105), p. 105, en Google Libros
Obtenido de «https://es.wikipedia.org/wiki/Alcalino»
Alcalinotérreos
 Los metales alcalinotérreos son un grupo de elementos que se encuentran situados en el grupo 2 de la tabla periódica y son los siguientes: berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra). Este último no siempre se considera, pues tiene un tiempo de vida media corto.
Los metales alcalinotérreos son un grupo de elementos que se encuentran situados en el grupo 2 de la tabla periódica y son los siguientes: berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra). Este último no siempre se considera, pues tiene un tiempo de vida media corto.
El nombre «alcalinotérreos» proviene del nombre que recibían sus óxidos, «tierras», que tienen propiedades básicas (alcalinas). Poseen una electronegatividad ≤ 1,57 según la escala de Pauling.
Los alcalinotérreos son más duros que los metales alcalinos, tienen brillo y son buenos conductores eléctricos; menos reactivos que los alcalinos, buenos agentes reductores y forman compuestos iónicos. Todos ellos tienen dos electrones en su capa más externa (electrones de Valencia).
Características
- Tienen una configuración electrónica ns2.
- Tienen baja energía de ionización, aunque mayor que los alcalinos del mismo período, tanto menor si se desciende en el grupo.
- A excepción del berilio, forman compuestos claramente iónicos.
- Son metales de baja densidad, coloreados y blandos.
- La solubilidad de sus compuestos es bastante menor que sus correspondientes alcalinos.
- Todos tienen sólo dos electrones en su nivel energético más externo, con tendencia a perderlos, por su lado con lo que forman un ion positivo.
- Todos tienen como valencia +2.
- Se comportan como alcalinos y térreos al mismo tiempo.
Reacciones
Reaccionan con facilidad con halógenos para formar sales iónicas.
M + X2 —> MX2
Metales alcalinotérreos, obtención y aplicaciones
Existen dos métodos fundamentales de obtención:
Electrólisis de sus haluros fundidos: MX2(l) —> M(l) + X2(g). Reducción de sus óxidos con carbono: MO(s) + C(s) —> M(s) + CO(g)
El Berilio se emplea en la tecnología nuclear y en aleaciones de baja densidad, elevada solidez y estabilidad frente a la corrosión.
Referencias
1. Emsley, John (2001). Nature's Building Blocks: An A–Z Guide to the Elements. Oxford, England, UK: Oxford University Press. ISBN 0-19-850340-7.
Lantánidos
Los lantanoides (nombre recomendado por la IUPAC) o lantánidos son un grupo de elementos que forman parte del periodo 6 de la tabla periódica de los elementos. Estos elementos son llamados «tierras raras» debido a que se encuentran en forma de óxidos, y también, junto con los actínidos, forman los «elementos de transición interna».
El nombre procede del elemento químico lantano, que suele incluirse dentro de este grupo, dando un total de 15 elementos, desde el de número atómico 57 (el lantano) al 71 (el lutecio). Aunque se suela incluir en este grupo, el lantano no tiene electrones ocupando ningún orbital f, mientras que los catorce siguientes elementos tienen este orbital 4f parcial o totalmente lleno (véase configuración electrónica).
Estos elementos son químicamente bastante parecidos entre sí puesto que los electrones situados en orbitales f son poco importantes en los enlaces que forman, en comparación con los de p y d. También son bastante parecidos a los lantánidos los elementos itrio y escandio, debido a que tienen un radio similar y, al igual que los lantánidos, su estado de oxidación más importante es el +3. Éste es el estado de oxidación más importante de los lantánidos, pero también presentan el estado de oxidación +2 y +4.
La abundancia de estos elementos en la corteza terrestre es relativamente alta, en minerales como por ejemplo la monacita, en la cual se encuentran distintos lantánidos e itrio.
En la tabla periódica, estos elementos se suelen situar debajo del resto, junto con los actínidos, dando una tabla más compacta que si se colocaran entre los elementos del bloque s y los del bloque d, aunque en algunas tablas periódicas sí que se pueden ver situados entre estos bloques, dando una tabla mucho más ancha.
El radio de los lantánidos va disminuyendo conforme aumenta el número atómico; no son variaciones grandes, pero se van acumulando. Esto provoca que los elementos del bloque d de la segunda y tercera serie de transición presenten radios similares dentro de un grupo: deberían aumentar al bajar en un grupo, pero al haberse intercalado los lantánidos, este aumento en el radio por bajar dentro de un grupo se ve contrarrestado por la disminución del radio por la presencia de los lantánidos. Esto se conoce como contracción de los lantánidos.
Propiedades magnéticas y espectrales
Varios de los aspectos del comportamiento magnético y espectral de los lantánidos difieren fundamentalmente de los del bloque de correspondiente a los elementos de transición. La razón básica de estas diferencias reside en que los electrones que son responsables de las propiedades de los iones lantánidos son electrones 4f, y que los orbitales 4f están protegidos muy efectivamente de la influencia de fuerzas externas en las capas externas 5s2 y 5p6. Es por ello que los estados que se originan desde las diversas configuraciones 4fn sólo son ligeramente afectados por el medio que rodea a los iones y permanecen prácticamente invariables para determinado ion en todos sus compuestos.
Las constantes de acoplamiento de spin-órbita son bastante grandes. Esto tiene por consecuencia que, salvo unas cuantas excepciones, los iones lantánidos posean estados fundamentales con un solo y bien definido valor del momento angular total J, con el siguiente estado inferior de J, y con energías muchas veces mayores que el valor de KT, y por consiguiente el estado superior está virtualmente no poblado.
Los colores y estados electrónicos fundamentales de los iones M3+ se dan en la tabla que se encuentra a continuación; la consecuencia de los colores en la serie del lantano al gadolinio se repiten accidentalmente en la serie del lutecio al gadolinio. Como ha quedado implícito en las explicaciones anteriores, los colores se deben a transiciones f-f , las cuales son virtualmente independientes del entorno exterior de iones.
Referencias
1. Gray, Theodore (2009). The Elements: A Visual Exploration of Every Known Atom in the Universe. New York: Black Dog & Leventhal Publishers. p. 240. ISBN 978-1-57912-814-2.
Tabla Periódica
La tabla periódica de los elementos es una disposición de los elementos químicos en forma de tabla, ordenados por su número atómico (número de protones), por su configuración de electrones y sus propiedades químicas. Este ordenamiento muestra tendencias periódicas, como elementos con comportamiento similar en la misma columna.
Las filas de la tabla se denominan períodos y las columnas grupos. Algunos grupos tienen nombres. Así por ejemplo el grupo 17 es el de los halógenos y el grupo 18 el de los gases nobles. La tabla también se divide en cuatro bloques con algunas propiedades químicas similares. Debido a que las posiciones están ordenadas, se puede utilizar la tabla para obtener relaciones entre las propiedades de los elementos, o pronosticar propiedades de elementos nuevos todavía no descubiertos o sintetizados. La tabla periódica proporciona un marco útil para analizar el comportamiento químico y es ampliamente utilizada en química y otras ciencias.
Dmitri Mendeléyev publicó en 1869 la primera versión de tabla periódica que fue ampliamente reconocida. La desarrolló para ilustrar tendencias periódicas en las propiedades de los elementos entonces conocidos, al ordenar los elementos basándose en sus propiedades químicas, si bien Julius Lothar Meyer, trabajando por separado, llevó a cabo un ordenamiento a partir de las propiedades físicas de los átomos. Mendeléyev también pronosticó algunas propiedades de elementos entonces desconocidos que anticipó que ocuparían los lugares vacíos en su tabla. Posteriormente se demostró que la mayoría de sus predicciones eran correctas cuando se descubrieron los elementos en cuestión.
MANUAL
Cuando colocas el cursor sobre cada elemento podrá ver un detalle ampliado en la sección que se muestra a continuación:
Puedes hacer clic con el cursor sobre cada elemento/categoría/orden/grupo para ver su artículo informativo asociado:

Los artículos publicados en esta web referentes a los elementos de la tabla periódica son cortesía:
Dayah, M. (1997, Cotubre 1). Ptable: Tabla Periódica. Ptable. https://ptable.com/